Steroid 11β-Hydroxylase - Steroid 11β-hydroxylase
| Steroid 11β-Monooxygenase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifikatoren | |||||||||
| EG-Nr. | 1.14.15.4 | ||||||||
| CAS-Nr. | 9029-66-7 | ||||||||
| Datenbanken | |||||||||
| IntEnz | IntEnz-Ansicht | ||||||||
| BRENDA | BRENDA-Eintrag | ||||||||
| ExPASy | NiceZyme-Ansicht | ||||||||
| KEGG | KEGG-Eintrag | ||||||||
| MetaCyc | Stoffwechselweg | ||||||||
| PRIAM | Profil | ||||||||
| PDB- Strukturen | RCSB PDB PDBe PDBsum | ||||||||
| Gen-Ontologie | AmiGO / QuickGO | ||||||||
| |||||||||
| CYP11B1 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Identifikatoren | |||||||||||||||||||||||||
| Aliase | CYP11B1 , CPN1, CYP11B, FHI, P450C11, Cytochrom P450 Familie 11 Unterfamilie B Mitglied 1 | ||||||||||||||||||||||||
| Externe IDs | OMIM : 610613 MGI : 88.584 Homologene : 128035 Genecards : CYP11B1 | ||||||||||||||||||||||||
| EG-Nummer | 1.14.15.4 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Orthologe | |||||||||||||||||||||||||
| Spezies | Menschlich | Maus | |||||||||||||||||||||||
| Entrez | |||||||||||||||||||||||||
| Ensemble | |||||||||||||||||||||||||
| UniProt | |||||||||||||||||||||||||
| RefSeq (mRNA) | |||||||||||||||||||||||||
| RefSeq (Protein) | |||||||||||||||||||||||||
| Standort (UCSC) | Chr 8: 142,87 – 142,88 Mb | n / A | |||||||||||||||||||||||
| PubMed- Suche | |||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
Steroid 11β-Hydroxylase , auch bekannt als Steroid 11β-Monooxygenase , ist eine Steroidhydroxylase, die in der Zona glomerulosa und Zona fasciculata der Nebennierenrinde vorkommt . Offiziell als Cytochrom P450 11B1 bezeichnet, mitochondrial , ist es ein Protein , das beim Menschen vom CYP11B1- Gen kodiert wird . Das Enzym wird in der Biosynthese beteiligten adrenale Corticosteroide durch Katalyse der Addition von Hydroxylgruppen bei Oxidationsreaktionen.
Gen
Das CYP11B1- Gen kodiert für 11β-Hydroxylase – ein Mitglied der Cytochrom-P450- Enzym- Superfamilie . Die Cytochrom-P450-Proteine sind Monooxygenasen , die viele Reaktionen katalysieren, die am Arzneimittelstoffwechsel und an der Synthese von Cholesterin , Steroiden und anderen Lipiden beteiligt sind . Das Produkt dieses CYP11B1-Gens ist das 11β-Hydroxylase-Protein. Dieses Protein lokalisiert an der mitochondrialen Innenmembran und ist an der Umwandlung verschiedener Steroide in der Nebennierenrinde beteiligt. Für dieses Gen wurden Transkriptvarianten festgestellt, die für verschiedene Isoformen kodieren .
Das CYP11B1- Gen wird durch Etomidat und Metyrapon reversibel gehemmt .
Funktion
11β-Hydroxylase ist ein steroidogenes Enzym , dh das Enzym, das am Stoffwechsel von Steroiden beteiligt ist .
Der Mensch besitzt zwei Isozyme mit 11β-Hydroxylase-Aktivität: CYP11B1 und CYP11B2.
CYP11B1 (11β-Hydroxylase) wird in hohen Konzentrationen exprimiert und durch ACTH reguliert , während CYP11B2 ( Aldosteronsynthase ) normalerweise in niedrigen Konzentrationen exprimiert und durch Angiotensin II reguliert wird . Neben der 11β-Hydroxylase-Aktivität weisen beide Isozyme 18-Hydroxylase-Aktivität auf. Das CYP11B1-Isozym hat eine starke 11β-Hydroxylase-Aktivität, aber die Aktivität von 18-Hydroxylase beträgt nur ein Zehntel von CYP11B2. Die schwache 18-Hydroxylase-Aktivität von CYP11B1 erklärt, warum eine Nebenniere mit unterdrückter CYP11B2-Expression weiterhin 18-Hydroxycorticosteron synthetisiert .
Hier sind einige der Steroide, gruppiert nach der katalytischen Aktivität des CYP11B1-Isozyms:
- starke Aktivität:
- mittlere Aktivität:
- schwache Aktivität:
Außerdem kann 11β-Hydroxylase am Metabolismus von 17α-Hydroxyprogesteron zu 21-Desoxycortisol beteiligt sein , insbesondere bei einem Mangel an 21-Hydroxylase .
Cortisol- und Corticosteron-Stoffwechsel
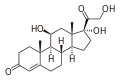
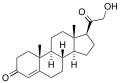
11β-Hydroxylase hat eine starke katalytische Aktivität während der Umwandlung von 11-Desoxycortisol zu Cortisol und 11-Desoxycorticosteron zu Corticosteron , indem sie die Hydroxylierung der Kohlenstoff-Wasserstoff-Bindung an der 11-Beta-Position katalysiert. Beachten Sie das zusätzliche "–OH", das an der 11-Position hinzugefügt wurde (in der Nähe der Mitte, auf Ring "C"):
Wirkmechanismus
Als mitochondriales P450-System ist P450c11 von zwei Elektronentransferproteinen abhängig, Adrenodoxinreduktase und Adrenodoxin, die für jede durch das Enzym katalysierte Monooxygenasereaktion 2 Elektronen von NADPH auf P450 übertragen. In den meisten Hinsichten scheint dieser Vorgang des Elektronentransfers dem des P450scc- Systems ähnlich zu sein, das die Spaltung der Cholesterin-Seitenkette katalysiert. Ähnlich wie bei P450scc ist der Vorgang des Elektronentransfers undicht, was zur Bildung von Superoxid führt. Die Rate des Elektronenlecks während des Metabolismus hängt von den funktionellen Gruppen des Steroidsubstrats ab.
Verordnung
Die Expression des Enzyms in Nebennierenrindenzellen wird durch das trophische Hormon Corticotropin ( ACTH ) reguliert .
Klinische Bedeutung
Eine Mutation ist mit einer angeborenen Nebennierenhyperplasie aufgrund eines 11β-Hydroxylase-Mangels verbunden .
Siehe auch
Zusätzliche Bilder

Verweise
Weiterlesen
- Helmberg A (August 1993). „Zwillinge und endokrine Erkrankungen: CYP21- und CYP11B-Gene“. Acta-Endocrinol . 129 (2): 97–108. doi : 10.1530/acta.0.1290097 . PMID 8372604 .
- Stowasser M, Gunasekera TG, Gordon RD (Dezember 2001). „Familienvarianten des primären Aldosteronismus“. Klin. Erw. Pharmacol. Physiol . 28 (12): 1087–90. doi : 10.1046/j.1440-1681.2001.03574.x . PMID 11903322 . S2CID 23091842 .
- Helmberg A, Ausserer B, Kofler R (November 1992). „Frameshift durch Insertion von 2 Basenpaaren in Codon 394 von CYP11B1 verursacht kongenitale Nebennierenhyperplasie aufgrund eines Steroid-11-Beta-Hydroxylase-Mangels“. J. Clin. Endokrinol. Metab . 75 (5): 1278–81. doi : 10.1210/jc.75.5.1278 . PMID 1430088 .
- Pascoe L, Curnow KM, Slutsker L, Connell JM, Speiser PW, New MI, White PC (September 1992). „Glucocorticoid-unterdrückbar Hyperaldosteronismus resultiert aus Hybridgen durch ungleichen Crossovers zwischen CYP11B1 und CYP11B2 erstellt“ . Proz. Natl. Akad. Wissenschaft USA . 89 (17): 8327–31. Bibcode : 1992PNAS...89.8327P . doi : 10.1073/pnas.89.17.8327 . PMC 49911 . PMID 1518866 .
- T. Kawamoto, Y. Mitsuuchi, K. Toda, Y. Yokoyama, K. Miyahara, S. Miura, T. Ohnishi, Y. Ichikawa, K. Nakao, H. Imura (Februar 1992). "Rolle von Steroid 11 Beta-Hydroxylase und Steroid 18-Hydroxylase bei der Biosynthese von Glukokortikoiden und Mineralokortikoiden beim Menschen" . Proz. Natl. Akad. Wissenschaft USA . 89 (4): 1458–62. Bibcode : 1992PNAS...89.1458K . doi : 10.1073/pnas.89.4.1458 . PMC 48470 . PMID 1741400 .
- White PC, Dupont J, New MI, Leiberman E, Hochberg Z, Rösler A (Mai 1991). "Eine Mutation in CYP11B1 (Arg-448----His) im Zusammenhang mit Steroid-11-Beta-Hydroxylase-Mangel bei Juden marokkanischen Ursprungs" . J. Clin. Investieren . 87 (5): 1664–7. doi : 10.1172/JCI115182 . PMC 295260 . PMID 2022736 .
- T. Kawamoto, Y. Mitsuuchi, K. Toda, K. Miyahara, Y. Yokoyama, K. Nakao, K. Hosoda, Y. Yamamoto, H. Imura, Y. Shizuta (September 1990). "Klonierung von cDNA und genomischer DNA für menschliches Cytochrom P-45011 beta" . FEBS Lett . 269 (2): 345–9. doi : 10.1016/0014-5793(90)81190-Y . PMID 2401360 . S2CID 35151332 .
- Mornet E, Dupont J, Vitek A, White PC (Dezember 1989). "Charakterisierung von zwei Genen, die das menschliche Steroid 11-beta-Hydroxylase (P-450(11) beta) codieren" . J. Biol. Chem . 264 (35): 20961–7. doi : 10.1016/S0021-9258(19)30030-4 . PMID 2592361 .
- Chua SC, Szabo P, Vitek A, Grzeschik KH, John M, White PC (Oktober 1987). "Klonierung von cDNA, die für Steroid 11-beta-Hydroxylase (P450c11) kodiert" . Proz. Natl. Akad. Wissenschaft USA . 84 (20): 7193–7. Bibcode : 1987PNAS...84.7193C . doi : 10.1073/pnas.84.20.7193 . PMC 299256 . PMID 3499608 .
- Y. Naiki, T. Kawamoto, Y. Mitsuuchi, K. Miyahara, K. Toda, T. Orii, H. Imura, Y. Shizuta (Dezember 1993). "Eine Nonsense-Mutation (TGG [Trp116] --> TAG [Stop]) in CYP11B1 verursacht Steroid-11-Beta-Hydroxylase-Mangel". J. Clin. Endokrinol. Metab . 77 (6): 1677–82. doi : 10.1210/jc.77.6.1677 . PMID 7903314 .
- Joehrer K., Geley S., Strasser-Wozak EM, Azziz R, Wollmann HA, Schmitt K, Kofler R, White PC (Oktober 1997). „CYP11B1-Mutationen verursachen nicht-klassische Nebennierenhyperplasie aufgrund eines 11-Beta-Hydroxylase-Mangels“ . Summen. Mol.-Nr. Genet . 6 (11): 1829–34. doi : 10.1093/hmg/6.11.1829 . PMID 9302260 .
- Cargill M, Altshuler D, Irland J, Sklar P, Ardlie K, Patil N, Shaw N, Lane CR, Lim EP, Kalyanaraman N, Nemesh J, Ziaugra L, Friedland L, Rolfe A, Warrington J, Lipshutz R, Daley GQ , Lander ES (Juli 1999). „Charakterisierung von Single-Nukleotid-Polymorphismen in kodierenden Regionen menschlicher Gene“. Nat. Genet . 22 (3): 231–8. doi : 10.1038/10290 . PMID 10391209 . S2CID 195213008 .
- Halushka MK, Fan JB, Bentley K, Hsie L, Shen N, Weder A, Cooper R, Lipshutz R, Chakravarti A (Juli 1999). „Muster von Single-Nukleotid-Polymorphismen in Kandidatengenen für die Blutdruckhomöostase“. Nat. Genet . 22 (3): 239–47. doi : 10.1038/10297 . PMID 10391210 . S2CID 4636523 .
- Cao PR, Bernhardt R. (Juni 1999). "Interaktion von CYP11B1 (Cytochrom P-45011 beta) mit CYP11A1 (Cytochrom P-450scc) in COS-1-Zellen" . EUR. J. Biochem . 262 (3): 720–6. doi : 10.1046/j.1432-1327.1999.00414.x . PMID 10411633 .
- L. Loidi, C. Quinteiro, F. Barros, F. Domínguez, J. Barreiro, M. Pombo (Dezember 1999). "Die C494F-Variante im CYP11B1-Gen ist ein Sequenzpolymorphismus in der spanischen Bevölkerung" . J. Clin. Endokrinol. Metab . 84 (12): 4749. doi : 10.1210/jc.84.12.4749 . PMID 10599751 .
- O Chabre, S. Portrat-Doyen, P. Chaffanjon, J. Vivier, P. Liakos, F. Labat-Moleur, E. Chambaz, Y. Morel, G. Defaye (November 2000). „Bilaterale laparoskopische Adrenalektomie bei kongenitaler Nebennierenhyperplasie mit schwerer Hypertonie, resultierend aus zwei neuen Mutationen in Spleißspenderstellen von CYP11B1“ . J. Clin. Endokrinol. Metab . 85 (11): 4060–8. doi : 10.1210/jc.85.11.4060 . PMID 11095433 .
- Fisher A, Friel EC, Bernhardt R, Gomez-Sanchez C, Connell JM, Fraser R, Davies E (September 2001). „Auswirkungen von 18-hydroxylierten Steroiden auf die Kortikosteroidproduktion durch menschliche Aldosteronsynthase und 11beta-Hydroxylase“. J. Clin. Endokrinol. Metab . 86 (9): 4326–9. doi : 10.1210/jc.86.9.4326 . PMID 11549669 .
- Hampf M., Dao NT, Hoan NT, Bernhardt R. (September 2001). „Ungleiche Kreuzung zwischen Aldosteronsynthase und 11beta-Hydroxylase-Genen verursacht angeborene Nebennierenhyperplasie“. J. Clin. Endokrinol. Metab . 86 (9): 4445–52. doi : 10.1210/jc.86.9.4445 . PMID 11549691 .
Externe Links
- Steroid+11-Beta-Hydroxylase bei der US National Library of Medicine Medical Subject Headings (MeSH)