AGR1 - EGR1
EGR-1 (Early Growth Response Protein 1), auch bekannt als ZNF268 (Zinkfinger Protein 268) oder NGFI-A (Nervenwachstumsfaktor-induziertes Protein A) ist ein Protein , das beim Menschen vom EGR1- Gen kodiert wird .
EGR-1 ist ein Säugetier- Transkriptionsfaktor . Es wurde auch Krox-24, TIS8 und ZENK genannt . Es wurde ursprünglich bei Mäusen entdeckt .
Funktion
Das von diesem Gen kodierte Protein gehört zur EGR-Familie der Zinkfingerproteine vom Cys 2 His 2 -Typ . Es ist ein Kernprotein und fungiert als Transkriptionsregulator. Die Produkte der aktivierten Zielgene werden für die Differenzierung und Mitogenese benötigt . Studien legen nahe, dass dies ein Tumorsuppressorgen ist .
Es hat ein ausgeprägtes Expressionsmuster im Gehirn, und seine Induktion ist mit neuronaler Aktivität verbunden. Mehrere Studien legen nahe, dass es eine Rolle bei der neuronalen Plastizität spielt .
EGR-1 ist ein wichtiger Transkriptionsfaktor in Speicherbildung. Es hat eine wesentliche Rolle im Gehirn Neuronen epigenetische Reprogrammierung. EGR-1 rekrutiert das TET1- Protein, das einen Weg der DNA-Demethylierung einleitet . Das Entfernen von DNA-Methylierungsmarkierungen ermöglicht die Aktivierung nachgeschalteter Gene. EGR-1 wird zusammen mit TET1 bei der Programmierung der Verteilung von Methylierungsstellen auf der Gehirn-DNA während der Gehirnentwicklung, beim Lernen und bei der langfristigen neuronalen Plastizität eingesetzt . Es wurde auch festgestellt, dass EGR-1 die Expression von VAMP2 (einem Protein, das für die synaptische Exozytose wichtig ist ) reguliert .
Neben seiner Funktion im Nervensystem gibt es signifikante Hinweise darauf, dass EGR-1 zusammen mit seinem Paralog EGR-2 bei fibrotischen Erkrankungen induziert wird, Schlüsselfunktionen bei der Fibrinogenese hat und für die experimentell induzierte Fibrose bei Mäusen notwendig ist.
Es kann auch an der Eierstockfunktion beteiligt sein
Struktur
Die DNA-bindende Domäne von EGR-1 besteht aus drei Zinkfingerdomänen vom Cys 2 His 2 Typ. Die Aminosäurestruktur der EGR-1-Zinkfingerdomäne ist in dieser Tabelle unter Verwendung des Einzelbuchstaben-Aminosäurecodes angegeben. Die Finger 1 bis 3 sind mit f1 - f3 gekennzeichnet. Die Zahlen beziehen sich auf die Reste (Aminosäuren) der Alpha-Helix (es gibt keine Null). Die mit „x“ gekennzeichneten Reste gehören nicht zu den Zinkfingern, sondern dienen dazu, sie alle miteinander zu verbinden.
| -1 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | x | x | x | x | x | |||||||||||||||||||||||
| f1 | m | EIN | E | E | R | P | Ja | EIN | C | P | V | E | S | C | D | R | R | F | S | R | S | D | E | L | T | R | h | ich | R | ich | h | T | g | Q | K | P | |
| f2 | F | Q | C | EIN | ich | - | - | C | m | R | n | F | S | R | S | D | h | L | T | T | h | ich | EIN | T | h | T | g | E | K | P | |||||||
| f3 | F | EIN | C | D | ich | - | - | C | g | R | K | F | EIN | R | S | D | E | R | K | R | h | T | K | ich | h | L | R | Q | K | D |
Aminosäureschlüssel: Alanin (Ala, A), Arginin (Arg, R), Asparagin (Asn, N), Asparaginsäure (Asp, D), Cystein (Cys, C), Glutaminsäure (Glu, E), Glutamin ( Gln, Q), Glycin (Gly, G), Histidin (His, H), Isoleucin (Ile, I), Leucin (Leu, L), Lysin (Lys, K), Methionin (Met, M), Phenylalanin (Phe , F), Prolin (Pro, P), Serin (Ser, S), Threonin (Thr, T), Tryptophan (Trp, W), Tyrosin (Tyr, Y), Valin (Val, V)
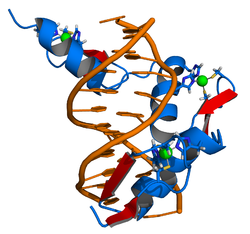
Die Kristallstruktur der DNA , die durch die Zinkfingerdomäne von EGR-1 gebunden ist, wurde 1991 aufgeklärt, was die frühe Forschung an DNA-bindenden Zinkfingerdomänen stark unterstützte.
Das menschliche EGR-1-Protein enthält (in seiner unverarbeiteten Form) 543 Aminosäuren mit einem Molekulargewicht von 57,5 kDa und das Gen befindet sich auf dem Chromosom 5 .
DNA-Bindungsspezifität
EGR-1 bindet die DNA-Sequenz 5'-GCG TGG GCG-3' (und ähnliche wie 5'-GCG GGG GCG-3'). Die f1-Position 6 bindet das 5'-G (die erste Basenzählung von links); die f1-Position 3 zur zweiten Base (C); f1-Position -1 bindet an die dritte Position (G); f2 Position 6 zur vierten Base (T); und so weiter.
Interaktionen
Es wurde gezeigt, dass EGR-1 interagiert mit:
Siehe auch
Verweise
Weiterlesen
- Heath RG (März 1975). „Gehirnfunktion und Verhalten. I. Emotion und sensorische Phänomene bei psychotischen Patienten und bei Versuchstieren“. Das Journal für Nerven- und Geisteskrankheiten . 160 (3): 159–75. doi : 10.1097/00005053-197503000-00002 . PMID 1090709 . S2CID 23024944 .
- Silverman ES, Collins T (März 1999). „Wege der Egr-1-vermittelten Gentranskription in der Gefäßbiologie“ . Das American Journal of Pathology . 154 (3): 665–70. doi : 10.1016/S0002-9440(10)65312-6 . PMC 1866415 . PMID 10079243 .
- Adamson ED, Mercola D (2002). „Egr1-Transkriptionsfaktor: mehrere Rollen im Wachstum und Überleben von Prostatatumorzellen“. Tumorbiologie . 23 (2): 93–102. doi : 10.1159/000059711 . PMID 12065847 . S2CID 46795197 .
- Blaschke F, Bruemmer D, Law RE (August 2004). "Egr-1 ist ein wichtiger vaskulärer pathogener Transkriptionsfaktor bei Atherosklerose und Restenose". Bewertungen in Endokrine und metabolische Störungen . 5 (3): 249–54. doi : 10.1023/B:REMD.0000032413.88756.ee . PMID 15211096 . S2CID 11968305 .
- Abdulkadir SA (November 2005). „Mechanismen der Prostatatumorogenese: Rollen für die Transkriptionsfaktoren Nkx3.1 und Egr1“. Annalen der New Yorker Akademie der Wissenschaften . 1059 : 33–40. doi : 10.1196/annals.1339.018 . PMID 16382041 . S2CID 6774788 .
- Khachigian LM (Februar 2006). "Frühe Wachstumsreaktion-1 in der kardiovaskulären Pathobiologie" . Kreislaufforschung . 98 (2): 186–91. doi : 10.1161/01.RES.0000200177.53882.c3 . PMID 16456111 .
Externe Links
- Zif+268+protein,+human an der US National Library of Medicine Medical Subject Headings (MeSH)
- FactorBook Egr-1
- Übersicht über alle in der PDB verfügbaren Strukturinformationen für UniProt : P18146 (Human Early growth response protein 1) an der PDBe-KB .
- Übersicht über alle in der PDB verfügbaren Strukturinformationen für UniProt : P08046 (Mouse Early growth response protein 1) an der PDBe-KB .