Marfan-Syndrom - Marfan syndrome
| Marfan-Syndrom | |
|---|---|
| Andere Namen | Marfan-Syndrom |
 | |
| Ectopie lentis bei Marfan-Syndrom: Zonulafasern sind zu sehen. | |
| Spezialität | Medizinische Genetik |
| Symptome | Großer, schlanker Körperbau; lange Arme, Beine und Finger; flexible Finger und Zehen |
| Komplikationen | Skoliose , Mitralklappenprolaps , Aortenaneurysma |
| Dauer | Langfristig |
| Ursachen | Genetisch ( autosomal-dominant ) |
| Diagnosemethode | Gent Kriterien |
| Differenzialdiagnose | Loeys-Dietz-Syndrom , Ehlers-Danlos-Syndrom |
| Medikation | Betablocker , Calciumkanalblocker , ACE-Hemmer |
| Prognose | Oft normale Lebenserwartung |
| Frequenz | 1 von 5.000–10.000 |
Das Marfan-Syndrom ( MFS ) ist eine genetische Störung , die das Bindegewebe betrifft . Diejenigen mit dieser Erkrankung sind in der Regel groß und dünn, mit langen Armen, Beinen, Fingern und Zehen . Sie haben typischerweise auch zu flexible Gelenke und Skoliose . Die schwerwiegendsten Komplikationen betreffen das Herz und die Aorta , mit einem erhöhten Risiko für einen Mitralklappenprolaps und ein Aortenaneurysma . Auch Lunge, Augen, Knochen und die Bedeckung des Rückenmarks sind häufig betroffen. Die Schwere der Symptome von MFS ist variabel.
MFS wird durch eine Mutation in FBN1 verursacht , einem der Gene, die Fibrillin bilden , was zu abnormalem Bindegewebe führt. Es handelt sich um eine autosomal-dominante Erkrankung. Ungefähr 75 % der Zeit wird die Erkrankung von einem Elternteil mit der Erkrankung geerbt, während es sich in 25 % der Fälle um eine neue Mutation handelt. Die Diagnose basiert oft auf den Genter Kriterien .
Es gibt keine bekannte Heilung für MFS. Viele Betroffene haben bei richtiger Behandlung eine normale Lebenserwartung. Die Behandlung umfasst häufig die Anwendung von Betablockern wie Propranolol oder Atenolol oder, wenn diese nicht vertragen werden, Kalziumkanalblockern oder ACE-Hemmern . Eine Operation kann erforderlich sein, um die Aorta zu reparieren oder eine Herzklappe zu ersetzen . Menschen mit dieser Erkrankung wird empfohlen, anstrengende Übungen zu vermeiden.
Ungefähr 1 von 5.000 bis 1 von 10.000 Menschen haben MFS. Die Raten der Erkrankung sind in verschiedenen Regionen der Welt ähnlich. Es ist nach dem französischen Kinderarzt Antoine Marfan benannt , der es 1896 erstmals beschrieb.
Anzeichen und Symptome

Mehr als 30 Anzeichen und Symptome sind unterschiedlich mit dem Marfan-Syndrom verbunden. Die bekanntesten davon betreffen das Skelett-, Herz-Kreislauf- und Augensystem, aber das gesamte faserige Bindegewebe im ganzen Körper kann betroffen sein.
Skelettsystem
Die meisten der gut sichtbaren Zeichen sind mit dem Skelettsystem verbunden . Viele Menschen mit Marfan-Syndrom werden überdurchschnittlich groß und einige haben überproportional lange, schlanke Gliedmaßen mit dünnen, schwachen Handgelenken und langen Fingern und Zehen .
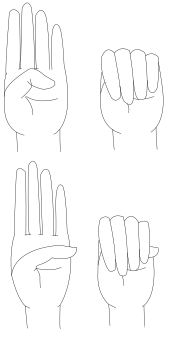
Das Steinberg-Zeichen, auch Daumenzeichen genannt, ist einer der klinischen Untersuchungstests für die Marfan-Krankheit an den Händen. Es ist ein klinischer Test, bei dem die Daumenspitze medial des kleinen Fingers sichtbar ist, wenn sie in der geballten Hand gehalten wird. [ [1] ]
Abgesehen von der Beeinträchtigung der Größe und der Gliedmaßenproportionen können Menschen mit Marfan-Syndrom eine abnormale seitliche Krümmung der Wirbelsäule (Skoliose), eine Thoraxlordose , eine abnormale Einbuchtung ( Pectus Excatum ) oder eine Vorwölbung (Pectus Carinatum) des Brustbeins , eine abnormale Gelenkflexibilität , ein hochgewölbtes Gaumen mit zusammengedrängten Zähnen und einem Überbiss, Plattfüßen , Hammerzehen , gebeugten Schultern und unerklärlichen Dehnungsstreifen auf der Haut. Es kann auch Schmerzen in den Gelenken, Knochen und Muskeln verursachen. Einige Menschen mit Marfan haben Sprachstörungen aufgrund von symptomatischen hohen Gaumen und kleinen Kiefern. Frühe Arthrose kann auftreten. Andere Anzeichen sind eine eingeschränkte Beweglichkeit der Hüften, da der Hüftkopf in ungewöhnlich tiefe Hüftpfannen ragt .
Augen
Beim Marfan-Syndrom kann die Gesundheit des Auges in vielerlei Hinsicht beeinträchtigt werden, aber die Hauptveränderung ist eine partielle Linsendislokation , bei der die Linse aus ihrer normalen Position verschoben wird. Dies geschieht aufgrund einer Schwäche der Ziliarzonula , der Bindegewebsstränge, die die Linse im Auge aufhängen . Die für das Marfan-Syndrom verantwortlichen Mutationen schwächen die Zonula und bewirken, dass sie sich dehnen. Die unteren Zonulae werden am häufigsten gestreckt, was dazu führt, dass sich die Linse nach oben und außen verschiebt, sie kann sich aber auch in andere Richtungen verschieben. Kurzsichtigkeit (Myopie) und verschwommenes Sehen sind häufig aufgrund von Bindegewebsdefekten im Auge. Auch Weitsichtigkeit kann auftreten, insbesondere wenn die Linse stark subluxiert ist. Eine Subluxation (partielle Luxation) der Linse kann bei etwa 60 % der Menschen mit Marfan-Syndrom mit einem Spaltlampen- Biomikroskop klinisch nachgewiesen werden . Wenn die Linsensubluxation subtil ist, kann eine Bildgebung mit hochauflösender Ultraschall-Biomikroskopie verwendet werden.
Andere Anzeichen und Symptome, die das Auge betreffen, umfassen eine vergrößerte Länge entlang einer Achse des Augapfels , Myopie, Hornhautflachheit, Strabismus , Exotropie und Esotropie . Menschen mit MFS haben auch ein hohes Risiko für frühes Glaukom und frühe Katarakte .
Herz-Kreislauf-System
Die schwerwiegendsten Zeichen und mit Marfan - Syndrom Symptome beinhalten das Herz - Kreislauf - System : übermäßige Müdigkeit , Atemnot , Herzklopfen , Rennen Herzschlag oder Brustschmerzen mit Ausstrahlung in dem Rücken, Schulter oder Arm. Auch kalte Arme, Hände und Füße können wegen unzureichender Durchblutung mit MFS in Verbindung gebracht werden. Ein Herzgeräusch , ein anormaler Ablesewert auf einem EKG oder Symptome einer Angina pectoris können auf weitere Untersuchungen hinweisen. Die Anzeichen einer Regurgitation durch einen Prolaps der Mitral- oder Aortenklappen (die den Blutfluss durch das Herz steuern) resultieren aus einer zystischen medialen Degeneration der Klappen, die häufig mit MFS verbunden ist (siehe Mitralklappenprolaps , Aorteninsuffizienz ). Das wichtigste Anzeichen, das einen Arzt jedoch dazu veranlassen würde, eine Grunderkrankung in Betracht zu ziehen, ist eine erweiterte Aorta oder ein Aortenaneurysma . Manchmal sind keine Herzprobleme erkennbar, bis die Schwächung des Bindegewebes (zystische mediale Degeneration) in der Aorta ascendens ein Aortenaneurysma oder eine Aortendissektion , einen chirurgischen Notfall, verursacht. Eine Aortendissektion ist meistens tödlich und führt zu Schmerzen, die in den Rücken ausstrahlen und ein reißendes Gefühl verursachen.
Da zugrunde liegende Anomalien des Bindegewebes MFS verursachen, ist die Inzidenz einer Dehiszenz der Mitralklappenprothese erhöht. Es sollte darauf geachtet werden, dass beschädigte Herzklappen eher repariert als ersetzt werden.
Lunge
Personen mit Marfan-Syndrom können von verschiedenen Lungenproblemen betroffen sein. Eine Studie ergab, dass nur 37 % der untersuchten Patientenstichprobe (mittleres Alter 32 ± 14 Jahre; M 45 %) eine normale Lungenfunktion aufwiesen. Ein spontaner Pneumothorax ist häufig. Beim spontanen einseitigen Pneumothorax entweicht Luft aus einer Lunge und besetzt den Pleuraraum zwischen der Brustwand und einer Lunge. Die Lunge wird teilweise komprimiert oder kollabiert. Dies kann zu Schmerzen, Kurzatmigkeit, Zyanose und, wenn nicht behandelt, zum Tod führen. Andere mögliche pulmonale Manifestationen des MFS sind Schlafapnoe und idiopathische obstruktive Lungenerkrankung. Pathologische Veränderungen in der Lunge wurden beschrieben, wie zystische Veränderungen, Emphysem , Pneumonie , Bronchiektasen , Blasen , apikale Fibrose und angeborene Fehlbildungen wie Mittellappenhypoplasie.
Nervöses System
Die Duralektasie , die Schwächung des Bindegewebes des das Rückenmark umgebenden Duralsacks , kann zu einem Verlust an Lebensqualität führen . Sie kann über einen langen Zeitraum bestehen bleiben, ohne erkennbare Symptome hervorzurufen. Symptome, die auftreten können, sind Kreuzschmerzen, Beinschmerzen, Bauchschmerzen, andere neurologische Symptome in den unteren Extremitäten oder Kopfschmerzen – Symptome, die normalerweise beim Liegen nachlassen. Auf dem Röntgenbild ist eine Dura-Ektasie jedoch im Frühstadium nicht oft sichtbar. Eine Verschlechterung der Symptome kann eine MRT der unteren Wirbelsäule rechtfertigen . Eine bis zu diesem Stadium fortgeschrittene Duralektasie würde in einem MRT als ein erweiterter Beutel erscheinen, der sich an den Lendenwirbeln abnutzt . Andere Rückenprobleme im Zusammenhang mit MFS gehören degenerative Bandscheibenerkrankungen , Rücken Zysten und Dysfunktion des autonomen Nervensystems .
Genetik

Jeder Elternteil mit der Erkrankung hat ein 50%iges Risiko, den genetischen Defekt aufgrund seiner autosomal-dominanten Natur an jedes Kind weiterzugeben . Die meisten Menschen mit MFS haben ein weiteres betroffenes Familienmitglied. Etwa 75% der Fälle werden vererbt. Andererseits sind etwa 15–30% aller Fälle auf de novo genetische Mutationen zurückzuführen ; solche spontanen Mutationen treten bei etwa einer von 20.000 Geburten auf. Das Marfan-Syndrom ist auch ein Beispiel für dominante negative Mutation und Haploinsuffizienz . Es ist mit variabler Expressivität verbunden ; unvollständige Penetranz ist nicht endgültig dokumentiert.
Pathogenese

Das Marfan-Syndrom wird durch Mutationen im FBN1- Gen auf Chromosom 15 verursacht , das für Fibrillin 1 kodiert , eine Glykoproteinkomponente der extrazellulären Matrix. Fibrillin-1 ist für die ordnungsgemäße Bildung der extrazellulären Matrix, einschließlich der Biogenese und Aufrechterhaltung der elastischen Fasern, unerlässlich. Die extrazelluläre Matrix ist sowohl für die strukturelle Integrität des Bindegewebes entscheidend, dient aber auch als Reservoir für Wachstumsfaktoren. Elastische Fasern sind im ganzen Körper zu finden, besonders häufig jedoch in der Aorta, den Bändern und den Ziliarzonula des Auges; folglich gehören diese Gebiete zu den am stärksten betroffenen. Es kann auch durch eine Reihe von intravenösen Kristallbehandlungen bei Patienten verursacht werden, die für die Erkrankung anfällig sind.
Es wurde eine transgene Maus geschaffen, die eine einzelne Kopie eines mutierten Fibrillin-1 trägt, eine Mutation ähnlich derjenigen, die im menschlichen Gen gefunden wird, von dem bekannt ist, dass es MFS verursacht. Dieser Mausstamm rekapituliert viele Merkmale der menschlichen Krankheit und verspricht Einblicke in die Pathogenese der Krankheit. Eine Verringerung des normalen Fibrillin-1-Spiegels verursacht bei Mäusen eine Marfan-bedingte Krankheit.
Der transformierende Wachstumsfaktor Beta ( TGF-β ) spielt eine wichtige Rolle bei MFS. Fibrillin-1 bindet direkt eine latente Form von TGF-β, hält es sequestriert und unfähig, seine biologische Aktivität auszuüben. Das einfachste Modell legt nahe, dass reduzierte Fibrillin-1-Spiegel einen Anstieg der TGF-β-Spiegel aufgrund unzureichender Sequestrierung ermöglichen. Obwohl nicht bewiesen ist, wie erhöhte TGF-β-Spiegel für die bei der Krankheit beobachtete spezifische Pathologie verantwortlich sind, ist bekannt, dass eine entzündliche Reaktion auftritt, die Proteasen freisetzt, die die elastischen Fasern und andere Komponenten der extrazellulären Matrix langsam abbauen. Die Bedeutung des TGF-β-Wegs wurde durch die Entdeckung des ähnlichen Loeys-Dietz-Syndroms bestätigt, an dem das TGFβR2- Gen auf Chromosom 3 , einem Rezeptorprotein von TGF-β, beteiligt ist. Das Marfan-Syndrom wurde oft mit dem Loeys-Dietz-Syndrom verwechselt, da die beiden Pathologien beträchtliche klinische Überschneidungen aufweisen.
Marfanoid-Progeroid-Lipodystrophie-Syndrom
Das Marfanoid-Progeroid-Lipodystrophie-Syndrom (MPL), auch als Marfan-Lipodystrophie-Syndrom (MFLS) bezeichnet, ist eine Variante des MFS, bei der die Marfan-Symptome von Merkmalen begleitet werden, die normalerweise mit dem neonatalen Progeroid-Syndrom (auch als Wiedemann-Rautenstrauch-Syndrom bezeichnet) verbunden sind. bei denen die Spiegel des weißen Fettgewebes reduziert sind. Seit 2010 häufen sich Hinweise darauf, dass MPL durch Mutationen in der Nähe des 3'-Terminus des FBN1- Gens verursacht wird . Es wurde gezeigt, dass diese Menschen auch einen Mangel an Asprosin haben , einem glukoregulierenden Proteinhormon, das das C-terminale Spaltprodukt von Profibrillin ist. Die bei diesen Personen beobachteten Asprosinspiegel waren niedriger als für einen heterozygoten Genotyp erwartet, was mit einer dominanten negativen Wirkung übereinstimmt .
Diagnose
1996 wurden die diagnostischen Kriterien des MFS international vereinbart. Allerdings ist das Marfan-Syndrom bei Kindern oft schwer zu diagnostizieren, da sie typischerweise erst bei Erreichen der Pubertät Symptome zeigen. Eine Diagnose basiert auf der Familienanamnese und einer Kombination von Haupt- und Nebenindikatoren der Erkrankung, die in der Allgemeinbevölkerung selten sind und bei einer Person auftreten – zum Beispiel: vier Skelettzeichen mit einem oder mehreren Zeichen in einem anderen Körpersystem wie Augen und Herz-Kreislauf bei einer Person. Die folgenden Zustände können von MFS herrühren, können aber auch bei Menschen ohne bekannte Grunderkrankung auftreten.
- Aortenaneurysma oder Dilatation
- Arachnodaktylie
- GERD
- Bikuspide Aortenklappe
- Zysten
- Zystische mediale Nekrose
- Degenerative Bandscheibenerkrankung
- Krumme Nasenscheidewand
- Durale Ektasie
- Frühe Katarakte
- Frühes Glaukom
- Frühe Arthrose
- Ektopie lentis
- Emphysem
- Iris Kolobom
- Überdurchschnittliche Höhe
- Herzklopfen
- Hernien
- Hochgewölbter Gaumen
- Hypermobilität der Gelenke
- Kyphose (nach hinten gebeugt)
- Undichte Herzklappe
- Malokklusion
- Mikrognathie (kleiner Unterkiefer)
- Mitralklappenprolaps
- Myopie (Kurzsichtigkeit)
- Obstruktive Lungenerkrankung
- Osteopenie (niedrige Knochendichte)
- Pectus carinatum oder Excavum
- Pes planus ( Plattfüße )
- Pneumothorax (kollabierte Lunge)
- Netzhautablösung
- Skoliose
- Schlafapnoe
- Dehnungsstreifen nicht von Schwangerschaft oder Fettleibigkeit
- Zähne überfüllt
- "Schmales, dünnes Gesicht"
- Kiefergelenksdysfunktion (TMD)
Überarbeitete Genter Nosologie
Im Jahr 2010 wurde die Genter Nosologie überarbeitet und die bisherige Vereinbarung von 1996 durch neue Diagnosekriterien ersetzt. Die sieben neuen Kriterien können zu einer Diagnose führen:
In Ermangelung einer Familienanamnese von MFS:
- Aortenwurzel Z-Score ≥ 2 UND Ektopie lentis
- Aortenwurzel-Z-Score ≥ 2 UND eine FBN1-Mutation
- Aortenwurzel-Z-Score ≥ 2 UND ein systemischer Score* > 7 Punkte
- Ectopia lentis UND eine FBN1-Mutation mit bekannter Aortenpathologie
Bei Vorliegen einer Familienanamnese von MFS (wie oben definiert):
- Ektopie lentis
- Systemischer Score* ≥ 7
- Aortenwurzel Z-Score ≥ 2
- Punkte für den systemischen Score:
- Handgelenk UND Daumenzeichen = 3 (Handgelenk ODER Daumenzeichen = 1)
- Pectus carinatum-Deformität = 2 (Pectus Excavum oder Brustasymmetrie = 1)
- Rückfußdeformität = 2 (einfacher Pes planus = 1)
- Durale Ektasie = 2
- Protrusio acetabuli = 2
- Pneumothorax = 2
- Reduziertes Verhältnis von oberem Segment zu unterem Segment UND erhöhter Arm/Höhe UND keine schwere Skoliose = 1
- Skoliose oder thorakolumbale Kyphose = 1
- Reduzierte Ellbogenstreckung = 1
- Gesichtsmerkmale (3/5) = 1 ( Dolichozephalie , enophthalmos , downslanting Lidspalten , malar Hypoplasie , Retrognathie )
- Hautstreifen ( Dehnungsstreifen ) = 1
- Myopie > 3 Dioptrien = 1
- Mitralklappenprolaps = 1
Das Daumenzeichen (Steinberg-Zeichen) wird ausgelöst, indem die Person aufgefordert wird, den Daumen so weit wie möglich zu beugen und dann die Finger darüber zu schließen. Ein positives Daumenzeichen ist, wenn die gesamte distale Phalanx über den ulnaren Handrand hinaus sichtbar ist , verursacht durch eine Kombination aus Hypermobilität des Daumens sowie einem Daumen, der länger als gewöhnlich ist.
Das Handgelenkszeichen (Walker-Murdoch-Zeichen) wird ausgelöst, indem die Person aufgefordert wird, den Daumen und die Finger einer Hand um das andere Handgelenk zu legen. Ein positives Handgelenkzeichen ist, wenn sich der kleine Finger und der Daumen überlappen, verursacht durch eine Kombination aus dünnen Handgelenken und langen Fingern.
Differenzialdiagnose
Viele andere Erkrankungen können die gleichen Körpermerkmale wie das Marfan-Syndrom hervorrufen. Gentests und die Bewertung anderer Anzeichen und Symptome können helfen, diese zu unterscheiden. Im Folgenden sind einige der Störungen aufgeführt, die sich als "Marfanoid" manifestieren können:
- Angeborene kontrakturale Arachnodaktylie , auch bekannt als Beals-Hecht-Syndrom
- Ehlers-Danlos-Syndrom
- Homocystinurie
- Loeys-Dietz-Syndrom
- MASS-Phänotyp
- Multiple endokrine Neoplasie, Typ 2B
- Shprintzen-Goldberg-Syndrom
- Stickler-Syndrom
Verwaltung
Es gibt keine Heilung für das Marfan-Syndrom, aber die Lebenserwartung ist in den letzten Jahrzehnten deutlich gestiegen und entspricht jetzt der des Durchschnittsmenschen.
Regelmäßige Kontrollen werden empfohlen, um den Zustand der Herzklappen und der Aorta zu überwachen . Das Marfan-Syndrom wird behandelt, indem jedes Problem so behandelt wird, wie es auftritt, und insbesondere durch vorbeugende Medikamente auch bei kleinen Kindern, um das Fortschreiten der Aortenerweiterung zu verlangsamen. Das Ziel dieser Behandlungsstrategie besteht darin, das Fortschreiten der Aortenerweiterung zu verlangsamen und Schäden an den Herzklappen zu verhindern, indem Herzrhythmusstörungen beseitigt , die Herzfrequenz minimiert und der Blutdruck gesenkt wird .
Physische Aktivität
Die American Heart Association gab die folgenden Empfehlungen für Menschen mit Marfan-Syndrom ohne oder mit leichter Aortenerweiterung:
- Wahrscheinlich zulässige Aktivitäten: Bowling, Golf, Skaten (aber kein Eishockey), Schnorcheln, zügiges Gehen, Laufband, Fahrradfahren, bescheidenes Wandern und Doppeltennis.
- Mittleres Risiko: Basketball (sowohl Voll- als auch Halbplatz), Racquetball, Squash, Laufen (Sprinten und Joggen), Skifahren (Abfahrt und Langlauf), Fußball, Einzeltennis, Touch-Fußball (Flagge), Baseball, Softball, Radfahren , Rundenschwimmen, Motorradfahren und Reiten.
- Hohes Risiko: Bodybuilding, Gewichtheben (ohne und mit freien Gewichten), Eishockey, Klettern, Windsurfen, Surfen und Tauchen.
Medikation
Die Behandlung umfasst häufig die Anwendung von Betablockern wie Propranolol oder, falls nicht vertragen, Kalziumkanalblockern oder ACE-Hemmern . Betablocker werden verwendet, um die Belastung der Aorta zu reduzieren und die Aortenerweiterung zu verringern.
Operation
Wenn die Dilatation der Aorta zu einem Aneurysma mit signifikantem Durchmesser fortschreitet , eine Dissektion oder eine Ruptur verursacht oder zum Versagen der Aorta oder einer anderen Klappe führt, wird eine Operation (möglicherweise ein zusammengesetztes Aortenklappentransplantat oder ein klappenerhaltender Aortenwurzelersatz ) notwendig. Obwohl eine Aortentransplantation (oder jede Gefäßchirurgie) ein ernstes Unterfangen ist, ist sie im Allgemeinen erfolgreich, wenn sie auf Wahlbasis durchgeführt wird. Wesentlich problematischer ist die Operation im Rahmen einer akuten Aortendissektion oder -ruptur. Eine elektive Aortenklappen-/Transplantatoperation wird normalerweise in Betracht gezogen, wenn der Aortenwurzeldurchmesser 50 Millimeter (2,0 Zoll) erreicht, aber jeder Fall muss von einem qualifizierten Kardiologen speziell untersucht werden. Neue klappenerhaltende Operationstechniken werden immer häufiger. Da Menschen mit Marfan-Syndrom länger leben, werden andere Gefäßreparaturen häufiger, zB Reparaturen von absteigenden thorakalen Aortenaneurysmen und Aneurysmen anderer Gefäße als der Aorta.
Die skelettalen und okulären Manifestationen des Marfan-Syndroms können ebenfalls schwerwiegend sein, jedoch nicht lebensbedrohlich. Diese Symptome werden in der Regel der Erkrankung entsprechend behandelt, beispielsweise mit Schmerzmitteln oder Muskelrelaxantien . Da das Marfan-Syndrom asymptomatische Wirbelsäulenanomalien verursachen kann, sollte jede geplante Wirbelsäulenoperation bei einer Person von Marfan unabhängig von der Indikation für eine Operation nur einer detaillierten Bildgebung und einer sorgfältigen Operationsplanung folgen. Die okulären Komplikationen des MFS können oft operativ behandelt werden. Ektopie lentis kann behandelt werden, da künstliche Linsen chirurgisch implantiert werden können. Darüber hinaus kann eine Operation Glaukom und Katarakte behandeln .
Die Behandlung eines Spontanpneumothorax hängt vom Luftvolumen im Pleuraspalt und dem natürlichen Krankheitsverlauf ab. Ein kleiner Pneumothorax kann ohne aktive Behandlung innerhalb von ein bis zwei Wochen verschwinden. Rezidivierende Pneumothoraces können eine Brustoperation erfordern. Mäßig Größe Pneumothoraces Möglicherweise müssen Thoraxdrainage für mehrere Tage in einem Krankenhaus - Management. Große Pneumothoraces sind wahrscheinlich medizinische Notfälle, die eine Notfalldekompression erfordern.
Alternativ werden auch maßgefertigte Stützen für die Aortenwurzel verwendet. Bis 2020 wurde dieses Verfahren bei über 300 Personen angewendet, wobei der erste Fall im Jahr 2004 auftrat.
Schwangerschaft
Während der Schwangerschaft besteht bei Frauen mit Marfan-Syndrom auch ohne präkonzeptionelle kardiovaskuläre Anomalie ein erhebliches Risiko einer Aortendissektion, die selbst bei rascher Behandlung oft tödlich verläuft. Frauen mit Marfan-Syndrom sollten daher vor der Empfängnis einer gründlichen Untersuchung unterzogen werden und während der Schwangerschaft sollte alle sechs bis zehn Wochen eine Echokardiographie durchgeführt werden, um den Durchmesser der Aortenwurzel zu bestimmen. Für die meisten Frauen ist eine sichere vaginale Entbindung möglich.
Bei Frauen mit Marfan-Syndrom können vorgeburtliche Tests durchgeführt werden, um festzustellen, ob die Erkrankung bei ihrem Kind vererbt wurde. In der 10. bis 12. Schwangerschaftswoche kann ein Stück Plazentagewebe durch einen Test namens Chorionzottenbiopsie untersucht werden, um eine Diagnose zu stellen. In der 16. bis 18. Schwangerschaftswoche kann ein weiterer pränataler Test namens Amniozentese durchgeführt werden.
Das Marfan-Syndrom wird dominant exprimiert. Dies bedeutet, dass ein Kind mit einem Elternteil, einem Träger des Gens, eine 50%-ige Wahrscheinlichkeit hat, das Syndrom zu bekommen. 1996 wurde die erste genetische Präimplantationstest (PGT)-Therapie für Marfan durchgeführt; Im Wesentlichen bedeutet PGT, einen genetischen Test an IVF- Embryozellen im Frühstadium durchzuführen und die von der Marfan-Mutation betroffenen Embryonen zu verwerfen.
Prognose
Vor modernen kardiovaskulären Operationstechniken und Medikamenten wie Losartan und Metoprolol war die Prognose von Patienten mit Marfan-Syndrom nicht gut: Eine Reihe von nicht behandelbaren kardiovaskulären Problemen war häufig. Die Lebenserwartung wurde um mindestens ein Drittel verkürzt, und viele starben im Teenager- und Zwanzigerjahre an Herz-Kreislauf-Problemen. Heute sind kardiovaskuläre Symptome des Marfan-Syndroms immer noch die wichtigsten Probleme bei der Diagnose und Behandlung der Krankheit, aber eine angemessene prophylaktische Überwachung und prophylaktische Therapie bietet etwas, das einer normalen Lebensdauer nahekommt, und mehr Manifestationen der Krankheit werden entdeckt, je länger die Patienten leben. Frauen mit Marfan-Syndrom leben länger als Männer.
Epidemiologie
Das Marfan-Syndrom betrifft Männer und Frauen gleichermaßen, und die Mutation zeigt keine ethnische oder geografische Voreingenommenheit. Schätzungen gehen davon aus, dass etwa 1 von 5.000 bis 10.000 Personen das Marfan-Syndrom hat.
Geschichte
Das Marfan-Syndrom ist nach Antoine Marfan benannt , dem französischen Kinderarzt, der die Erkrankung erstmals 1896 beschrieb, nachdem er bei einem fünfjährigen Mädchen auffällige Merkmale bemerkt hatte. Das mit der Krankheit in Verbindung stehende Gen wurde erstmals 1991 von Francesco Ramirez am Mount Sinai Medical Center in New York City identifiziert .
Siehe auch
- Ehlers-Danlos-Syndrom
- Kaschin-Beck-Krankheit
- Loeys-Dietz-Syndrom
- Nagel-Patella-Syndrom
- Mitralklappenprolaps
Verweise
Externe Links
| Einstufung | |
|---|---|
| Externe Ressourcen |