Phthalsäure - Phthalic acid
|
|
|
|
| Namen | |
|---|---|
|
Bevorzugter IUPAC-Name
Benzol-1,2-dicarbonsäure |
|
| Andere Namen
1,2-Benzendisäure
Phthalsäure Benzol-1,2-disäure ortho -Phthalsäure |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA-InfoCard |
100.001.703 |
| EG-Nummer | |
|
PubChem- CID
|
|
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| C 8 H 6 O 4 | |
| Molmasse | 166.132 g/mol |
| Aussehen | weißer Feststoff |
| Dichte | 1,593 g/cm 3 , fest |
| Schmelzpunkt | 207 °C (405 °F; 480 K) |
| 0,6 g / 100 ml | |
| Säure (p K a ) | 2.89, 5.51 |
| -83,61·10 -6 cm 3 /mol | |
| Gefahren | |
| NFPA 704 (Feuerdiamant) | |
| Verwandte Verbindungen | |
|
Verwandte Carbonsäuren
|
Isophthalsäure Terephthalsäure |
|
Verwandte Verbindungen
|
Phthalsäureanhydrid Phthalimid Phthalhydrazid Phthaloylchlorid Benzol- 1,2 - dicarboxaldehyd |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
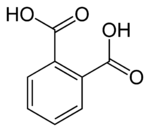
Phthalsäure ist eine aromatische Dicarbonsäure mit der Formel C 6 H 4 (CO 2 H) 2 . Es ist ein Isomer von Isophthalsäure und Terephthalsäure . Obwohl Phthalsäure von bescheidener kommerzieller Bedeutung ist, ist das eng verwandte Derivat Phthalsäureanhydrid eine in großem Maßstab hergestellte Grundchemikalie. Phthalsäure ist eines von drei Isomeren der Benzoldicarbonsäure , die anderen sind Isophthalsäure und Terephthalsäure .
Produktion
Phtalsäure wird durch die katalytische Oxidation von hergestellten Naphthalin- oder ortho- Xylol direkt mit Phthalsäureanhydrid und anschließender Hydrolyse des Anhydrids.
Phthalsäure wurde erstmals 1836 vom französischen Chemiker Auguste Laurent durch Oxidation von Naphthalintetrachlorid gewonnen. Er glaubte, die resultierende Substanz sei ein Naphthalin-Derivat und nannte sie "Naphthalinsäure". Nachdem der Schweizer Chemiker Jean Charles Galissard de Marignac die richtige Formel bestimmt hatte, gab Laurent ihr ihren heutigen Namen. Zu den Herstellungsmethoden des 19. Jahrhunderts gehörten die Oxidation von Naphthalintetrachlorid mit Salpetersäure oder besser die Oxidation des Kohlenwasserstoffs mit rauchender Schwefelsäure unter Verwendung von Quecksilber oder Quecksilber(II)-Sulfat als Katalysator.
Synthese
Naphthalin ergibt bei Oxidation mit Kaliumpermanganat oder Kaliumdichromat Phthalsäure.
Reaktionen und Verwendungen
Es ist eine zweibasige Säure mit einem p K a s von 2,89 und 5,51. Das Monokaliumsalz Kaliumhydrogenphthalat ist eine Standardsäure in der analytischen Chemie . Typischerweise werden Phthalatester aus dem weit verbreiteten Phthalsäureanhydrid hergestellt . Reduktion von Phthalsäure mit Natriumamalgam in Gegenwart von Wasser ergibt das 1,3-Cyclohexadien- Derivat.
Sicherheit
Die Toxizität von Phthalsäure ist mit einer LD 50 (Maus) von 550 mg/kg gering .
Biologischer Abbau
Das Bakterium Pseudomonas sp. P1 baut Phthalsäure ab.
Siehe auch
- Isophthalsäure
- Phthalat
- Phthalsäureanhydrid
- Kaliumhydrogenphthalat , ein Primärstandard für Säure-Base-Titrationen
- Terephthalsäure
Verweise
- ^ "PHTHALISÄURE" . hazard.com .
- ^ Brown, HC, et al., in Baude, EA und Nachod, FC, Determination of Organic Structures by Physical Methods , Academic Press, New York, 1955.
- ^ Es werden mehrere Schmelzpunkte angegeben, zum Beispiel: (i) 480. K (NIST-Website), (ii) 210−211 °C mit Zersetzung (Sigma-Aldrich online), (iii) 191 °C in einem verschlossenen Röhrchen (Ullmann's Encyclopedia of Industrial Chemistry), (iv) 230 °C mit Umwandlung in Phthalsäureanhydrid und Wasser (JTBaker MSDS).
- ^ a b Lorz, Peter M.; Towae, Friedrich K.; Enke, Walter; Jäckh, Rudolf; Bhargava, Naresh; Hillesheim, Wolfgang (2007). „Phthalsäure und Derivate“. Ullmanns Enzyklopädie der Technischen Chemie . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a20_181.pub2 .
- ^ a b c d Chisholm, Hugh, Hrsg. (1911). . Encyclopædia Britannica . 21 (11. Aufl.). Cambridge University Press. S. 545–546.
-
^ Siehe:
- Auguste Laurent (1836) "Sur l'acide naphtalique et ses combinaisons" (Über Naphthalsäure und ihre Verbindungen), Annales de Chimie et de Physique , 61 : 113-125. (Anmerkung: Die empirischen Formeln der in diesem Artikel analysierten Verbindungen sind falsch, zum Teil, weil Chemiker in dieser Zeit falsche Atommassen für Kohlenstoff (6 statt 12) und andere Elemente verwendeten.)
- In deutscher Sprache abgedruckt als: Auguste Laurent (1836) "Über Naphthalinsäure und ihre Verbindungen" , Annalen der Pharmacie , 19 (1): 38-50; zur Herstellung von Phthalsäure siehe Seite 41.
- ^ C. de Marignac (1841) "Ueber die Naphtalinsäure und ein bei ihrer Darstellung entstehendes flüchtiges Produkt" , Annalen der Chemie und Pharmacie , 38 (1) : 13 -20. (Anmerkung: Auch hier sind die empirischen Formeln von Marignac falsch, da Chemiker zu dieser Zeit falsche Atommassen verwendeten.)
-
^ Siehe:
- Auguste Laurent (1841) "Sur de nouvelles combinaisons nitrogénées de la naphtaline et sur les acides phtalique et nitrophthalique" (Über neue stickstoffhaltige Verbindungen von Naphthalin sowie über Phthalsäure und Nitrophthalsäure), Revue Scientifique et Industrielle , 6 : 76-99; auf Seite 92 prägt Laurent den Namen "acide phtalique" (Phthalsäure) und gibt zu, dass seine frühere empirische Formel für Phthalsäure falsch war.
- Abgedruckt in deutscher Sprache als: Auguste Laurent (1842) "Ueber neue stickstoffhaltige Verbindungen des Naphtalins, über Phtalinsäure und Nitrophthalinsäure" , Annalen der Chemie und Pharmacie , 41 (1) : 98-114; auf Seite 108 prägt Laurent den Namen "Phtalinsäure" (Phthalsäure).
- ^ Richard N. McDonald und Charles E. Reineke (1988). "trans-1,2-Dihydrophthalsäure" . Organische Synthesen .; Sammelband , 6 , p. 461
- ^ Ishtiaq Ali, Mohammed (2011). Mikrobieller Abbau von Polyvinylchlorid-Kunststoffen (PDF) (Ph.D.). Quaid-i-Azam-Universität. s. 47.
- Merck-Index, 9. Aufl., #7178


