Umgekehrte Zoonose - Reverse zoonosis
Reverse Zoonose , auch bekannt als Zooanthroponose, und manchmal Anthroponose (griechisch Zoon „Tier“, anthropos „man“, nosos „ Krankheit“), bezieht sich auf Krankheitserreger in bevorratet Menschen , die fähig sind , auf nicht-menschliche übertragen werden Tiere .
Terminologie
Anthroponose bezieht sich auf vom Menschen stammende Krankheitserreger und kann die Übertragung von Mensch zu Tier, aber auch von Mensch zu Mensch umfassen. Der Begriff Zoonose bezieht sich technisch auf eine Krankheit, die zwischen einem Tier und einem anderen Tier, Mensch oder Nicht-Mensch, ohne Ermessen übertragen wird, und wurde auch als Krankheit definiert, die vom Tier auf den Menschen und umgekehrt übertragen wird . Aufgrund der auf den Menschen ausgerichteten medizinischen Voreingenommenheit wird die Zoonose jedoch in der Regel auf die gleiche Weise wie die Anthropozoonose verwendet, die sich speziell auf Krankheitserreger bezieht, die in nichtmenschlichen Tieren vorhanden sind und auf den Menschen übertragbar sind.
Zusätzliche Verwirrung aufgrund der Häufigkeit von Wissenschaftlern, die "Anthropozoonose" und "Zooanthroponose" austauschbar verwenden, wurde während einer Sitzung des Gemeinsamen Ausschusses für Ernährung und Landwirtschaft und der Weltgesundheitsorganisation 1967 gelöst , die die Verwendung von "Zoonose" zur Beschreibung des bidirektionalen Austauschs infektiöser Krankheitserreger zwischen Tieren und Tieren empfahl Menschen.
Da der Mensch zudem selten in direktem Kontakt mit Wildtieren steht und Krankheitserreger durch „sanften Kontakt“ einschleppt, muss der Begriff „Sapronoten“ eingeführt werden. Sapronosen (griechisch sapros "zerfallend") bezieht sich auf menschliche Krankheiten, die die Fähigkeit besitzen, in abiotischen Umgebungen wie Boden, Wasser, verwesenden Pflanzen, Tierleichen, Exkrementen und anderen Substraten zu wachsen und sich zu vermehren (nicht nur zu überleben oder zu kontaminieren) . Darüber hinaus können Sapro-Zoonosen dadurch charakterisiert werden, dass sie sowohl einen lebenden Wirt als auch einen nicht-tierischen Entwicklungsstandort von organischem Material, Boden oder Pflanzen aufweisen. Es muss beachtet werden, dass obligate intrazelluläre Parasiten, die sich außerhalb von Zellen nicht replizieren können und vollständig reproduktiv darauf angewiesen sind, in die Zelle einzudringen, um intrazelluläre Ressourcen wie Viren, Rickettsien, Chlamydien und Cryptosporidium parvum zu nutzen, keine Sapronoten sein können.
Etymologische Fallstricke
Die Kategorisierung von Krankheiten in epidemiologische Klassen nach der vermeintlichen Quelle der Infektion oder der Übertragungsrichtung wirft eine Reihe von Widersprüchen auf, die durch die Verwendung zyklischer Modelle gelöst werden könnten, wie die folgenden Szenarien zeigen:
Zoonose vs. umgekehrte Zoonose vs. Anthroponose
Bei Krankheiten, die von arthropoden Vektoren übertragen werden, wie Gelbfieber , Dengue , Typhus , Zeckenrückfallfieber , Zika-Fieber und Malaria , wird die Begriffsdifferenzierung immer verschwommener. Zum Beispiel wird ein mit Malaria infizierter Mensch von einer Mücke gebissen, die anschließend ebenfalls infiziert wird. Dies ist ein Fall von umgekehrter Zoonose (von Mensch zu Tier). Die neu infizierte Mücke infiziert dann jedoch einen anderen Menschen. Dies könnte ein Fall von Zoonose (von Tier zu Mensch) sein, wenn die Mücke als ursprüngliche Quelle angesehen wird, oder Anthroponose (von Mensch zu Mensch), wenn der Mensch als ursprüngliche Quelle betrachtet wird. Wenn diese infizierte Mücke stattdessen einen nicht-menschlichen Primaten infiziert, könnte dies als Fall einer umgekehrten Zoonose/Zooanthroponose (von Mensch zu Tier) angesehen werden, wenn der Mensch als primäre Quelle betrachtet wird, oder einfach als Zoonose (von Tier zu Tier), wenn die Mücke in Betracht gezogen wird die primäre Quelle.
Zoonose vs. Anthroponose
In ähnlicher Weise könnten HIV, das von Affen stammt (Crossover aufgrund des Verzehrs von wildem Schimpansen- Buschfleisch durch den Menschen ) und Influenza-A- Viren, die von Vögeln stammen (Crossover aufgrund einer Antigenverschiebung) ursprünglich als zoonotische Übertragung angesehen worden sein, da die Infektionen zuerst von Wirbeltieren ausgingen, aber derzeit wegen ihres Übertragungspotentials von Mensch zu Mensch als Anthroponose angesehen werden.
Sapronose vs Sapro-Zoonose
Typische Beispiele für Sapronotika sind Pilze wie Kokzidioidomykose , Histoplasmose , Aspergillose , Kryptokokkose , Microsporum gypseum . Einige können bakteriell sein, vom sporulierenden Clostridium und Bazillus bis hin zu Rhodococcus equi, Burkholderia pseudomallei, Listeria , Erysipelothrix , Yersinia pseudotuberculosis, Legionellose, Pontiac-Fieber und nichttuberkulöse Mykobakteriosen. Andere Sapronotika sind Amöben wie bei der primären Amöben-Meningoenzephalitis . Schwierigkeiten bei der Einordnung treten wiederum bei sporulierenden Bakterien auf, deren infektiöse Sporen erst nach einer signifikanten Phase inaktiven vegetativen Wachstums in einer abiotischen Umgebung gebildet werden, die jedoch immer noch als Sapronosen angesehen wird. Jedoch können Fälle von Zoosapronosen, an denen Listeria , Erysipelothrix , Yersinia pseudotuberculosis , Burkholderia pseudomallei und Rhodococcus equi beteiligt sind, durch ein Tier oder ein abiotisches Substrat übertragen werden, treten jedoch normalerweise über einen fäkal-oralen Weg zwischen Menschen und anderen Tieren auf.
Fälle mit Übertragungsmodi
Arthropoden-Vektoren
Malaria
Malaria bezeichnet die zyklische Infektion von Tieren (Mensch und Nicht-Mensch) und Stechmücken der Gattung Anopheles mit einer Reihe von Plasmodium- Arten. Der Plasmodium-Parasit wird auf die Mücke übertragen, während sie sich vom Blut des infizierten Tieres ernährt, woraufhin er einen sporogenen Zyklus im Darm der Mücke beginnt, der bei der nächsten Blutmahlzeit ein anderes Tier infiziert. Es scheint keine schädlichen Auswirkungen der Parasiteninfektion auf die Mücke zu geben. Der normalerweise bei Primaten vorkommende Parasit Plasmodium brasilianum ist morphologisch dem Malaria-induzierenden Plasmodium malariae ähnlich, das häufiger beim Menschen vorkommt, und es ist umstritten, ob es sich tatsächlich um unterschiedliche Arten handelt. Dennoch gab es 12 Berichte über Malaria in den abgelegenen indigenen Yanomami- Gemeinschaften des venezolanischen Amazonas , wo überraschenderweise festgestellt wurde, dass sie durch einen Stamm von P. brasilianum verursacht wurde, der zu 100% identisch mit Sequenzen war, die in Alouatta seniculus- Affen gefunden wurden. Dies deutet auf eine eindeutige Zoonose und eine hohe Wahrscheinlichkeit eines Rückstaus in nichtmenschliche Primatenbanden als umgekehrte Zoonosen hin.
Afrikanische Schlafkrankheit
Trypanosoma brucei gambiense (T. b. gambiense) ist eine Art afrikanischer Trypanosomen, bei denen es sich um protozoische Hämoflagellaten handelt, die für Trypanosomiasis (besser bekannt als Afrikanische Schlafkrankheit ) bei Menschen und anderen Tieren verantwortlich sind. Die Protozoen werden über Tsetsefliegen übertragen, wo sie sich vermehren und während der Blutmahlzeit der Fliege auf einen weiteren tierischen Wirt übertragen werden können. Ausbrüche der Schlafkrankheit in bestimmten menschlichen Gemeinschaften wurden eliminiert, aber nur vorübergehend, da die ständige Wiedereinschleppung aus unbekannten Quellen statistisch auf das Vorhandensein eines nicht-menschlichen Reservoirs hindeutet, in dem das Zurückfließen des Erregers in einem silvatischen Zyklus aufrechterhaltenund wieder in die Stadt eingeschleppt wird Kreislauf. Die Anwesenheit von T. b. gambiense wurde bei Menschen und Nutztieren getrennt nachgewiesen. Dies führte zu einer molekularen Studie, in der die Serumreaktivität von Schweinen , Ziegen und Kühen mit Humanserum verglichenwurde,wobei bemerkenswerte Ähnlichkeiten in allen Proben, insbesondere jedoch in Schweineproben, auftraten. Zusammengenommen implizieren diese Ergebnisse eine umgekehrte zoonotische Übertragung von Mensch zu Tier.
Arboviren
Gelbfieber-Viren, Dengue-Fieber-Viren und Zika-Viren gehören zu den Flavivirus- Gattungen und das Chikungunya- Virus gehört zu den Alphavirus- Gattungen. Alle von ihnen gelten als Arboviren, was ihre Fähigkeit zur Übertragung durch Arthropodenvektoren bezeichnet. Sylvatische Übertragungszyklen für Arboviren innerhalb nichtmenschlicher Primatengemeinschaften haben das Potenzial, in einen urbanen Zyklus innerhalb des Menschen überzugehen, in dem der Mensch in Szenarien, in denen eine weitere Vermischung eliminiert wird, aber viel wahrscheinlicher ist, ein Wiederauftreten dieser Viren in einen der Zyklen als Sackgassenwirte auftreten könnte wegen Rückstau. Anscheinend erfordert die Aufrechterhaltung eines arboviralen urbanen Zyklus zwischen Menschen eine seltene oder wenig erforschte Kombination von Faktoren. Eine der folgenden Situationen tritt ein:
- Ein infizierter Mensch in einer städtischen Umgebung füttert eine sylvatische (normalerweise abgelegene ) Mücke wie Haemogogus (die im Vergleich zu anderen Mücken eine relativ lange Lebensdauer hat und das Virus über längere Zeit übertragen kann), die einen anderen Menschen oder ein nicht-menschliches Tier infiziert, das wird als Reservoir dienen.
- Ein urbaner Aedes (der häufiger in städtischen Gebieten zu finden ist) ernährt und überträgt das Virus auf ein anderes menschliches oder nicht-menschliches Tier, das als Reservoir dient.
- Eine ausreichende Anzahl von sylvatischen Vektormücken und dem Tierreservoir bewohnen die gleiche ökologische Nische in engem Kontakt, um den Zoonosezyklus des Virus zu fördern und aufrechtzuerhalten.
- Das tierische Virusreservoir hält einen geeigneten Virusspiegel im Blut aufrecht, um die Infektion einer Vektormücke zu ermöglichen.
- Eine Brückenvektormücke wie Aedes albopictus , die in einem städtischen Gebiet überleben und sich auf ländliche, halbländliche und Waldgebiete ausbreiten kann, könnte das Virus in eine waldige Umgebung übertragen.
- Zika-Fieber: Das Zika-Virus wird durch das einzelsträngige RNA- Flavivirus verursacht, das die Aedes-Mücke als Vektor verwendet, um andere menschliche und tierische Wirte zu infizieren. A 2015 zika Virusstamm aus einem Menschen in isoliertem Brasilien wurde verwendet , um schwanger zu infizieren Rhesusmakaken intravenös und intra Frucht Verbündeter. Sowohl die Muttertiere als auch die Plazenten wurden mit Zika-positiven Gewebeproben infiziert, die bis zu 105 Tage lang aufgezeichnet wurden. Dies bestätigt ein umgekehrtes zoonotisches Übertragungspotential zwischen Menschen und nichtmenschlichen Primaten.
- Gelbfieber: Das Gelbfiebervirus wird auch durch den Stich einer infizierten Mückenart Aedes oder Haemagogus übertragen, die sich von einem infizierten Tier ernähren. Der historische Verlauf des amerikanischen Sklavenhandels ist ein Paradebeispiel für die Einschleppung eines Krankheitserregers, um einen völlig neuen Sylvatzyklus zu schaffen. Frühere Hypothesen eines " New World YFV" wurden in einer Studie aus dem Jahr 2007 zunichte gemacht, in der die Raten der Nukleotidsubstitution und -divergenz untersucht wurden, um festzustellen, dass Gelbfieber vor etwa 400 Jahren aus Westafrika nach Amerika eingeschleppt wurde . Etwa im 17. Jahrhundert wurde Gelbfieber auch von Europäern dokumentiert, die sich am Sklavenhandel beteiligt hatten. Die tatsächliche Art der Einführung hätte sich in einer Reihe von Szenarien abspielen können, ob ein virämischer Mensch der Alten Welt, eine infizierte Mücke der Alten Welt, Eier, die von einer infizierten Mücke der Alten Welt gelegt wurden, oder alle drei nach Amerika transportiert wurden, da die Übertragung von Gelbfieber nicht erfolgte auf Segelschiffen ungewöhnlich. Inmitten neuerer Gelbfieber-Ausbrüche im Südosten Brasiliens wurde das Spillback-Potenzial sehr deutlich. Molekulare Vergleiche von nicht-menschlichen Primaten-Ausbruchsstämmen erwiesen sich als enger verwandt mit menschlichen Stämmen als Stämme, die von anderen nicht-menschlichen Primaten abgeleitet wurden, was auf eine anhaltende umgekehrte Zoonose schließen lässt.
- Chikungunya: Das Chikungunya-Virus ist ein einzelsträngiges RNA-Alphavirus, das typischerweise von den Aedes-Mücken auf einen anderen tierischen Wirt übertragen wird. Es gibt keine Hinweise darauf, dass Chikungunya einen Wirtswechsel zwischen Menschen und nicht-menschlichen Primaten behindern könnte, da er bei keiner bestimmten Primatenart bevorzugt wird. Es hat ein hohes Potenzial, in Sylvatic-Zyklen überzulaufen oder zurückzufließen, wie es bei dem ähnlichen Arbovirus der Fall war, das während des Sklavenhandels nach Amerika importiert wurde. Studien haben das Potenzial von Chikungunya zur oralen Infektion von sylvatischen Mückenarten wie Haemagogus leucocelaenus und Aedes terrens nachgewiesen . Darüber hinaus zeigten in einer serologischen Untersuchung, die an nichtmenschlichen Primaten in städtischen und stadtnahen Gebieten des Bundesstaates Bahia durchgeführt wurde , 11 Tiere neutralisierende Chikungunya- Antikörper .
- Dengue-Fieber: Das Dengue-Virus ist ein Flavivirus, das auch durch Aedes- Mückenvektoren auf andere tierische Wirte übertragbar ist. Dengue wurde zusammen mit Aedes aegypti auch durch den Sklavenhandel nach Amerika eingeführt . Eine Studie 2009 in Französisch - Guayana gefunden , dass Infektionen von Dengue - Viren - Typen 1 bis 4 in verschiedenen Arten von verschiedenen vorhanden waren neotropical Wald Säugetiere andere als Primaten wie Nagetiere , Beuteltiere und Fledermäuse . Nach Sequenzanalysen zeigte sich, dass die 4 nicht-humanen Säugerstämme einen Ähnlichkeitsindex von 89% bis 99% zu gleichzeitig zirkulierenden humanen Stämmen aufwiesen. Dies bestätigt, dass andere Säugetiere in der Nähe das Potenzial haben, durch menschliche Quellen infiziert zu werden, und weist auf das Vorhandensein eines städtischen Kreislaufs hin. Ein Fall, der beweist, dass die Arthropoden-Vektoren infiziert werden können, stammt aus Brasilien, wo Aedes albopictus (der die Hinterhöfe von Menschenhäusern besucht, sich aber leicht in ländliche, halbländliche und wilde Umgebungen ausbreitet) in São Paulo . mit dem Dengue-Virus 3 infiziert gefunden wurde Bundesland. Inzwischen im US- Bundesstaat Bahia, der silvatischen Vektor Haemogogus leucocelaenus wurde gefunden , mit Dengue - Virus infiziert wird 1. In einer weiteren Studie , die im durchgeführten Atlantischen Regenwald von Bahia, Primaten ( Leontopithecus chrysomelas und Sapajus xanthosternos ) wurde mit Antikörpern Dengueviren gefunden 1 und 2, während Faultiere ( Bradypus torquatus ) Antikörper gegen das Dengue-Virus 3 aufwiesen, was auf das mögliche Vorhandensein eines etablierten sylvatischen Zyklus hindeutet.
Wilde Tiere
Eine Vielzahl von Wildtieren mit Lebensräumen, in die der Mensch noch nicht vorgedrungen ist, werden durch verunreinigtes Wasser noch immer von Sapronotika befallen.
Giardien
- Biber : Giardia wurde den Bibern durch den Abfluss von menschlichem Abwasser stromaufwärts einer Biberkolonie eingeschleppt.
Influenza-A-Virus-Subtyp H1N1
- Robben : Im Jahr 1999 wurden wilde Robben mit grippeähnlichen Symptomen in ein niederländisches Rehabilitationszentrum für Robben aufgenommenund es wurde festgestellt, dass sie tatsächlich mit einem menschlichen Influenza-B- Virus infiziert waren, das 1995 beim Menschen zirkulierte und eine Antigenverschiebung durchgemacht hatteseit Anpassung an seinen neuen Siegelwirt.
Tuberkulose
- Rothirsch , Wildschwein : In Gebieten intensiver Wildbewirtschaftung, die Großwildzäune, Ergänzungsfutterstellen und Weidevieh umfassten, traten Fälle von Tuberkulose- Läsionen bei Wildrotwild und Wildschweinen auf. Einige Wildschweine und Hirsche teilten die gleichen Tuberkulosestämme, die denen ähnlich waren, die bei Nutztieren und Menschen gefunden wurden, was auf eine mögliche sapronotische oder saprozoonotische Kontamination gemeinsamer Wasserquellen, Ergänzungsfuttermittel, direkter Kontakt mit Menschen oder Vieh oder deren Ausscheidungen hindeutet.
Domestizierte Begleittiere
E coli
- Hunde , Pferde : Bei mehreren Hunden und Pferden in ganz Europa wurdenHinweise auf eine Infektion durch menschliche E. coli- Stämme gefunden, was die Möglichkeit einer zoonotischen interspeziellen Übertragung multiresistenter Stämme vom Menschen auf Haustiere und umgekehrt impliziert.
Tuberkulose
- Hund: Ein Yorkshire-Terrier wurde mit chronischem Husten, schlechter Gewichtsretention und Erbrechen monatelang in eine Tierklinik eingeliefert, wobei sich herausstellte, dass sich der Besitzer von Tuberkulose erholt hatte Tests und wurde entlassen. 8 Tage später wurde der Hund wegen einer Harnröhrenobstruktion euthanasiert . Eine Nekroskopie wurde durchgeführt, bei der Leber- und tracheobronchiale Lymphknotenproben tatsächlich positiv auf genau den gleichen Tuberkulose-Stamm getestet wurden, den der Besitzer zuvor hatte. Dies ist ein ganz klarer Fall von umgekehrter Zoonose.
Influenza-A-Virus-Subtyp H1N1
- Frettchen : Frettchen werden häufig in klinischen Studien am Menschen verwendet,daher wurde das Potenzial für eine Infektion mit der menschlichen Influenza zuvor bestätigt. Die Bestätigung der natürlichen Übertragung eines menschlichen H1N1-Stamms vom Ausbruch 2009 bei Haustierfrettchen impliziert jedoch weiter die Übertragung von Mensch zu Tier.
COVID-19
Inmitten der 2020 globalen Pandemie von COVID-19 , die Anfälligkeit von Katzen, Frettchen, Hunde, Hühner , Schweine und Enten auf die SARS-CoV-2 corona wurde untersucht und es wurde festgestellt , dass es sein kann , repliziert bei Katzen und Frettchen mit tödlichen Ergebnisse .
- Katzen : Das Virus kann zwischen Katzen über die Luft übertragen werden. Virale RNA wurde innerhalb von 3–5 Tagen nach der Infektion im Stuhl nachgewiesen, und pathologische Studien wiesen virale RNA im weichen Gaumen , in den Mandeln und in der Luftröhre nach . Kätzchen erworben massive Läsionen in der Lunge, Nasen- und Trachea Schleimhaut Epithelien . Die Überwachung von SARS-CoV-2 bei Katzen sollte als Ergänzung zur Eliminierung von COVID-19 beim Menschen in Betracht gezogen werden.
- Frettchen: Frettchen wurden mit Virusstämmen aus der Umgebung des Huanan Seafood Market in Wuhan, China, sowie mit menschlichen Isolaten aus Wuhan geimpft. Es wurde festgestellt, dass sich das Virus bei beiden Isolaten bis zu 8 Tage lang in den oberen Atemwegen von Frettchen vermehren kann, ohne Krankheit oder Tod zu verursachen, und virale RNA wurde in Rektalabstrichen nachgewiesen . Pathologische Studien, die nach 13 Tagen Infektion durchgeführt wurden, zeigten unter anderem eine leichte Peribronchitis in der Lunge, eine schwere lymphoplasmazytäre Perivaskulitis und Vaskulitis mit Antikörperproduktion gegen SARS-CoV-2, die bei allen Frettchen nachgewiesen wurde. Die Tatsache, dass sich SARS-CoV-2 in den oberen Atemwegen von Frettchen effizient repliziert, macht sie zu einem Tiermodell-Kandidat für die Bewertung antiviraler Medikamente oder Impfstoffkandidaten gegen COVID-19.
- Hunde: Von den Beagle Hunden getestet, viraler RNA in Fäkalien und 50% des Beagles festgestellt wurde , dass beimpft Serokonversion nach 14 Tagen , während das andere 50% blieb seronegativ eine geringe Anfälligkeit für SARS-CoV-2 bei Hunden demonstriert.
- Huhn, Ente, Schwein: Es gab keine Hinweise auf eine Anfälligkeit bei Hühnern, Enten oder Schweinen, wobei alle viralen RNA-Abstriche nach 14 Tagen nach der Inokulation negative Ergebnisse lieferten und seronegativ waren.
Domestizierte Nutztiere
Influenza-A-Virus-Subtyp H1N1
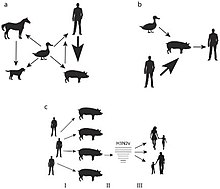
- Truthähne : Eine norwegische Herde des Truthahnzüchter zeigte einen Rückgang der Eierproduktion keine anderen klinischen Anzeichen nach einer Farm Hand berichtet mit H1N1 . Eine Studie ergab, dass die Truthähne auch H1N1 aufwiesen und für seine Antigene seropositiv waren. Im Eigelb wurden mütterlicherseits abgeleitete H1N1-Antikörper nachgewiesen und weitere genetische Analysen ergaben bei den Puten einen identischen H1N1-Stamm wie der Landarbeiter, der die Puten wahrscheinlich während der künstlichen Besamung infiziert hat.
- Schweine: Die Übertragung von H1N1 von Mensch zu Schwein wurde in Kanada und Korea gemeldet und umfasste während des Ausbruchs 2009 schließlich alle Kontinente außer der Antarktis. Es ist auch bekannt, dass es sich während saisonaler Epidemien in Frankreich zwischen Menschen und Schweinen ausbreitet .
Methicillin-resistenter Staphylococcus aureus
- Pferde: 11 Pferdepatienten, die aus verschiedenen Gründen über einen Zeitraum von ca. einem Jahr aus verschiedenen Betrieben in eine Tierklinik eingeliefert wurden, zeigten später MRSA- Infektionen. In Anbetracht der Tatsache, dass MRSA-Isolate bei Pferden äußerst selten sind, wurde vermutet, dass der MRSA-Ausbruch auf eine nosokomiale Infektion eines Menschen während des Krankenhausaufenthalts des Pferdes zurückzuführen war.
- Kühe, Truthähne, Schweine: Ein Fall von reverser Zoonose wurde vorgeschlagen, um zu erklären, wie ein bestimmter humaner Methicillin- sensitiver Streptococcus Aureus-Stamm in Nutztieren (Schweine, Truthähne, Kühe) mit nicht nur einem Verlust menschlicher Virulenzgene (was das Zoonosepotenzial verringern könnte) gefunden wurde zur Besiedlung des Menschen), aber auch die Zugabe einer Methicillin-Resistenz und eines Tetracyclins (was das Auftreten von MRSA-Infektionen erhöht). Die hier Sorge , dass ein übermäßiges ist der Gebrauch von Antibiotika in der Tierproduktion verschärft die Schaffung neuartiger Antibiotika - resistenter zoonotische Erreger .
Wilde Tiere in Gefangenschaft
Tuberkulose
- Elefanten : 1996 meldete die Hawthorne Circus Corporation, dass 4 ihrer Elefanten und 11 ihrer Pfleger M. tuberculosis- Infektionenbeherbergen. Leider waren diese Elefanten an verschiedene Zirkusveranstaltungen und zoologische Gärten in ganz Amerika untervermietet worden. Dies führte zu einer landesweiten Epidemie , aber da Tuberkulose keine Krankheit ist, die normalerweise von Tieren auf den Menschen übertragen wird, wurde vermutet, dass die Epidemie auf die Übertragung von einem menschlichen Führer auf einen in Gefangenschaft gehaltenen Elefanten zurückzuführen ist.
- Alpakas : Ein Ausbruch des Alpaka- Coronavirus im Jahr 2007 aufgrund der Vermischung bei einer nationalen Alpaka-Ausstellung führte zu einem Vergleich zwischen menschlichen und Alpaka-Coronaviren, um die Quelle des Ausbruchs abzuleiten. Es wurde festgestelltdass das Alpaka corona ist am evolutionär ähnlich einen menschlichen coronaStamm,in den 1960er Jahren isoliert wurde darauf hindeutetdass ein Alpaka corona seit Jahrzehnten im Umlauf sehr gut haben könnte verursachen Atemwegserkrankungen in für Mangel an diagnostischen Fähigkeiten Herden unentdeckt. Es deutet auch auf einen Übertragungsweg von Mensch zu Alpaka hin.
Helminthen und Protozoen
- Primaten : An der Universität von Ibadan Zoologischer Garten in Nigeria , Stuhlproben von zookeepers positiv getestet Würmern ( Ancylostoma duodenale , Ascaris und Peitschenwurm ) und Protozoen ( Giardia lamblia und Entamoeba histolytica ). Der exakt gleiche Stamm von Helminthen und Protozoenzysten wurde in den nicht-menschlichen Primaten des Zoos gefunden, was eine Zoonose zwischen den beiden impliziert.
Masern
- Nichtmenschliche Primaten: 1996 kam es in einem Schutzgebiet bei 94 nichtmenschlichen Primaten zu einem Masernausbruch . Obwohl die Quelle des Ausbruchs nie ermittelt wurde, zeigten Serum- und Urintests , dass das Virus definitiv mit den jüngsten Masernfällen beim Menschen in den USA in Verbindung gebracht wurde
Helicobacter pylori
- Beuteltiere : Das Streifengesichts-Dunnart ist ein australisches Beuteltier, dasin Gefangenschaftmehreren Ausbrüchen von Helicobacter pylori ausgesetzt war . Magenproben aus dem Beuteltier ergaben, dass derfür die Ausbrüche verantwortliche H. pylori- Stamm zu 100 % mit einem Stamm übereinstimmte, der aus dem menschlichen Darmtrakt stammt. Somit kann davon ausgegangen werden, dass der Ausbruch von den Behandlern verursacht wurde.
Wilde Tiere in Schutzgebieten
- Schimpansen : In den Jahren2016 bis 2017 wurdedie Übertragung des menschlichen Coronavirus HCoV-OC43 auf wildlebende Schimpansen ( Pan troglodytes verus ) im Taï-Nationalpark , Côte d´Ivoire, gemeldet Gemeinschaften seit den 1980er Jahren Das zur Spezies Betacoronavirus 1 (BetaCoV1)gehörende HCoV-OC43verursachtbeim Menschennormalerweise Erkältungsepisoden (dies schließt SARS und MERS aus ), wurde aber auch bei Huftieren , Fleischfressern und Hasentieren nachgewiesen . Daher ist es völlig plausibel, dass Forscher oder Wilderer das Virus versehentlich auf die Schimpansen übertragen haben und damit eine weitere Schnittstelle beim Wechsel des Coronavirus-Wirts aufgedeckt haben.
Rhinovirus C
- Schimpansen: Obwohl das menschliche Rhinovirus C zuvor als einzigartiger menschlicher Krankheitserreger galt, wurde festgestellt, dass es 2013 die Ursache für einen Ausbruch von Atemwegsinfektionen bei Schimpansen in Uganda war . Die Untersuchung von Schimpansen aus ganz Afrika ergab, dass sie eine universelle Homozygotie für das 3 CDHR3-Y529- Allel (ein mit Cadherin verwandtes Familienmitglied) aufweisen, ein Rezeptor , der die Anfälligkeit für Rhinovirus-C-Infektionen und Asthma beim Menschen drastisch erhöht . Wenn Atemwegsviren menschlichen Ursprungs in der Lage sind, die Zirkulation in nichtmenschlichen Primaten aufrechtzuerhalten, würde sich dies als schädlich erweisen, sollte die Infektion auf menschliche Gemeinschaften zurückgreifen.
Tuberkulose
- Elefanten: Bei einer Nekroskopie eines frei lebenden afrikanischen Elefanten ( Loxodonta africana ) im Krüger-Nationalpark in Südafrika wurden erhebliche Lungenschäden durch einen menschlichen Stamm von M. tuberculosis festgestellt . Elefanten erkunden ihre Umgebung mit ihren Rüsseln, daher war es sehr wahrscheinlich, dass aerosolisierte Krankheitserreger aus dem Hausmüll, kontaminiertes Wasser einer flussaufwärts gelegenen Menschengemeinschaft, menschliche Exkremente oder kontaminierte Lebensmittel von Touristen die Infektionsquelle waren.
Pneumoviren
- Schimpansen: In Uganda infizierten Berichte über Atemwegsviren menschlichen Ursprungs zwei Schimpansengemeinschaften (Pan troglodytes schweinfurthii) im selben Wald. Später wurde entdeckt, dass es durch ein humanes Metapneumovirus (auch bekannt als MPV, Pneumoviridae , Metapneumovirus ) und ein humanes Respirovirus 3 (auch bekannt als HRV3, Paramyxoviridae , Respirovirus oder früher bekannt als Parainfluenzavirus 3 ) verursacht wird.
Umgekehrte Zoonose bei Gorillas
- Gorillas : Schutzgebiete mit Ökotourismus in Uganda, Ruanda und der Demokratischen Republik Kongo , frei lebende Gorillas haben sich zunehmend an die Anwesenheit von Menschen gewöhnt, sei es in Form von Rangerführern, Touristen, Fährtenlesern, Tierärzten, Wilderern , oder Forscher. Iodamoeba buetschlii , Giardia lamblia , Chilomastix sp. , Endolimax nana , Entamoeba coli und Entamoeba histolytica wurden im Kot von Gorillas und promiskuitiven Defäkationen gefunden, die von Menschen hinterlassen wurden, die in den Lebensraum eindrangen. Darüber hinaus erhöhte sich die Zahl von Cryptosporidium sp. und Kapillarinfektionen wurden bei Gorillas gefunden, die häufiger Kontakt mit Menschen hatten als solche, die dies nicht taten. Zusammengenommen deuten diese Ergebnisse auf das Auftreten von reversen Zoonosen hin.