Hexosaminidase - Hexosaminidase
| β-N-Acetylhexosaminidase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
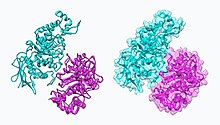 Hexosaminidase A (Hex A)
| |||||||||
| Identifikatoren | |||||||||
| EG-Nr. | 3.2.1.52 | ||||||||
| CAS-Nr. | 9012-33-3 | ||||||||
| Datenbanken | |||||||||
| IntEnz | IntEnz-Ansicht | ||||||||
| BRENDA | BRENDA-Eintrag | ||||||||
| ExPASy | NiceZyme-Ansicht | ||||||||
| KEGG | KEGG-Eintrag | ||||||||
| MetaCyc | Stoffwechselweg | ||||||||
| PRIAM | Profil | ||||||||
| PDB- Strukturen | RCSB PDB PDBe PDBsum | ||||||||
| Gen-Ontologie | AmiGO / QuickGO | ||||||||
| |||||||||
Hexosaminidase ( EC 3.2.1.52 , beta-acetylaminodeoxyhexosidase , N-Acetyl-beta-D-Hexosaminidase , N-Acetyl-beta-Hexosaminidase , N-Acetyl - Hexosaminidase , beta-Hexosaminidase , beta-acetylhexosaminidinase , beta-DN-acetylhexosaminidase , beta- N-Acetyl-D-Hexosaminidase , Beta-N-Acetylglucosaminidase , Hexosaminidase A , N-Acetylhexosaminidase , Beta-D-Hexosaminidase ) ist ein Enzym, das an der Hydrolyse terminaler N-Acetyl-D- Hexosamin- Reste in N-Acetyl-β . beteiligt ist -D-Hexosaminide.
Erhöhte Hexosaminidase-Spiegel im Blut und/oder Urin wurden als Biomarker für einen Rückfall bei der Behandlung von Alkoholismus vorgeschlagen.
Isozyme und Gene
Lysosomale A-, B- und S-Isozyme
Funktionelle lysosomale β-Hexosaminidase-Enzyme haben eine dimere Struktur. Drei Isozyme werden durch die Kombination von α- und β-Untereinheiten produziert, um eines von drei aktiven Dimeren zu bilden:
| Hexosaminidase- Isozym |
Untereinheitszusammensetzung | Funktion |
|---|---|---|
| EIN | α/β-Heterodimer | einziges Isozym, das G M2- Gangliosid in vivo hydrolysieren kann |
| B | β/β-Homodimer | existiert in Geweben, aber keine bekannte physiologische Funktion |
| S | α/α-Homodimer | existiert in Geweben, aber keine bekannte physiologische Funktion |
Die α- und β-Untereinheiten werden von separaten Genen, HEXA bzw. HEXB , kodiert . Beta-Hexosaminidase und das Cofaktor G M2- Aktivatorprotein katalysieren den Abbau der G M2- Ganglioside und anderer Moleküle, die terminale N-Acetylhexosamine enthalten. Genmutationen in HEXB führen oft zur Sandhoff-Krankheit ; wohingegen Mutationen in HEXA die Hydrolyse von G M2- Gangliosiden verringern , was die Hauptursache der Tay-Sachs-Krankheit ist .
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Funktion
Auch wenn die Alpha- und Beta - Untereinheiten von lysosomalen Hexosaminidase können beide cleave GalNAc Reste nur die Alpha - Untereinheit ist in der Lage zu hydrolysieren G M2 Gangliosid aufgrund eines Schlüsselrest, Arg -424, und eine Schleifenstruktur , die Formen von der Aminosäuresequenz in der Alpha-Untereinheit. Die Schleife in der alpha - Untereinheit, bestehend aus Gly -280, Ser -281, Glu -282 und Pro -283 , die in der Beta - Untereinheit nicht vorhanden ist, dienen als eine ideale Struktur für die Bindung des G M2 Aktivatorprotein (G M2 AP) und Arginin ist essentiell für die Bindung des N-Acetyl-Neuraminsäure-Rests von G M2- Gangliosiden. Das G M2- Aktivatorprotein transportiert G M2- Ganglioside und präsentiert die Lipide der Hexosaminidase, sodass ein funktionelles Hexosaminidase-Enzym in der Lage ist, G M2- Ganglioside in G M3- Ganglioside zu hydrolysieren, indem es den N-Acetylgalactosamin (GalNAc)-Rest von G M2- Gangliosiden entfernt.
Wirkmechanismus
Ein Michaelis-Komplex bestehend aus einem Glutamat- Rest, einem GalNAc-Rest am G M2- Gangliosid und einem Aspartat- Rest führt zur Bildung eines Oxazoliniumion-Zwischenprodukts. Ein Glutamatrest (alpha-Glu-323/beta-Glu-355) wirkt als Säure, indem er seinen Wasserstoff an das glykosidische Sauerstoffatom am GalNAc-Rest abgibt. Ein Aspartatrest (alpha-Asp-322/beta-Asp-354) positioniert die C2-Acetamindo-Gruppe so, dass sie vom Nukleophil (N-Acetamido-Sauerstoffatom an Kohlenstoff 1 des Substrats) angegriffen werden kann. Der Aspartatrest stabilisiert die positive Ladung am Stickstoffatom im Oxazoliniumion-Zwischenprodukt. Nach der Bildung des Oxazoliniumion-Zwischenprodukts greift Wasser den elektrophilen Acetalkohlenstoff an. Glutamat wirkt als Base, indem es das Wasser deprotoniert, was zur Bildung des Produktkomplexes und des G M3- Gangliosids führt.
Genmutationen, die zur Tay-Sachs-Krankheit führen
Es gibt zahlreiche Mutationen, die zu einem Hexosaminidase-Mangel führen, einschließlich Gendeletionen, Nonsense-Mutationen und Missense-Mutationen. Die Tay-Sachs-Krankheit tritt auf, wenn Hexosaminidase A ihre Funktionsfähigkeit verliert. Menschen mit Tay-Sachs-Krankheit sind nicht in der Lage, den GalNAc-Rest aus dem G M2- Gangliosid zu entfernen , und speichern als Ergebnis 100- bis 1000-mal mehr G M2- Ganglioside im Gehirn als der normale Mensch. Allein in infantilen Fällen der Tay-Sachs-Krankheit wurden über 100 verschiedene Mutationen entdeckt.
Die häufigste Mutation, die bei über 80 Prozent der Tay-Sachs-Patienten auftritt, resultiert aus einer Addition von vier Basenpaaren (TATC) im Exon 11 des Hex-A-Gens. Diese Insertion führt zu einem frühen Stoppcodon , das den Hex-A-Mangel verursacht.
Kinder, die mit Tay-Sachs geboren werden, sterben normalerweise zwischen zwei und vier Jahren an Aspiration und Lungenentzündung . Tay-Sachs verursacht zerebrale Degeneration und Blindheit. Die Patienten erleben auch schlaffe Extremitäten und Krampfanfälle. Zu diesem Zeitpunkt gibt es keine Heilung oder wirksame Behandlung der Tay-Sachs-Krankheit.
NAG-Thiazolin, NGT, wirkt als mechanismusbasierter Inhibitor der Hexosaminidase A. Bei Patienten mit Tay-Sachs-Krankheit (fehlgefaltete Hexosaminidase A) wirkt NGT als molekulares Chaperon, indem es an das aktive Zentrum von Hexosaminidase A bindet, was zur Bildung einer richtig gefalteten Hexosaminidase beiträgt A. Die stabile Dimer-Konformation von Hexosaminidase A hat die Fähigkeit, das endoplasmatische Retikulum zu verlassen und wird zum Lysosom geleitet, wo es den Abbau von GM2- Gangliosiden durchführen kann. Die beiden Untereinheiten der Hexosaminidase A sind unten dargestellt:
Zytosolische C- und D-Isozyme
Das bifunktionelle Protein nCoats ( n uclear c ytoplasmic O -GlcNAcase und ein Cetyl t ransferase) , die durch das kodiert wird MGEA5 Gen sowohl Hexosaminidase und besitzt eine Histon - Acetyltransferase - Aktivitäten. NCOAT ist auch als Hexosaminidase C bekannt und weist im Vergleich zur lysosomalen Hexosaminidase A unterschiedliche Substratspezifitäten auf. Ein Einzelnukleotid-Polymorphismus im menschlichen O-GlcNAcase-Gen ist mit Diabetes mellitus Typ 2 verbunden .
Ein viertes Säugetier-Hexosaminidase-Polypeptid, das als Hexosaminidase D ( HEXDC ) bezeichnet wurde, wurde kürzlich identifiziert.
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Verweise
Externe Links
- GeneReviews/NCBI/NIH/UW-Eintrag zu Hexosaminidase-A-Mangel, Tay-Sachs-Krankheit
- Hexosaminidase A an der US National Library of Medicine Medical Subject Headings (MeSH)
- EG 3.2.1.52




