Schwefeloxosäure - Sulfur oxoacid
Die Schwefel Oxosäuren sind chemische Verbindungen , die enthalten Schwefel , Sauerstoff und Wasserstoff . Die bekannteste und wichtigste industriell verwendete ist Schwefelsäure . Schwefel hat mehrere Oxosäuren; Einige davon sind jedoch nur aus ihren Salzen bekannt (diese sind in der folgenden Tabelle kursiv dargestellt). Die charakterisierten Säuren enthalten eine Vielzahl von Strukturmerkmalen, zum Beispiel:
- tetraedrischer Schwefel, wenn er an Sauerstoff koordiniert ist
- terminale und verbrückende Sauerstoffatome
- terminale Peroxogruppen
- Klemme S = S.
- Ketten von (−S−) n
| Acid | Formel | Formale Oxidationszahl | Struktur | Verwandte Anionen | Anmerkungen |
|---|---|---|---|---|---|
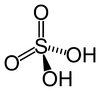
| Schwefelsäure | H 2 SO 4 | +6 |
|
Sulfat , SO 2− 4 und Schwefelwasserstoff, allgemein bekannt als Bisulfat , HSO - 4 |
Am bekanntesten und industriell bedeutsam. |
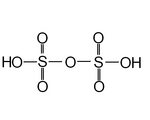
| Polysulfonsäuren, einschließlich Disulfursäure oder Pyrosulfonsäure | H 2 SO 4 · n SO 3 | +6 |
|
Disulfat (allgemein bekannt als Pyrosulfat ), S. 2 Ö 2− 7 und Trisulfat, S. 3 Ö 2− 10 |
Reine Schwefelsäure schmilzt bei 36 ° C. Vorhanden in rauchender Schwefelsäure, Oleum . Beispiele bekannt für n = 1 und n = 2. |
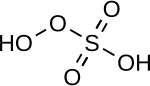
| Peroxymonoschwefelsäure | H 2 SO 5 | +6 |
|
Peroxomonosulfat , OOSO 2− 3 |
"Carosäure", ein Feststoff, der bei 45 ° C schmilzt |
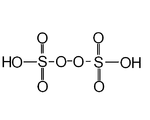
| Peroxydisulfonsäure | H 2 S 2 O 8 | +6 |
|
Peroxydisulfat , O. 3 SOO SO 2− 3 |
"Marshall's Acid", ein Feststoff, der bei 65 ° C schmilzt. |
| Dithionsäure | H 2 S 2 O 6 | +5 |

|
Dithionate , O. 3 SSO 2− 3 |
Nicht in reiner Form isoliert, es wurden nur konzentrierte Lösungen hergestellt |
| Thiosulfonsäure | H 2 S 2 O 3 | 0 (für den terminalen Schwefel), +4 (für das Zentralatom) |
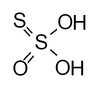
|
Thiosulfat , S. 2 Ö 2− 3 Hydrogenthiosulfat HS 2 Ö - 3 (Ammoniumsalz, hergestellt in wasserfreiem Methanol bei –80 ° C) |
Wässrige Lösungen zersetzen sich. |
| Schwefelsäure oder pyroschwefelsäure | H 2 S 2 O 5 | +5 (des an 3 Sauerstoffatome gebundenen Schwefelatoms), +3 (des anderen Schwefelatoms) |
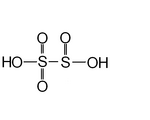
|
Disulfit allgemein bekannt als Metabisulfit , S. 2 Ö 2− 5 |
Nicht bekannt. |
| Schwefelsäure | H 2 SO 3 | +4 |
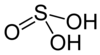
|
Bisulfit , HSO - 3 und Sulfit , SO 2− 3 |
Nicht bekannt. |
| Dithionsäure | H 2 S 2 O 4 | +3 |

|
Dithionit , O. 2 SSO 2− 2 |
Nicht bekannt. |
| Sulfoxylsäure | H 2 SO 2 | +2 |
|
Sulfoxylat , SO 2− 2 |
Freie Säure nicht bekannt |
| Polythionsäure | H 2 S x O 6 | 0 (für die verbrückenden S-Atome), +5 (für die terminalen zentralen S-Atome) |

|
Polythionate , O. 3 S (S. x −2 )SO 2− 3 . Beispiel Trithionat , Tetrathionat , Pentathionat , Hexathionat , Heptathionat , Octathionat , Nichtathionat , Decathionat , Undecathionat , Dodecathionat , Tridecathionat und Tetradecathionat . |
Beispiele bekannt mit x = 3, 4, 5, 6, 7, 8, 10, 12, 14. |
| Thiosulfonsäure | H 2 S 2 O 2 | −1 (für das äußere Schwefelatom), +3 (für das Zentralatom) |
|
Thiosulfite | Nicht bekannt |
| Dihydroxydisulfan | H 2 S 2 O 2 | +1 |
|
Säure bekannt |
Siehe auch
- Chlorschwefelsäure
- Fluorschwefelsäure
- Nitrosylschwefelsäure
- Peroxydisulfonsäure
- Sulfinsäuren
- Sulfonsäuren
Verweise
Externe Links
- Schwefel + Säuren in der US-amerikanischen Nationalbibliothek für Medizin Medizinische Themen (MeSH) Schwefeloxosäuren zusammen mit anderen schwefelhaltigen Säuren
