Ca v 1.2 -Cav1.2
Der Calciumkanal, spannungsabhängig, L-Typ, Alpha 1C-Untereinheit (auch bekannt als Ca v 1.2 ) ist ein Protein , das beim Menschen vom CACNA1C- Gen kodiert wird . Ca v 1.2 ist eine Untereinheit des spannungsabhängigen Calciumkanals vom L-Typ .
Struktur und Funktion
Dieses Gen kodiert für eine Alpha-1-Untereinheit eines spannungsabhängigen Calciumkanals . Calcium - Kanäle vermitteln den Einstrom von Calciumionen (Ca 2+ ) in die Zelle auf Membranpolarisation (siehe Membranpotential und Calcium in der Biologie ).
Die Alpha-1-Untereinheit besteht aus 24 Transmembransegmenten und bildet die Pore, durch die Ionen in die Zelle gelangen. Der Calciumkanal besteht aus einem Komplex von Alpha-1-, Alpha-2/Delta- und Beta-Untereinheiten im Verhältnis 1:1:1. Die S3-S4-Linker von Cav1.2 bestimmen den Gating-Phänotyp und die modulierte Gating-Kinetik des Kanals. Cav1.2 wird häufig in der glatten Muskulatur , in Pankreaszellen , Fibroblasten und Neuronen exprimiert . Es ist jedoch besonders wichtig und bekannt für seine Expression im Herzen, wo es L-Typ-Ströme vermittelt, die eine Calcium-induzierte Calciumfreisetzung aus den ER-Speichern über Ryanodinrezeptoren bewirken . Es depolarisiert bei -30 mV und hilft, die Form des Aktionspotentials in Herz- und glatter Muskulatur zu definieren. Das von diesem Gen kodierte Protein bindet an Dihydropyridin und wird von diesem gehemmt . In den Arterien des Gehirns erhöht ein hoher Kalziumspiegel in den Mitochondrien die Aktivität des nuklearen Faktors Kappa B NF-κB und die Transkription von CACNA1c und die funktionelle Cav1.2-Expression steigen. Cav1.2 reguliert auch den Osteoprotegerinspiegel .
Ca V 1.2 wird durch die Wirkung von STIM1 gehemmt .
Verordnung
Die Aktivität der CaV1.2-Kanäle wird stark durch die von ihnen erzeugten Ca 2+ -Signale reguliert . Eine Erhöhung der intrazellulären Ca 2+ Konzentration in Cav1.2 Erleichterung gebracht, eine Form der positiven Rückkopplung genannt Ca 2+ -abhängigen Erleichterung, daß verstärkt Ca 2+ -Einstroms. Darüber hinaus hat die Zunahme der intrazellulären Ca 2+ -Konzentration des Einströmens impliziert, dass sie den gegenteiligen Effekt der Ca 2+ -abhängigen Inaktivierung ausübt. Diese Aktivierungs- und Inaktivierungsmechanismen beinhalten beide die Ca 2+ -Bindung an Calmodulin (CaM) in der IQ-Domäne im C-terminalen Schwanz dieser Kanäle. Cav1.2-Kanäle sind in der Zellmembran im Durchschnitt zu acht Clustern angeordnet. Wenn Calciumionen an Calmodulin binden, das wiederum an einen Cav1.2-Kanal bindet, ermöglicht es den Cav1.2-Kanälen innerhalb eines Clusters, miteinander zu interagieren. Dies führt dazu, dass Kanäle kooperativ arbeiten, wenn sie sich gleichzeitig öffnen, um mehr Kalziumionen eindringen zu lassen und sich dann zu schließen, damit sich die Zelle entspannen kann.

Klinische Bedeutung
Mutationen im CACNA1C-Gen, dem Einzelnukleotid-Polymorphismus im dritten Intron des Cav1.2-Gens, werden mit einer Variante des Long-QT-Syndroms namens Timothy-Syndrom und auch mit dem Brugada-Syndrom in Verbindung gebracht . Groß angelegte genetische Analysen haben die Möglichkeit gezeigt, dass CACNA1C mit einer bipolaren Störung und später auch mit Schizophrenie in Verbindung gebracht wird . Außerdem wurde ein CACNA1C-Risikoallel mit einer Störung der Gehirnkonnektivität bei Patienten mit bipolarer Störung in Verbindung gebracht, während dies bei ihren nicht betroffenen Verwandten oder gesunden Kontrollpersonen nicht oder nur in geringem Maße gegeben ist.
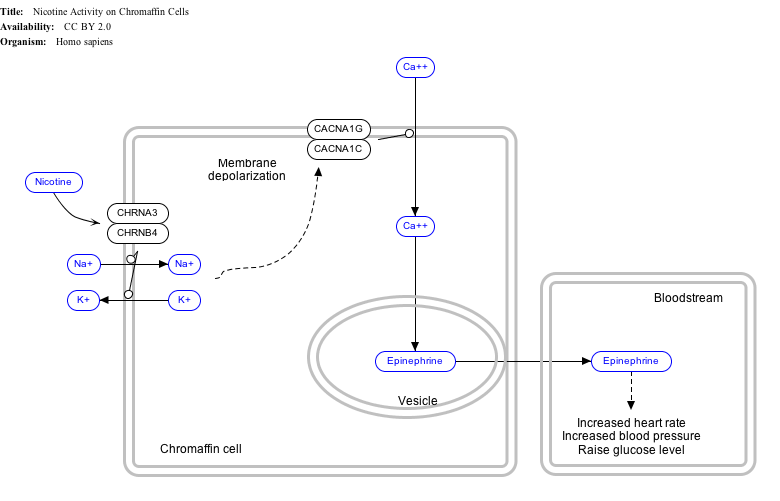
Interaktiver Wegplan
Klicken Sie unten auf Gene, Proteine und Metaboliten, um zu den entsprechenden Wikipedia-Artikeln zu verlinken.
Siehe auch
Verweise
Weiterlesen
- Kempton MJ, Ruberto G, Vassos E, Tatarelli R, Girardi P, Collier D, Frangou S (Dezember 2009). „Auswirkungen des CACNA1C-Risikoallels für bipolare Störungen auf das Volumen der zerebralen grauen Substanz bei gesunden Personen“. Das amerikanische Journal für Psychiatrie . 166 (12): 1413–4. doi : 10.1176/appi.ajp.2009.09050680 . PMID 19952088 .
- Soldatov NM (Mai 1992). "Molekulare Vielfalt von L-Typ Ca2+-Kanal-Transkripten in menschlichen Fibroblasten" . Proceedings of the National Academy of Sciences of the United States of America . 89 (10): 4628–32. Bibcode : 1992PNAS...89.4628S . doi : 10.1073/pnas.89.10.4628 . PMC 49136 . PMID 1316612 .
- Powers PA, Gregg RG, Hogan K (September 1992). „Verbindungskartierung des menschlichen Gens für die Alpha-1-Untereinheit des kardialen DHP-sensitiven Ca2+-Kanals (CACNL1A1) auf Chromosom 12p13.2-pter unter Verwendung einer Dinukleotidwiederholung“. Genomik . 14 (1): 206–7. doi : 10.1016/S0888-7543(05)80312-X . PMID 1330882 .
- Sun W, McPherson JD, Hoang DQ, Wasmuth JJ, Evans GA, Montal M (Dezember 1992). „Mapping eines menschlichen Gehirns spannungsgesteuerten Kalziumkanals auf das menschliche Chromosom 12p13-pter“. Genomik . 14 (4): 1092–4. doi : 10.1016/S0888-7543(05)80135-1 . PMID 1335957 .
- Powers PA, Gregg RG, Lalley PA, Liao M, Hogan K (Juli 1991). „Zuordnung des menschlichen Gens für die Alpha-1-Untereinheit des kardialen DHP-sensitiven Ca2+-Kanals (CCHL1A1) zum Chromosom 12p12-pter“. Genomik . 10 (3): 835–9. doi : 10.1016/0888-7543(91)90471-P . PMID 1653763 .
- Perez-Reyes E., Wei XY, Castellano A, Birnbaumer L (Nov. 1990). "Molekulare Vielfalt von L-Typ-Calciumkanälen. Beweise für alternatives Spleißen der Transkripte von drei nicht-allelischen Genen" . Die Zeitschrift für biologische Chemie . 265 (33): 20430–6. doi : 10.1016/S0021-9258(17)30522-7 . PMID 2173707 .
- Soldatov NM, Bouron A, Reuter H (Mai 1995). „Unterschiedliche spannungsabhängige Hemmung durch Dihydropyridine von humanen Ca2+-Kanal-Spleißvarianten“ . Die Zeitschrift für biologische Chemie . 270 (18): 10540–3. doi : 10.1074/jbc.270.18.10540 . PMID 7737988 .
- Soldatov NM (Juli 1994). „Genomische Struktur des menschlichen L-Typ-Ca2+-Kanals“. Genomik . 22 (1): 77–87. doi : 10.1006/geno.1994.1347 . PMID 7959794 .
- Tang S, Mikala G, Bahinski A, Yatani A, Varadi G, Schwartz A (Juni 1993). "Molekulare Lokalisierung von Ionenselektivitätsstellen innerhalb der Pore eines menschlichen kardialen Calciumkanals vom L-Typ" . Die Zeitschrift für biologische Chemie . 268 (18): 13026–9. doi : 10.1016/S0021-9258(19)38613-2 . PMID 8099908 .
- Schultz D, Mikala G, Yatani A, Engle DB, Iles DE, Segers B, Sinke RJ, Weghuis DO, Klöckner U, Wakamori M (Juli 1993). "Klonierung, chromosomale Lokalisation und funktionelle Expression der Alpha-1-Untereinheit des spannungsabhängigen Calciumkanals vom L-Typ aus dem normalen menschlichen Herzen" . Proceedings of the National Academy of Sciences of the United States of America . 90 (13): 6228–32. Bibcode : 1993PNAS...90.6228S . doi : 10.1073/pnas.90.13.6228 . PMC 46901 . PMID 8392192 .
- Perets T, Blumenstein Y, Shistik E, Lotan I, Dascal N (Apr 1996). „Ein potenzieller Ort der funktionellen Modulation durch Proteinkinase A in der kardialen Ca2+-Kanal-Alpha 1C-Untereinheit“ . FEBS-Briefe . 384 (2): 189–92. doi : 10.1016/0014-5793(96)00303-1 . PMID 8612821 . S2CID 40550657 .
- Andersson B, Wentland MA, Ricafrente JY, Liu W, Gibbs RA (Apr 1996). „Eine „Doppeladapter“-Methode für eine verbesserte Konstruktion der Schrotflintenbibliothek“. Analytische Biochemie . 236 (1): 107–13. doi : 10.1006/abio.1996.0138 . PMID 8619474 .
- Soldatov NM, Zühlke RD, Bouron A, Reuter H (Februar 1997). "Molekulare Strukturen, die an der Inaktivierung des L-Typ-Calciumkanals beteiligt sind. Rolle der Carboxyl-terminalen Region, die von den Exons 40-42 in der alpha1C-Untereinheit kodiert wird, in der Kinetik und der Ca2+-Abhängigkeit der Inaktivierung" . Die Zeitschrift für biologische Chemie . 272 (6): 3560–6. doi : 10.1074/jbc.272.6.3560 . PMID 9013606 .
- Klöckner U, Mikala G, Eisfeld J, Iles DE, Strobeck M, Mershon JL, Schwartz A, Varadi G (März 1997). „Eigenschaften von drei COOH-terminalen Spleißvarianten einer menschlichen kardialen L-Typ Ca2+-Kanal-Alpha1-Untereinheit“. Das American Journal of Physiology . 272 (3 Pt 2): H1372–81. doi : 10.1152/ajpheart.1997.272.3.H1372 . PMID 9087614 .
- Yu W, Andersson B, Worley KC, Muzny DM, Ding Y, Liu W, Ricafrente JY, Wentland MA, Lennon G, Gibbs RA (Apr 1997). "Verkettungs-cDNA-Sequenzierung im großen Maßstab" . Genomforschung . 7 (4): 353–8. doi : 10.1101/gr.7.4.353 . PMC 139146 . PMID 9110174 .
- Gao T, Yatani A, Dell'Acqua ML, Sako H, Green SA, Dascal N, Scott JD, Hosey MM (Juli 1997). „Die cAMP-abhängige Regulation kardialer Ca2+-Kanäle vom L-Typ erfordert Membran-Targeting von PKA und Phosphorylierung von Kanaluntereinheiten“ . Neuron . 19 (1): 185–96. doi : 10.1016/S0896-6273(00)80358-X . PMID 9247274 . S2CID 3253007 .
- Zühlke RD, Bouron A, Soldatov NM, Reuter H (Mai 1998). „Die Ca2+-Kanal-Sensitivität gegenüber dem Blocker Isradipin wird durch alternatives Spleißen des menschlichen alpha1C-Untereinheitsgens beeinflusst“. FEBS-Briefe . 427 (2): 220–4. doi : 10.1016/S0014-5793(98)00425-6 . PMID 9607315 . S2CID 32580111 .
- Meyers MB, Puri TS, Chien AJ, Gao T, Hsu PH, Hosey MM, Fishman GI (Juli 1998). „Sorcin assoziiert mit der porenbildenden Untereinheit von spannungsabhängigen Ca2+-Kanälen vom L-Typ“ . Die Zeitschrift für biologische Chemie . 273 (30): 18930–5. doi : 10.1074/jbc.273.30.18930 . PMID 9668070 .
- Liu WS, Soldatov NM, Gustavsson I, Chowdhary BP (1999). „Faser-FISH-Analyse der 3'-terminalen Region des menschlichen L-Typ-Ca2+-Kanal-alpha 1C-Untereinheitsgens“. Heredita . 129 (2): 169–75. doi : 10.1111/j.1601-5223.1998.00169.x . PMID 10022083 .
Externe Links
- GeneReviews/NIH/NCBI/UW-Eintrag zum Brugada-Syndrom
- CACNA1C+protein,+human an der US National Library of Medicine Medical Subject Headings (MeSH)
- GeneReviews/NIH/NCBI/UW-Eintrag zum Timothy-Syndrom
Dieser Artikel enthält Texte der National Library of Medicine der Vereinigten Staaten , die gemeinfrei sind .