Etonitazene - Etonitazene
 | |
 | |
| Klinische Daten | |
|---|---|
| ATC-Code | |
| Rechtsstellung | |
| Rechtsstellung | |
| Identifikatoren | |
| |
| CAS-Nummer | |
| PubChem- CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| ChEMBL | |
| CompTox-Dashboard ( EPA ) | |
| ECHA-Infokarte |
100.011.827 |
| Chemische und physikalische Daten | |
| Formel | C 22 H 28 N 4 O 3 |
| Molmasse | 396.491 g·mol -1 |
| 3D-Modell ( JSmol ) | |
| |
| |
|
| |
Etonitazen ist ein schmerzstillendes Medikament, das erstmals 1957 veröffentlicht wurde und bei Tieren eine ungefähr eintausend- bis eintausendfünfhundertfache Potenz von Morphin aufweist
Da es durch ein starkes Abhängigkeitspotential und eine Neigung zu einer starken Atemdepression gekennzeichnet ist , wird es beim Menschen nicht angewendet. Es ist jedoch in Tiermodellen für Suchtstudien nützlich , insbesondere wenn die Tiere das Mittel trinken oder einnehmen müssen, da es nicht so bitter ist wie Opiatsalze wie Morphinsulfat .
unerlaubte Produktion
Die illegale Produktion und der Verkauf von Etonitazen wurden eingeschränkt. 1998 auf dem Moskauer illegalen Drogenmarkt entdeckt , wurde es hauptsächlich in geschnürten Zigaretten geraucht. Ein Chemiker bei Morton Thiokol stellte die Verbindung her und gab sie in einen Naseninhalator. Das Medikament wurde 1996 in Russland hergestellt und als „Chinesischer Zwerg“ verkauft. Das Medikament führte aufgrund seiner ungewissen Wirksamkeit zu einer unbestätigten Anzahl von Todesfällen. Es scheint eine steile Dosis-Wirkungs-Kurve und eine unvorhersehbare Pharmakokinetik zu haben, insbesondere wenn es injiziert wird, ähnlich wie einige andere potente Opioide wie Dextromoramid , was dazu führen kann, dass Etonitazen im Vergleich zu Opioiden ähnlicher Wirksamkeit wie Fentanyl besonders gefährlich ist .
Analoga
Es sind eine Reihe von Analoga bekannt, wobei die einzige andere bekannte Verbindung, die aus der ursprünglichen Forschung der 1950er Jahre stammt, Clonitazen ist , das viel schwächer ist als Etonitazen (etwa 3x Morphin). In jüngerer Zeit, seit etwa Ende 2018, sind eine Reihe von Designer- Analoga auf illegalen Märkten auf der ganzen Welt aufgetaucht , wobei die bekanntesten Verbindungen Metonitazen , Isotonitazen und Etazen sind , obwohl andere weiterhin auftauchen.
Von diesen Analoga sind nur Etonitazen und Clonitazen ausdrücklich unter UN-Konventionen aufgeführt und werden daher weltweit kontrolliert. Der Rest wäre nur in Ländern wie den USA, Australien und Neuseeland illegal, die Gesetze haben, die dem Federal Analog Act gleichwertig sind . In den Vereinigten Staaten handelt es sich um eine narkotisch kontrollierte Substanz der Liste I mit einem DEA ASCCN von 9624 und einer jährlichen Produktionsquote von null ab 2013.
Synthese
Etonitazen und den damit verbundenen Opioid - Agonisten Benzimidazole wurden in den späten 1950er Jahren von einem Team von Schweizer Forscher entdeckten bei der Pharmafirma arbeitet CIBA (heute Novartis ). Eine der ersten vom Schweizer Team untersuchten Verbindungen war 1- (β-Diethylaminoethyl) -2-benzylbenzimidazol, von dem festgestellt wurde, dass es 10% der analgetischen Aktivität von Morphin besitzt, wenn es in Nagetier-Bioassays getestet wurde. Dieser Befund ermutigte die Gruppe, eine umfassende systematische Untersuchung von 2-Benzylbenzimidazolen zu beginnen und die Struktur-Wirkungs-Beziehung dieser neuen Familie von Analgetika zu ermitteln. Zur Herstellung dieser Verbindungen wurden zwei allgemeine Synthesemethoden entwickelt.
Das erste Verfahren beinhaltete die Kondensation von o-Phenylendiamin mit Phenylacetonitril , um ein 2-Benzylbenzimidazol zu bilden. Das Benzimidazol wird dann mit dem gewünschten 1-Chlor-2-dialkylaminoethan alkyliert, wodurch das Endprodukt gebildet wird. Dieses spezielle Verfahren war am nützlichsten für die Herstellung von Benzimidazolen, denen Substituenten an den Benzolringen fehlten. Ein Diagramm dieser Methode wird unten angezeigt.
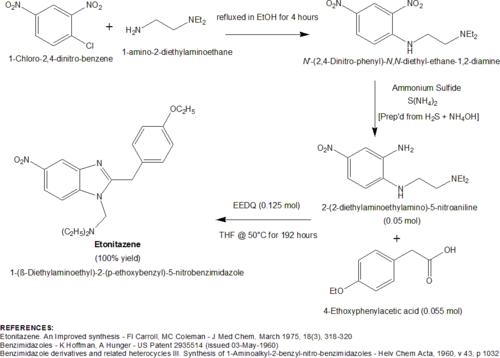
Die vielseitigste vom Schweizer Team entwickelte Synthese umfasste zunächst die Alkylierung von 2,4-Dinitrochlorbenzol mit 1-Amino-2-diethylaminoethan zu N-(β-Diethylaminoethyl)-2,4-dinitroanilin [aka: N'-(2, 4-Dinitrophenyl)-N,N-diethyl-ethan-1,2-diamin]. Das 2-Nitro - Substituenten o n die 2,4-Dinitroanilin - Verbindung wird dann selektiv reduziert , um die entsprechende primäre Amin durch Verwendung von Ammoniumsulfid als Reduktionsmittel . Das Ammoniumsulfid kann in situ durch Zugabe von konzentriertem wässrigem Ammoniumhydroxid gebildet werden, gefolgt von einer Sättigung der Lösung mit Schwefelwasserstoffgas . Das Zwischenprodukt durch die selektive Reduktion der 2-Nitro - Substituenten gebildet, 2- (β-Diethylaminoethylamino) -5- nitroanilin , wird dann mit dem umgesetzten Hydrochlorid - Salz des imino ethyl ethers von 4-ethoxy phenylacetonitril p-Ethoxybenzyl Cyanid: (auch bekannt als ). Der Iminoether, 2- (4-Ethoxyphenyl) -acetimidic acid ethyl ester - Hydrochlorid wird hergestellt , indem das 4-substituierte Lösen von Benzylcyanid in einem Gemisch aus wasserfreiem Ethanol und Chloroform , und dann diese Lösung mit trockenem Sättigen Chlorwasserstoff Gas. Die Reaktion zwischen dem 2-(β-Dialkylaminoalkylamin)-5-nitroanilin und dem HCl-Salz des Iminoethylethers führt zur Bildung von Etonitazen. Dieses Verfahren ist besonders nützlich bei der Herstellung der 4-, 5-, 6- und 7-Nitrobenzimidazole. Eine Variation der Wahl des substituierten Phenylessigsäureiminoethers liefert Verbindungen mit einer Vielzahl von Substituenten am Benzolring in 2-Position. Ein Diagramm dieser speziellen Synthese, wie es auf die Herstellung von Etonitazen angewendet wird, ist unten gezeigt.
Eine besonders neuartige Synthese von Etonitazen mit hoher Ausbeute wurde Mitte der 1970er Jahre von FI Carroll und MC Coleman entwickelt. Die Autoren wurden mit der Herstellung großer Mengen von Etonitazen beauftragt, fanden die konventionelle Synthese jedoch nicht ausreichend. Das Problem bei der herkömmlichen Synthese war die Labilität des Iminoetherreaktanten 2-(4-Ethoxyphenyl)acetimidsäureethylester (hergestellt durch Umsetzung von 4-Ethoxyphenylacetonitril mit ethanolischer HCl). Der Iminoether erforderte die Verwendung wasserfreier Reaktionsbedingungen und war in großen Mengen unbequem herzustellen. Dies führte die Autoren dazu, mit der Verwendung eines Kupplungsreagens, EEDQ (N-Ethoxycarbonyl-2-ethoxy-1,2-dihydrochinolin), zu experimentieren , um die Kondensation von 2- (2-Diethylaminoethylamino) -5-nitroanilin mit zu fördern 4-Ethoxyphenylessigsäure. Unglaublicherweise entdeckten die Autoren, dass, wenn diese Kondensation in Gegenwart von 2 oder mehr Moläquivalenten EEDQ (portionsweise in 3 Schritten zugegeben) in THF bei 50 °C für 192 Stunden (8 Tage) durchgeführt wurde, eine nahezu quantitative Ausbeute (100% ) von Etonitazen erhalten. Zusätzlich zu der beeindruckenden Verbesserung der Ausbeute gegenüber dem herkömmlichen Verfahren wurde das Aufarbeitungsverfahren stark vereinfacht, da Chinolin , Kohlendioxid und Ethanol die einzigen gebildeten Nebenprodukte waren. Ein Diagramm dieses Verfahrens ist unten gezeigt.
Eine Veröffentlichung aus dem Jahr 2011 [J. Org. Chem., 2011, 76 (23), 9577-9583] von einem südkoreanischen Team skizzierten eine neuartige Eintopfsynthese für substituierte und unsubstituierte 2-Benzylbenzimidazole, die leicht an die Herstellung von Etonitazen angepasst werden kann. Die Dreikomponentensynthese der direkten Etonitazen-Vorstufe, 2-(4-Ethoxybenzyl)-5-nitro-1H-benzoimidazol, besteht aus einem 2-Brom- oder 2-Iod-5-nitro-phenylamin (1,0 Moläquivalent), a 4-substituierter Benzaldehyd (1,2 Äquiv.) und Natriumazid (2 Äquiv.). Das 2-Halo-5-nitro-phenylamin benötigt für eine optimale Aktivität eine Brom- oder Jodgruppe. 2-Chlor-phenylamine sind völlig unreaktiv. Zusätzlich zu diesen drei Komponenten wurde die Reaktion in Gegenwart von 0,05 Moläquivalenten (5 Mol-%) eines Katalysators, Kupfer(I)-chlorid, und 5 Mol-% eines Liganden, TMEDA ( Tetramethylethylendiamin ) optimiert . Nach 12-stündigem Erhitzen dieser Komponenten auf 120ºC in DMSO wurde der direkte Etonitazen-Vorläufer, 2-(4-Ethoxybenzyl)-5-nitro-1H-benzoimidazol, in einer Ausbeute von etwa 80-90% gebildet. Der sekundäre Aminstickstoff von 2-(4-Ethoxybenzyl)-5-nitro-1H-benzoimidazol wurde dann mit (2-Chlorethyl)diethylamin alkyliert, um Etonitazen zu bilden. Ein Diagramm dieser Synthese ist unten gezeigt.
Siehe auch
- Etazen (Desnitroetonitazen)