Fluoren - Fluorene
|
|

|
|

|
|
| Namen | |
|---|---|
|
Bevorzugter IUPAC-Name
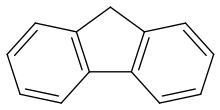
9 H -Fluoren |
|
|
Systematischer IUPAC-Name
Tricyclo[7.4.0.0 2,7 ]trideca-2,4,6,9,11,13-hexaen |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA-InfoCard |
100.001.541 |
| EG-Nummer | |
| KEGG | |
|
PubChem- CID
|
|
| RTECS-Nummer | |
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| C 13 H 10 | |
| Molmasse | 166,223 g·mol −1 |
| Dichte | 1.202 g/ml |
| Schmelzpunkt | 116 bis 117 °C (241 bis 243 °F; 389 bis 390 K) |
| Siedepunkt | 295 °C (563 °F; 568 K) |
| 1,992 mg/l | |
| Löslichkeit | organische Lösungsmittel |
| log P | 4.18 |
| Säure (p K a ) | 22.6 |
| -110,5·10 -6 cm 3 /mol | |
| Gefahren | |
| Sicherheitsdatenblatt | Sigma-Aldrich |
| NFPA 704 (Feuerdiamant) | |
| Flammpunkt | 152 °C (306 °F; 425 K) |
| Letale Dosis oder Konzentration (LD, LC): | |
|
LD 50 ( mediane Dosis )
|
16000 mg/kg (oral, Ratte) |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
Fluoren / f l ʊər í n / oder 9 H -fluoren ist eine organische Verbindung mit der Formel (C 6 H 4 ) 2 CH 2 . Es bildet weiße Kristalle, die einen charakteristischen, aromatischen Geruch aufweisen, der dem von Naphthalin ähnelt . Es hat eine violette Fluoreszenz , daher der Name. Für kommerzielle Zwecke wird es aus Steinkohlenteer gewonnen . Es ist in Wasser unlöslich und in vielen organischen Lösungsmitteln löslich. Obwohl manchmal als polyzyklischer aromatischer Kohlenwasserstoff klassifiziert , hat der fünfgliedrige Ring keine aromatischen Eigenschaften. Fluoren ist leicht sauer.
Synthese, Struktur und Reaktivität
Fluoren wird zwar aus Steinkohlenteer gewonnen, kann aber auch durch Dehydrierung von Diphenylmethan hergestellt werden . Alternativ kann es durch die Reduktion von Fluorenon mit Zink hergestellt werden . Das Fluorenmolekül ist nahezu planar, obwohl jeder der beiden Benzolringe mit dem zentralen Kohlenstoff 9 koplanar ist.
Säure
Die C9-H - Stellen des Fluorenrings sind schwach sauer ( pK a = 22,6 in DMSO .) Die Deprotonierung ergibt die stabilen fluorenyl Anion, nominell C 13 H 9 - , welches aromatisch und hat eine intensive orange Farbe. Das Anion ist ein Nukleophil . Elektrophile reagieren damit, indem sie an der 9-Position addieren. Die Reinigung von Fluoren nutzt seinen Säuregehalt und die geringe Löslichkeit seines Natriumderivats in Kohlenwasserstofflösungsmitteln.
Beide Protonen können von C9 entfernt werden. Zum Beispiel kann 9,9-Fluorenyldikalium durch Behandeln von Fluoren mit Kaliummetall in siedendem Dioxan erhalten werden .
Ligandeneigenschaften
Fluoren und seine Derivate können deprotoniert werden, um Liganden zu ergeben , die Cyclopentadienid ähnlich sind .

Verwendet
Fluoren ist ein Vorläufer anderer Fluorenverbindungen; die Elternart hat wenige Anwendungen. Fluoren-9-carbonsäure ist eine Vorstufe von Arzneimitteln. Die Oxidation von Fluoren ergibt Fluorenon , das nitriert wird, um kommerziell nützliche Derivate zu ergeben. 9-Fluorenylmethylchlorformiat (Fmoc Chlorid) wird verwendet , um den 9-Fluorenylmethyl carbamat (Fmoc) einzuführen Schutzgruppe von Aminen in der Peptidsynthese .
Polyfluoren- Polymere (bei denen Kohlenstoff 7 einer Einheit mit Kohlenstoff 2 der nächsten verknüpft ist, wodurch zwei Wasserstoffe verdrängt werden) sind elektrisch leitfähig und elektrolumineszierend und wurden als Luminophor in organischen Leuchtdioden viel untersucht .
Fluorenfarbstoffe
Fluorenfarbstoffe sind gut entwickelt. Die meisten werden durch Kondensation der aktiven Methylengruppe mit Carbonylen hergestellt. 2-Aminofluoren, 3,6-Bis-(dimethylamino)fluoren und 2,7-Diiodfluoren sind Vorläufer von Farbstoffen.
Siehe auch
Verweise
Externe Links
- Fluoren in der Datenbank des National Institute of Standards and Technology.

