Kaliumferricyanid - Potassium ferricyanide
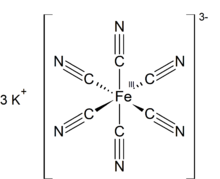
|
|

|
|
| Namen | |
|---|---|
|
IUPAC-Name
Kaliumhexacyanoferrat(III)
|
|
| Andere Namen
Rotes Preußen von Kali,
Preußisches Rot, Kaliumferricyanid |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA-InfoCard |
100.033.916 |
| EG-Nummer | |
| 21683 | |
|
PubChem- CID
|
|
| RTECS-Nummer | |
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| K 3 [Fe(CN) 6 ] | |
| Molmasse | 329,24 g/mol |
| Aussehen | tiefrote Kristalle, manchmal kleine Pellets, orange bis dunkelrotes Pulver |
| Dichte | 1,89 g/cm 3 , fest |
| Schmelzpunkt | 300 °C (572 °F; 573 K) |
| Siedepunkt | zersetzt |
| 330 g/L („Kaltwasser“) 464 g/L (20 °C) 775 g/L („Heißwasser“) |
|
| Löslichkeit | leicht löslich in Alkohol löslich in Säure löslich in Wasser |
| +2290,0·10 -6 cm 3 /mol | |
| Struktur | |
| monoklin | |
| oktaedrisch bei Fe | |
| Gefahren | |
| Sicherheitsdatenblatt | Sicherheitsdatenblatt |
| GHS-Piktogramme |

|
| GHS-Signalwort | Warnung |
| H302 , H315 , H319 , H332 , H335 | |
| P261 , P264 , P270 , P271 , P280 , P301+312 , P302+352 , P304+312 , P304+340 , P305+351+338 , P312 , P321 , P330 , P332+313 , P337+313 , P362 . , P403+ 233 , P405 , P501 | |
| NFPA 704 (Feuerdiamant) | |
| Flammpunkt | Nicht brennbar |
| Letale Dosis oder Konzentration (LD, LC): | |
|
LD 50 ( mediane Dosis )
|
2970 mg/kg (Maus, oral) |
| Verwandte Verbindungen | |
|
Andere Anionen
|
Kaliumferrocyanid |
|
Andere Kationen
|
Preußischblau |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
Kaliumferricyanid ist die chemische Verbindung mit der Formel K 3 [Fe(CN) 6 ]. Dieses leuchtend rote Salz enthält das oktaedrisch koordinierte [Fe(CN) 6 ] 3− -Ion. Es ist wasserlöslich und seine Lösung zeigt eine etwas grün-gelbe Fluoreszenz . Es wurde 1822 von Leopold Gmelin entdeckt.
Vorbereitung
Kaliumferrocyanid wird hergestellt, indem Chlor durch eine Lösung von Kaliumferrocyanid geleitet wird . Kaliumferricyanid trennt sich aus der Lösung:
- 2 K 4 [Fe(CN) 6 ] + Cl 2 → 2 K 3 [Fe(CN) 6 ] + 2 KCl
Struktur
Wie andere Metallcyanide hat festes Kaliumferricyanid eine komplizierte Polymerstruktur. Das Polymer besteht aus oktaedrischen [Fe(CN) 6 ] 3− -Zentren, die mit K + -Ionen vernetzt sind, die an die CN- Liganden gebunden sind . Die K + ---NCFe-Bindungen brechen, wenn der Feststoff in Wasser gelöst wird.
Anwendungen
Die Verbindung wird auch verwendet verhärten Eisen und Stahl , in Galvanotechnik , Färben Wolle , als Labor - Reagens , und als ein mildes Oxidationsmittel in der organischen Chemie .
Blaupausen und Fotografie
Die Verbindung hat weit verbreitete Verwendung in der Blaupausenzeichnung und in der Fotografie ( Cyanotypie- Verfahren). Mehrere Tonungsverfahren für fotografische Drucke beinhalten die Verwendung von Kaliumferricyanid.
Kaliumferricyanid wurde als Oxidationsmittel verwendet , um Silber während der Verarbeitung von Farbnegativen und -positiven zu entfernen , ein Prozess, der als Bleichen bezeichnet wird. Da Kaliumferricyanid-Bleichmittel umweltschädlich und kurzlebig sind und bei Mischung mit hohen Säurekonzentrationen und -volumina Blausäure freisetzen können, werden Bleichmittel mit Eisen- EDTA seit der Einführung des Kodak C-41-Prozesses im Jahr 1972 in der Farbverarbeitung eingesetzt . In der Farblithographie wird Kaliumferricyanid verwendet, um die Größe von Farbpunkten zu reduzieren, ohne ihre Anzahl zu verringern, als eine Art manuelle Farbkorrektur, die als Punktätzung bezeichnet wird. Es wird auch in der Schwarzweißfotografie mit Natriumthiosulfat (Hypo) verwendet, um die Dichte eines Negativs oder Gelatinesilberabzugs zu verringern, wobei die Mischung als Farmer's Reducer bekannt ist; Dies kann helfen, Probleme durch Überbelichtung des Negativs auszugleichen oder die Glanzlichter im Druck aufzuhellen.
Reagenz in der organischen Synthese
Kaliumferricyanid wird als Oxidationsmittel in der organischen Chemie verwendet. Es ist ein Oxidationsmittel für die Katalysatorregeneration bei Sharpless-Dihydroxylierungen .
Sensoren und Anzeigen
Kaliumferricyanid ist auch eine von zwei Verbindungen in Ferroxyl-Indikatorlösung (zusammen mit Phenolphthalein ), die in Gegenwart von Fe 2+ -Ionen blau ( Preußischblau ) werden und daher verwendet werden können, um Metalloxidation zu erkennen, die zu Rost führt. Aufgrund der sehr intensiven Farbe von Preußischblau ist es möglich, die Molzahl von Fe 2+ -Ionen mit einem Kolorimeter zu berechnen .
In physiologischen Experimenten bietet Kaliumferricyanid ein Mittel zur Erhöhung des Redoxpotentials einer Lösung (E°' ~ 436 mV bei pH 7). Als solches kann es reduziertes Cytochrom c (E°' ~ 247 mV bei pH 7) in isolierten Mitochondrien oxidieren. Als reduzierende Chemikalie wird in solchen Experimenten üblicherweise Natriumdithionit verwendet (E°' ~ -420 mV bei pH 7).
Kaliumferricyanid wird verwendet, um das Eisen(III)-Reduktionspotential einer Probe (Extrakt, chemische Verbindung usw.) zu bestimmen. Eine solche Messung wird verwendet, um die antioxidative Eigenschaft einer Probe zu bestimmen .
Kaliumferricyanid ist ein Bestandteil von amperometrischen Biosensoren als ein Elektronenübertragungsmittel , das das natürliche Elektronenübertragungsmittel eines Enzyms wie Sauerstoff wie beim Enzym Glukoseoxidase ersetzt . Es ist Bestandteil von handelsüblichen Blutzuckermessgeräten für Diabetiker .
Andere
Kaliumferricyanid wird mit Kaliumhydroxid (oder Natriumhydroxid als Ersatz) und Wasser kombiniert, um Murakamis Ätzmittel zu formulieren. Dieses Ätzmittel wird von Metallographen verwendet, um einen Kontrast zwischen Binder- und Karbidphasen in Sinterkarbiden herzustellen.
Preußischblau
Preußischblau , das tiefblaue Pigment im Blaudruck, entsteht durch die Reaktion von K 3 [Fe(CN) 6 ] mit Eisen(Fe 2+ )-Ionen sowie K 4 [Fe(CN) 6 ] mit Eisen ( III)-Salzen.
In der Histologie wird Kaliumferricyanid verwendet, um Eisen(II) in biologischem Gewebe nachzuweisen. Kaliumferricyanid reagiert mit Eisen(II) in saurer Lösung, um das unlösliche blaue Pigment zu erzeugen, das allgemein als Turnbull-Blau oder Preußisch-Blau bezeichnet wird . Um Eisen(III )-Eisen (Fe 3+ ) nachzuweisen , wird stattdessen Kaliumferrocyanid in der Preußisch-Blau- Färbemethode von Perls verwendet. Das bei der Turnbull-Blau-Reaktion gebildete Material und die bei der Preußisch-Blau-Reaktion gebildete Verbindung sind gleich.
Sicherheit
Kaliumferricyanid hat eine geringe Toxizität, seine Hauptgefahr besteht darin, dass es die Augen und die Haut leicht reizt. Unter sehr stark sauren Bedingungen entsteht jedoch hochgiftiges Blausäuregas nach der Gleichung:
- 6 H + + [Fe(CN) 6 ] 3− → 6 HCN + Fe 3+

