Primitive Streak - Primitive streak
| Primitive Streak | |
|---|---|
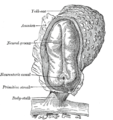
 Oberflächenansicht des Embryos eines Kaninchens .
arg. Embryonale Scheibe . pr. Primitiver Streifen. | |
| Einzelheiten | |
| Carnegie-Phase | 6b |
| Tage | fünfzehn |
| Bezeichner | |
| Latein | linea primitiv |
| Gittergewebe | D054240 |
| Anatomische Terminologie | |
Der Primitivstreifen ist eine Struktur, die sich in den frühen Stadien der Embryonalentwicklung von Vögeln , Reptilien und Säugetieren in der Blastula bildet . Es bildet sich auf der dorsalen (hinteren) Seite des sich entwickelnden Embryos zum kaudalen oder hinteren Ende hin.
Das Vorhandensein des Primitivstreifens wird eine bilaterale Symmetrie herstellen , den Ort der Gastrulation bestimmen und die Keimschichtbildung initiieren . Um den Streak zu bilden, ordnen Reptilien, Vögel und Säugetiere mesenchymale Zellen entlang der voraussichtlichen Mittellinie an, wodurch die zweite embryonale Achse sowie der Ort festgelegt werden, an dem Zellen während des Prozesses der Gastrulation und Keimschichtbildung eindringen und wandern. Der Primitivstreifen erstreckt sich durch diese Mittellinie und erzeugt die linke-rechte und kraniale-kaudale Körperachse und markiert den Beginn der Gastrulation. Dieser Prozess beinhaltet das Eindringen von Mesoderm- Vorläufern und ihre Wanderung zu ihrer endgültigen Position, wo sie sich in die Mesoderm-Keimschicht differenzieren, die zusammen mit den Endoderm- und Ektoderm-Keimschichten alle Gewebe des erwachsenen Organismus hervorbringt.
Komponenten
Da der Hühnerembryo leicht manipuliert werden kann, stammen die meisten unserer Kenntnisse über den Primitivstreifen aus Vogelstudien. Die Randzone eines Hühnerembryos enthält Zellen , die zum Streak beitragen. Dieser Bereich hat einen definierten Gradienten von vorne nach hinten in seiner Fähigkeit, den Primitivstreifen zu induzieren, wobei das hintere Ende das höchste Potential hat.
Der Epiblast , eine einzelne epitheliale Blastodiskus , ist die Quelle des gesamten embryonalen Materials in Amnioten und einige seiner Zellen werden den Primitivstreifen hervorbringen. Alle Zellen im Epiblast können auf Signale aus der Randzone reagieren, aber sobald eine bestimmte Region durch diese Signale induziert wird und eine Streifenbildung durchläuft, reagieren die verbleibenden Zellen im Epiblast nicht mehr auf diese induktiven Signale und verhindern die Bildung eines weiteren Streifens .
Dem Epiblast liegt der Hypoblast zugrunde , aus dem das extraembryonale Gewebe stammt. Beim Küken führt das Fehlen des Hypoblasten zu multiplen Streaks, was darauf hindeutet, dass seine Anwesenheit für die Regulierung der Bildung eines einzelnen Primitiv Streaks wichtig ist. Bei Mäusen wird diese Struktur als anteriores viszerales Endoderm (AVE) bezeichnet.
Zelluläre Bewegungen
Die Bildung des Primitivstreifens in der Blastozyste beinhaltet die koordinierte Bewegung und Neuanordnung von Zellen im Epiblast. Noch bevor der Streifen sichtbar ist, haben Epiblastzellen begonnen, sich zu bewegen. Am hinteren Ende, wo sich der Streifen bildet, treffen sich zwei gegenläufige Zellströme. Im Zentrum dieser Strömungen gibt es wenig Bewegung, während die größte Bewegung an der Peripherie der Wirbel beobachtet wird. Die Polonaise-Bewegung ist der Schlüssel zur Bildung des Primitivstreifens. Zellen, die die Koller-Sichel im hinteren Ende des Hühnerembryos überlagern, bewegen sich in Richtung der Mittellinie, treffen sich und ändern ihre Richtung zum Zentrum des Epiblasten. Zellen aus der lateralen posterioren Randzone ersetzen die Zellen, die die Koller-Sichel verlassen haben, indem sie sich im Zentrum dieser Region treffen, die Richtung ändern und sich nach vorne erstrecken. Während sich diese Zellen bewegen und sich am hinteren Ende des Embryos konzentrieren, durchläuft der Streifen einen ein- zu mehrschichtigen Übergang der Epithelschicht, der ihn zu einer makroskopisch sichtbaren Struktur macht. Mehrere Mechanismen, einschließlich orientierter Zellteilung , Zell-Zell- Interkalation und chemotaktischer Zellbewegung, wurden vorgeschlagen, um die Natur der Zellbewegungen zu erklären, die zur Bildung des Primitivstreifens erforderlich sind.
Formation
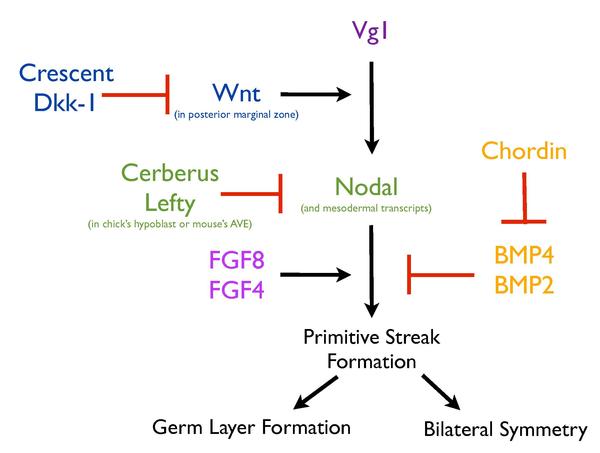
Die Bildung des Primitiv Streaks beruht auf einem komplexen Netzwerk von Signalwegen , die zusammenarbeiten, um sicherzustellen, dass dieser Prozess stark reguliert wird. Für diesen Prozess ist die Aktivierung verschiedener sezernierter Faktoren (Vg1, Nodal , Wnt8C , FGF8 und Chordin ) und Transkriptionsfaktoren ( Brachyury und Goosecoid ) neben der Stelle der Streifenbildung erforderlich. Darüber hinaus spielen auch Strukturen wie der Hypoblast eine wichtige Rolle bei der Regulation der Streak-Bildung. Die Entfernung des Hypoblasten im Küken führt zu korrekt gemusterten ektopischen Streifen, was darauf hindeutet, dass der Hypoblast dazu dient, die Bildung des Primitivstreifens zu hemmen.
Vg1- und Wnt-Signalisierung
In ähnlicher Weise können Vg1 (ein Mitglied der TGFB- Familie) Fehlexpression und Transplantate der hinteren Randzone bei Küken ebenfalls ektopische Streifen induzieren, jedoch nur innerhalb der Randzone des Embryos, was auf eine spezifische Eigenschaft dieser Region in ihrer Fähigkeit hindeutet, die Streifenbildung zu induzieren. Mehrere Beweislinien weisen auf die Wnt-Expression als Determinante dieser Fähigkeit hin. Die Deletion von Wnt3 in Mausembryonen führt zum Fehlen einer Streifenbildung, ähnlich dem Phänotyp von B-Catenin- Mutantenembryonen. Darüber hinaus führt die Mutation des intrazellulären negativen Regulators der Wnt-Signalgebung, Axin , und die Fehlexpression des Hühner-cWnt8C zu multiplen Streaks in Mausembryonen. Die Lokalisierung von Wnt und Komponenten seines Stoffwechselwegs, Lef1 und B-Catenin, unterstützt weiter die streifeninduzierende Rolle in der Randzone. Darüber hinaus wird es als ein von posterior nach anterior abnehmender Gradient ausgedrückt, der der Fähigkeit der Randzone zur Streak-Induktion entspricht. Die Fehlexpression von Vg1 oder Wnt1 allein konnte beim Küken keinen ektopischen Streifen induzieren, aber zusammen führte ihre Fehlexpression zur Bildung von ektopen Streifen, was bestätigt, dass die Fähigkeit der hinteren Randzone zur Auslösung von Streifen auf die Wnt-Signalgebung zurückgeführt werden kann und dass Vg1 und Wnt kooperieren, um diesen Prozess einzuleiten. Eine Fehlexpression von Vg1 zusammen mit Wnt-Antagonisten, Crescent oder Dkk-1 , verhindert die Bildung von ektopischen Streifen, was die Bedeutung der Wnt-Aktivität bei der Bildung von Vg1-induzierten ektopen Streifen und daher ihre Implikation bei der normalen primitiven Streifenbildung zeigt.
Hypoblast
Jeder gegebene Schnitt aus dem Blastoderm ist in der Lage, bis zum Zeitpunkt der Gastrulation und Primitivstreifenbildung eine komplette Achse zu erzeugen. Diese Fähigkeit, aus dem Hühnerembryo im Prä-Streak-Stadium einen Streak zu erzeugen, weist darauf hin, dass es einen Mechanismus geben muss, um sicherzustellen, dass sich nur ein einzelner Streak bildet. Die Zellmasse, Hypoblast , sondert einen Antagonisten von Nodal ab, der die Bildung von ektopischen Streifen beim Küken verhindert.
Knotensignalisierung
Nodal , ein bekannter mesodermaler Induktor der TGFB-Superfamilie, wurde mit der Streak-Bildung in Verbindung gebracht. Für Nodal mutierte Mausembryonen versagen bei der Gastrulation und ihnen fehlt das meiste Mesoderm, aber Nodal spielt nicht nur eine Rolle bei der Mesoderm-Induktion, sondern reguliert auch die Induktion und/oder Aufrechterhaltung des Primitivstreifens. In Gegenwart von Hypoblasten kann Nodal im Hühnerembryo keine ektopischen Streifen induzieren, während seine Entfernung die Expression von Nodal, Chordin und Brachyury induziert, was darauf hindeutet, dass der Hypoblast eine gewisse hemmende Wirkung auf die Nodal-Signalgebung haben muss. Tatsächlich hemmt der multifunktionale Antagonist der Nodal-, Wnt- und BMP-Signalgebung, Cerberus (im Hypoblast produziert) und Cerberus-Short (der nur Nodal hemmt) durch seine Wirkung auf die Nodal-Signalgebung die Streifenbildung. Schließlich wird der Hypoblast durch den sich bewegenden Endoblast nach anterior verdrängt, was die Streifenbildung am hinteren Ende ermöglicht. Am vorderen Ende hemmen die Anwesenheit des Hypoblasten und der von ihm sezernierten Antagonisten, wie Cerberus, die Expression von Nodal und beschränken somit die Streifenbildung nur auf das hintere Ende. Ähnlich wie der Hypoblast in Küken sezerniert der AVE in der Maus zwei Antagonisten der Nodal-Signalgebung, Cerberus-like, Cerl und Lefty1 . Bei der Maus Cer-/-; Lefty1-/- Doppelmutanten entwickeln multiple Streaks, wie durch die ektopische Expression von Brachyury angezeigt und können teilweise durch die Entfernung einer Kopie des Nodal-Gens gerettet werden. In der Maus schränkt AVE die Streifenbildung durch die redundanten Funktionen von Cer1 und Lefty1 ein, die die Nodal-Signalgebung negativ regulieren. Die Rolle des AVE der Maus bei der Sicherstellung der Bildung eines einzelnen Primitivstreifens ist im Hypoblasten des Kükens evolutionär konserviert.
FGF-Signalisierung
Ein weiterer wichtiger Weg bei der Modulation der Bildung des Primitivstreifens ist FGF , von dem angenommen wird, dass es mit Nodal zusammenarbeitet, um diesen Prozess zu regulieren. Die Hemmung der FGF-Signalgebung durch die Expression eines dominant negativen Rezeptors unter Verwendung eines FGF-Rezeptor-Inhibitors (SU5402) oder die Verarmung von FGF-Liganden hemmt die Mesodermbildung und dies wiederum hemmt die Streifenbildung. Darüber hinaus erforderte die durch Vg1 induzierte ektopische Streak-Bildung eine FGF-Signalgebung.
BMP-Signalisierung
Schließlich ist die BMP- Signalgebung auch wichtig für die Regulierung des Prozesses der Streifenbildung im Hühnerembryo. Der Ort der Streifenbildung ist durch niedrige BMP-Signale gekennzeichnet, während der Rest des Epiblasts eine hohe BMP-Aktivierung aufweist. Darüber hinaus verhindert die Fehlexpression von entweder BMP4 oder BMP7 die Streifenbildung, während der BMP-Inhibitor Chordin die Bildung von ektopischen Streifen beim Küken induziert, was darauf hindeutet, dass die Streifenbildung wahrscheinlich eine BMP-Hemmung erfordert.
Ethische Implikationen
Der Primitiv Streak ist ein wichtiges Konzept in der Bioethik , wo einige Experten argumentieren, dass Experimente mit menschlichen Embryonen erlaubt sind, jedoch nur bevor sich der Primitiv Streak entwickelt, im Allgemeinen um den vierzehnten Tag der Existenz. Die Entwicklung des Primitivstreifens wird von solchen Bioethikern als Zeichen für die Erschaffung eines einzigartigen menschlichen Wesens verstanden. In einigen Ländern ist es illegal, einen menschlichen Embryo länger als 14 Tage außerhalb des Körpers einer Frau zu entwickeln.
Zusätzliche Bilder
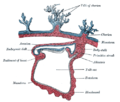
Lateraler Schnitt durch die Säugetier- Blastodisc .