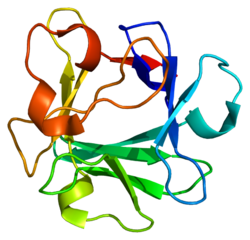
Basischer Fibroblasten-Wachstumsfaktor - Basic fibroblast growth factor
FGF2 , auch bekannt als basischer Fibroblasten-Wachstumsfaktor ( bFGF ) und FGF-β , ist ein Wachstumsfaktor und Signalprotein, das vom FGF2- Gen kodiert wird . Es bindet an spezifische Fibroblasten-Wachstumsfaktor-Rezeptor- (FGFR)-Proteine , die selbst eine Familie eng verwandter Moleküle sind , und übt Wirkungen aus . Das Fibroblasten-Wachstumsfaktor- Protein wurde erstmals 1975 gereinigt; kurz darauf wurden drei Varianten isoliert: „basischer FGF“ (FGF2); Heparin-bindender Wachstumsfaktor-2; und Endothelzellwachstumsfaktor-2. Die Gensequenzierung ergab, dass diese Gruppe das gleiche FGF2-Protein ist und ein Mitglied einer Familie von FGF- Proteinen ist.
Funktion
Wie andere Mitglieder der FGF-Familie besitzt der basische Fibroblasten-Wachstumsfaktor breite mitogene und Zellüberlebensaktivitäten und ist an einer Vielzahl von biologischen Prozessen beteiligt, einschließlich der embryonalen Entwicklung , des Zellwachstums , der Morphogenese , der Gewebereparatur , des Tumorwachstums und der Invasion.
In normalem Gewebe ist bFGF in Basalmembranen und in der subendothelialen extrazellulären Matrix von Blutgefäßen vorhanden . Es bleibt membrangebunden, solange kein Signalpeptid vorhanden ist .
Es wurde die Hypothese aufgestellt, dass sowohl während der Wundheilung von normalem Gewebe als auch der Tumorentwicklung die Wirkung von Heparansulfat- abbauenden Enzymen bFGF aktiviert, wodurch die Bildung neuer Blutgefäße vermittelt wird , ein Prozess, der als Angiogenese bekannt ist .
Darüber hinaus wird es von menschlichen Adipozyten synthetisiert und sezerniert und die Konzentration von FGF2 korreliert mit dem BMI in Blutproben. Es wurde auch gezeigt, dass es auf Präosteoblasten – in Form einer erhöhten Proliferation – wirkt, nachdem es an den Fibroblasten-Wachstumsfaktor-Rezeptor 1 gebunden und die Phosphoinositid-3-Kinase aktiviert hat .
In vorläufigen Tierstudien wurde gezeigt, dass FGF2 das Herz vor Verletzungen im Zusammenhang mit einem Herzinfarkt schützt, das Absterben von Gewebe reduziert und eine verbesserte Funktion nach der Reperfusion fördert .
Jüngste Beweise haben gezeigt, dass niedrige FGF2-Spiegel eine Schlüsselrolle beim Auftreten von übermäßiger Angst spielen.
Darüber hinaus ist FGF2 eine kritische Komponente des Kulturmediums für humane embryonale Stammzellen ; Der Wachstumsfaktor ist notwendig, damit die Zellen in einem undifferenzierten Zustand verbleiben, obwohl die Mechanismen, durch die dies geschieht, schlecht definiert sind. Es wurde gezeigt , dass es die Gremlin - Expression induziert , von der wiederum bekannt ist , dass sie die Induktion der Differenzierung durch knochenmorphogenetische Proteine hemmt . Es ist in von Maus-Feeder-Zellen abhängigen Kultursystemen sowie in Feeder- und serumfreien Kultursystemen erforderlich. FGF2 fördert in Verbindung mit BMP4 die Differenzierung von Stammzellen zu mesodermalen Abstammungslinien. Nach der Differenzierung produzieren mit BMP4 und FGF2 behandelte Zellen im Allgemeinen höhere Mengen an osteogener und chondrogener Differenzierung als unbehandelte Stammzellen. Jedoch ist eine niedrige Konzentration von bFGF (10 ng / ml) kann eine hemmende Wirkung auf ausüben Osteoblastendifferenzierung . Die Kernform von FGF2 wirkt beim mRNA-Export
FGF2 wird hauptsächlich als Polypeptid mit 155 Aminosäuren synthetisiert, was zu einem Protein von 18 kDa führt. Es gibt jedoch vier alternative Startcodons, die N-terminale Verlängerungen von 41, 46, 55 oder 133 Aminosäuren bereitstellen, was zu Proteinen von 22 kDa (insgesamt 196 AA), 22,5 kDa (insgesamt 201 AA), 24 kDa (210 .) führt aa insgesamt) bzw. 34 kDa (288 aa insgesamt). Im Allgemeinen wird die 155 aa/18 kDa-Form mit niedrigem Molekulargewicht (LMW) als zytoplasmatisch betrachtet und kann von der Zelle sezerniert werden, während die Formen mit hohem Molekulargewicht (HMW) zum Zellkern geleitet werden.
Interaktionen
Es wurde gezeigt, dass basischer Fibroblasten-Wachstumsfaktor mit Caseinkinase 2, Alpha 1 , RPL6 , ribosomalem Protein S19 und API5 interagiert .
Siehe auch
- Angiogenese
- Angststörungen
- Zytokin
- Fibroblasten-Wachstumsfaktor
- Wachstumsfaktor
- Proteasen in der Angiogenese
- Rezeptor (Biochemie)
- Signaltransduktion
Verweise
Weiterlesen
- Ornitz DM, Itoh N (2001). "Fibroblasten-Wachstumsfaktoren" . Genombiologie . 2 (3): REVIEWS3005. doi : 10.1186/gb-2001-2-3reviews3005 . PMC 138918 . PMID 11276432 .
- Orpana A, Salven P (Februar 2002). „Angiogene und lymphangiogene Moleküle bei hämatologischen Malignomen“. Leukämie und Lymphom . 43 (2): 219–24. doi : 10.1080/10428190290005964 . PMID 11999550 . S2CID 21908151 .
- Marie PJ, Debiais F, Haÿ E (2003). „Regulierung des menschlichen kranialen Osteoblasten-Phänotyps durch FGF-2-, FGFR-2- und BMP-2-Signalgebung“. Histologie und Histopathologie . 17 (3): 877–85. doi : 10.14670/HH-17.877 . PMID 12168799 .
- Zhao XC, Zhang LM, Tong DY, An P, Jiang C, Zhao P, Chen WM, Wang J (März 2013). "Propofol erhöht die Expression des basischen Fibroblasten-Wachstumsfaktors nach vorübergehender zerebraler Ischämie bei Ratten" . Neurochemische Forschung . 38 (3): 530–7. doi : 10.1007/s11064-012-0945-4 . PMC 3574197 . PMID 23247820 .
- Vincent T, Saklatvala J (Juni 2006). "Basic Fibroblast Growth Factor: ein extrazellulärer Mechanotransducer im Gelenkknorpel?". Transaktionen der Biochemischen Gesellschaft . 34 (Teil 3): 456–7. doi : 10.1042/BST0340456 . PMID 16709186 .
- Ribatti D, Vacca A, Rusnati M, Presta M (2007). „Die Entdeckung des basischen Fibroblasten-Wachstumsfaktors/Fibroblasten-Wachstumsfaktor-2 und seine Rolle bei hämatologischen Malignomen“. Zytokin & Wachstumsfaktor Bewertungen . 18 (3–4): 327–34. doi : 10.1016/j.cytogfr.2007.04.011 . PMID 17537668 .
- Watson R, Anthony F, Pickett M, Lambden P, Masson GM, Thomas EJ (September 1992). "Reverse Transkription mit verschachtelter Polymerase-Kettenreaktion zeigt die Expression von basischen Fibroblasten-Wachstumsfaktor-Transkripten in menschlichen Granulosa- und Kumuluszellen von In-vitro-Fertilisationspatienten". Biochemische und biophysikalische Forschungskommunikation . 187 (3): 1227–31. doi : 10.1016/0006-291X(92)90434-M . PMID 1417798 .
- Zhu X, Komiya H, Chirino A, Faham S, Fox GM, Arakawa T, Hsu BT, Rees DC (Januar 1991). „Dreidimensionale Strukturen von sauren und basischen Fibroblasten-Wachstumsfaktoren“. Wissenschaft . 251 (4989): 90–3. doi : 10.1126/science.1702556 . PMID 1702556 .
- Eriksson AE, Cousens LS, Weaver LH, Matthews BW (April 1991). "Dreidimensionale Struktur des menschlichen basischen Fibroblasten-Wachstumsfaktors" . Proceedings of the National Academy of Sciences of the United States of America . 88 (8): 3441-5. doi : 10.1073/pnas.88.8.3441 . PMC 51463 . PMID 1707542 .
- H. Ago, Y. Kitagawa, A. Fujishima, Y. Matsuura, Y. Katsube (September 1991). „Kristallstruktur des grundlegenden Fibroblasten-Wachstumsfaktors bei einer Auflösung von 1,6 A“. Zeitschrift für Biochemie . 110 (3): 360–3. doi : 10.1093/oxfordjournals.jbchem.a123586 . PMID 1769963 .
- Zhang JD, Cousens LS, Barr PJ, Sprang SR (April 1991). "Dreidimensionale Struktur des menschlichen basischen Fibroblasten-Wachstumsfaktors, ein strukturelles Homolog von Interleukin 1 beta" . Proceedings of the National Academy of Sciences of the United States of America . 88 (8): 3446–50. doi : 10.1073/pnas.88.8.3446 . PMC 51464 . PMID 1849658 .
- Wu DQ, Kan MK, Sato GH, Okamoto T, Sato JD (September 1991). "Charakterisierung und molekulare Klonierung eines mutmaßlichen Bindungsproteins für Heparin-bindende Wachstumsfaktoren" . Die Zeitschrift für biologische Chemie . 266 (25): 16778–85. doi : 10.1016/S0021-9258(18)55368-0 . PMID 1885605 .
- Fukushima Y, Byers MG, Fiddes JC, Shows TB (1991). „Das humane basische Fibroblasten-Wachstumsfaktor-Gen (FGFB) wird dem Chromosom 4q25 zugeordnet“. Zytogenetik und Zellgenetik . 54 (3–4): 159–60. doi : 10.1159/000132983 . PMID 2265560 .
- Lafage-Pochitaloff M, Galland F, Simonetti J, Prats H, Mattei MG, Birnbaum D (1990). "Das humane basische Fibroblasten-Wachstumsfaktor-Gen befindet sich auf dem langen Arm von Chromosom 4 bei den Banden q26-q27". Onkogenforschung . 5 (3): 241–4. PMID 2320377 .
- Geschichte MT, Esch F, Shimasaki S, Sasse J, Jacobs SC, Lawson RK (Februar 1987). „Amino-terminale Sequenz einer großen Form von basischem Fibroblasten-Wachstumsfaktor, isoliert aus menschlichem gutartigem Prostata-Hyperplastik-Gewebe“. Biochemische und biophysikalische Forschungskommunikation . 142 (3): 702–9. doi : 10.1016/0006-291X(87)91471-9 . PMID 2435284 .
- Kurokawa T, Sasada R, Iwane M, Igarashi K (März 1987). „Klonierung und Expression von cDNA, die menschlichen basischen Fibroblasten-Wachstumsfaktor kodiert“. FEBS-Briefe . 213 (1): 189–94. doi : 10.1016/0014-5793(87)81489-8 . PMID 2435575 . S2CID 28111330 .
- Prats H, Kaghad M, Prats AC, Klagsbrun M, Lélias JM, Liauzun P, Chalon P, Tauber JP, Amalric F, Smith JA (März 1989). "Hochmolekulare Formen des basischen Fibroblasten-Wachstumsfaktors werden durch alternative CUG-Codons initiiert" . Proceedings of the National Academy of Sciences of the United States of America . 86 (6): 1836–40. doi : 10.1073/pnas.86.6.1836 . PMC 286.799 . PMID 2538817 .
- Florkiewicz RZ, Sommer A (Juni 1989). "Das Gen für den menschlichen basischen Fibroblasten-Wachstumsfaktor kodiert für vier Polypeptide: drei initiieren die Translation von Nicht-AUG-Codons" . Proceedings of the National Academy of Sciences of the United States of America . 86 (11): 3978–81. doi : 10.1073/pnas.86.11.3978 . PMC 287.371 . PMID 2726761 .
- Abraham JA, Whang JL, Tumolo A, Mergia A, Fiddes JC (1987). „Menschlicher grundlegender Fibroblasten-Wachstumsfaktor: Nukleotidsequenz, genomische Organisation und Expression in Säugetierzellen“. Cold Spring Harbor Symposien zur Quantitativen Biologie . 51 Teil 1: 657–68. doi : 10.1101/sqb.1986.051.01.078 . PMID 3472745 .
- Sommer A, Brewer MT, Thompson RC, Moscatelli D, Presta M, Rifkin DB (April 1987). „Eine Form des menschlichen basischen Fibroblasten-Wachstumsfaktors mit einem verlängerten Aminoterminus“. Biochemische und biophysikalische Forschungskommunikation . 144 (2): 543–50. doi : 10.1016/S0006-291X(87)80001-3 . PMID 3579930 .
Externe Links
- Basic+Fibroblast+Growth+Factor in der US National Library of Medicine Medical Subject Headings (MeSH)
- Standort des menschlichen FGF2- Genoms und Detailseite des FGF2- Gens im UCSC-Genom-Browser .