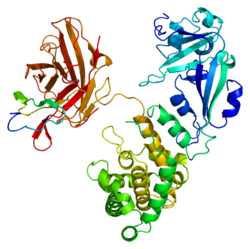
Heparin-bindender EGF-ähnlicher Wachstumsfaktor - Heparin-binding EGF-like growth factor
Der Heparin-bindende EGF-ähnliche Wachstumsfaktor ( HB-EGF ) ist ein Mitglied der EGF- Proteinfamilie, die beim Menschen vom HBEGF- Gen kodiert wird .
Der HB-EGF-ähnliche Wachstumsfaktor wird als membranverankertes mitogenes und chemotaktisches Glykoprotein synthetisiert . Ein epidermaler Wachstumsfaktor, der von Monozyten und Makrophagen aufgrund einer Affinität zu Heparin produziert wird, wird als HB-EGF bezeichnet. Es hat sich gezeigt, dass es eine Rolle bei der Wundheilung , der Herzhypertrophie und der Herzentwicklung und -funktion spielt. HB-EGF wurde erstmals im konditionierten Medium menschlicher Makrophagen-ähnlicher Zellen identifiziert und ist ein 87-Aminosäuren-Glykoprotein, das eine stark regulierte Genexpression zeigt. Die Abspaltung von Ektodomänen führt zur löslichen reifen Form von HB-EGF, die die Mitogenität und chemotaktische Faktoren für glatte Muskelzellen und Fibroblasten beeinflusst. Die transmembrane Form von HB-EGF ist der einzigartige Rezeptor für Diphtherietoxin und wirkt bei der juxtakrinen Signalübertragung in Zellen. Beide Formen von HB-EGF nehmen an normalen physiologischen Prozessen und an pathologischen Prozessen teil, einschließlich Tumorprogression und Metastasierung, Organhyperplasie und atherosklerotischer Erkrankung. HB-EGF kann an zwei Stellen auf Zelloberflächen binden: Heparansulfat-Proteoglykane und EGF-Rezeptor, die Zell-Zell-Interaktionen bewirken.
Interaktionen
Es wurde gezeigt, dass Heparin-bindender EGF-ähnlicher Wachstumsfaktor mit NRD1 , Zinkfinger und BTB-Domänen-enthaltendem Protein 16 und BAG1 interagiert .
Die biologischen Aktivitäten von HB-EGF mit diesen Genen beeinflussen die Zellzyklusprogression, die molekulare Chaperon-Regulierung, das Zellüberleben, die Zellfunktionen, die Adhäsion und die Vermittlung der Zellmigration. Das NRD1-Gen kodiert für das Protein Nardilysin, einen HB-EGF-Modulator. Zinkfinger und das BTB-Domänen-enthaltende Protein 16 und der molekulare Chaperon-Regulator der BAG-Familie fungieren als Co-Chaperon-Proteine in Prozessen, die HB-EGF beinhalten.
Rolle bei Krebs
Jüngste Studien weisen auf eine signifikante Erhöhung der HB-EGF-Genexpression bei einer Reihe von menschlichen Krebsarten sowie bei von Krebs abgeleiteten Zelllinien hin. Es gibt Hinweise darauf, dass HB-EGF eine bedeutende Rolle bei der Entwicklung von malignen Phänotypen spielt, die zum metastatischen und invasiven Verhalten von Tumoren beitragen. Die proliferativen und chemotaktischen Wirkungen von HB-EGF resultieren aus dem Zieleinfluss auf bestimmte Zellen, einschließlich Fibroblasten, Zellen der glatten Muskulatur und Keratinozyten. Für zahlreiche Zelltypen wie Brust- und Eierstocktumorzellen, menschliche Epithelzellen und Keratinozyten ist HB-EGF ein potentes Mitogen, das in solchen Proben zu einer nachgewiesenen Hochregulation von HB-EGF führt. Sowohl in-vivo- als auch in-vitro-Studien zur Tumorbildung in von Krebs abgeleiteten Zelllinien zeigen, dass die Expression von HB-EGF für die Tumorentwicklung essentiell ist. Als Ergebnis zeigen Studien, die den Einsatz von spezifischen HB-EGF-Inhibitoren und monoklonalen Antikörpern gegen HB-EGF implementieren , das Potenzial für die Entwicklung neuer Therapien zur Behandlung von Krebs durch gezielte HB-EGF-Expression.
Rolle in Herzentwicklung und Gefäßsystem
Die HB-EGF-Bindung und Aktivierung von EGF-Rezeptoren spielt eine entscheidende Rolle bei der Entwicklung von Herzklappengewebe und der Aufrechterhaltung einer normalen Herzfunktion bei Erwachsenen. Während der Entwicklung des Klappengewebes ist die Interaktion von HB-EGF mit EGF-Rezeptoren und Heparansulfat-Proteoglykanen für die Verhinderung von Fehlbildungen von Klappen aufgrund einer Vergrößerung von wesentlicher Bedeutung. Im Gefäßsystem zeigen Bereiche mit gestörtem Fluss eine Hochregulierung von HB-EGF mit Förderung von Gefäßläsionen, Atherogenese und Hyperplasie des Intimagewebes in Gefäßen. Die durch die HB-EGF-Expression bedingte Strömungsstörungsumbildung des Gefäßgewebes trägt zu Aortenklappenerkrankungen, peripheren Gefäßerkrankungen und Conduit-Stenosen bei.
Rolle bei der Wundheilung
HB-EGF ist der vorherrschende Wachstumsfaktor bei der Epithelisierung, die für die Wundheilung der Haut erforderlich ist. Die mitogenen und migratorischen Wirkungen von HB-EGF auf Keratinozyten und Fibroblasten fördern die dermale Reparatur und Angiogenese, die für die Wundheilung notwendig sind und ist ein Hauptbestandteil von Wundflüssigkeiten. HB-EGF zeigt während der frühen Stadien der Wundheilung eine Zielzellspezifität, die von Makrophagen, Monozyten und Keratinozyten freigesetzt wird. Die Bindung der HB-EGF-Zelloberfläche an Heparansulfat-Proteoglykane verbessert die mitogenfördernden Fähigkeiten, erhöht die Heilungsrate von Hautwunden, verkürzt die Heilungszeiten von menschlichen Hauttransplantaten und fördert die schnelle Heilung von Geschwüren, Verbrennungen und epidermalen Wunden mit Spaltdicke.
Rolle in anderen physiologischen Prozessen
HB-EGF wird als wichtiger Bestandteil für die Modulation der Zellaktivität in verschiedenen biologischen Interaktionen erkannt. Weit verbreitet in zerebralen Neuronen und Neuroglia gefunden, stimuliert HB-EGF, das durch Hirnhypoxie und/oder Ischämie induziert wird, anschließend die Neurogenese. Interaktionen zwischen Uterus-HB-EGF und epidermalen Wachstumsfaktorrezeptoren von Blastozysten beeinflussen die Embryo-Uterus-Interaktionen und die Implantation. Studien zeigen, dass HB-EGF Darmstammzellen und Darmepithelzellen bei nekrotisierender Enterokolitis , einer Krankheit, die Frühgeborene betrifft, schützt . In Verbindung mit einem Zusammenbruch der Darmbarrierefunktion kann nekrotisierende Enterokolitis durch HB-EGF-Wirkungen auf die Darmschleimhaut vermittelt werden. HB-EGF, das während der Skelettmuskelkontraktion exprimiert wird, erleichtert die periphere Glukoseentfernung, Glukosetoleranz und -aufnahme. Die Hochregulation von HB-EGF durch Bewegung könnte die molekulare Grundlage für die Abnahme von Stoffwechselstörungen wie Fettleibigkeit und Typ-2-Diabetes bei regelmäßiger Bewegung erklären .
Verweise
Weiterlesen
- Higashiyama S, Lau K, Besner GE et al. (1992). "Struktur des Heparin-bindenden EGF-ähnlichen Wachstumsfaktors. Mehrere Formen, Primärstruktur und Glykosylierung des reifen Proteins" . J. Biol. Chem . 267 (9): 6205–12. doi : 10.1016/S0021-9258(18)42682-8 . PMID 1556128 .
- Yoshizumi M., Kourembanas S., Temizer DH et al. (1992). "Tumornekrosefaktor erhöht die Transkription des Heparin-bindenden epidermalen Wachstumsfaktor-ähnlichen Wachstumsfaktor-Gens in vaskulären Endothelzellen" . J. Biol. Chem . 267 (14): 9467–9. doi : 10.1016/S0021-9258(19)50112-0 . PMID 1577791 .
- Higashiyama S, Abraham JA, Miller J, et al. (1991). „Ein Heparin-bindender Wachstumsfaktor, der von Makrophagen-ähnlichen Zellen sezerniert wird, der mit EGF verwandt ist“. Wissenschaft . 251 (4996): 936–9. Bibcode : 1991Sci...251..936H . doi : 10.1126/science.1840698 . PMID 1840698 . S2CID 23639487 .
- R. Iwamoto, H. Senoh, Y. Okada et al. (1991). „Ein Antikörper, der die Bindung von Diphtherietoxin an Zellen hemmt, zeigte die Assoziation eines 27-kDa-Membranproteins mit dem Diphtherietoxin-Rezeptor“ . J. Biol. Chem . 266 (30): 20463–9. doi : 10.1016/S0021-9258(18)54947-4 . PMID 1939101 .
- Hayes H, Kaneda Y, Uchida T, Okada Y (1988). „Regionale Zuordnung des Gens für Diphtherie-Toxin-Empfindlichkeit mit subchromosomalen Fragmenten in Mikrozellhybriden“. Chromosom . 96 (1): 26–32. doi : 10.1007/BF00285879 . PMID 3436221 . S2CID 35349033 .
- Bennett KL, Jackson DG, Simon JC et al. (1995). "CD44-Isoformen, die Exon V3 enthalten, sind für die Präsentation des Heparin-bindenden Wachstumsfaktors verantwortlich" . J. Cell Biol . 128 (4): 687–98. doi : 10.1083/jcb.128.4.687 . PMC 2199889 . PMID 7532176 .
- Pathak BG, Gilbert DJ, Harrison CA et al. (1995). "Chromosomenort der Maus von drei EGF-Rezeptorliganden: Amphiregulin (Areg), Betacellulin (Btc) und Heparin-bindender EGF (Hegfl)" . Genomik . 28 (1): 116–8. doi : 10.1006/geno.1995.1116 . PMID 7590736 .
- T. Mitamura, S. Higashiyama, N. Taniguchi et al. (1995). "Diphtherie-Toxin bindet an die epidermale Wachstumsfaktor (EGF)-ähnliche Domäne des menschlichen Heparin-bindenden EGF-ähnlichen Wachstumsfaktors/Diphtherietoxin-Rezeptors und hemmt spezifisch seine mitogene Aktivität" . J. Biol. Chem . 270 (3): 1015–9. doi : 10.1074/jbc.270.3.1015 . PMID 7836353 .
- K. Hashimoto, S. Higashiyama, H. Asada et al. (1994). "Heparin-bindender epidermaler Wachstumsfaktor-ähnlicher Wachstumsfaktor ist ein autokriner Wachstumsfaktor für menschliche Keratinozyten" . J. Biol. Chem . 269 (31): 20060–6. doi : 10.1016/S0021-9258(17)32127-0 . PMID 8051092 .
- Kobrin MS, Funatomi H, Friess H, et al. (1994). „Induktion und Expression von Heparin-bindendem EGF-ähnlichem Wachstumsfaktor bei menschlichem Bauchspeicheldrüsenkrebs“. Biochem. Biophys. Res. Komm . 202 (3): 1705–9. doi : 10.1006/bbrc.1994.2131 . PMID 8060360 .
- Maruyama K., Sugano S. (1994). „Oligo-Capping: eine einfache Methode, um die Cap-Struktur von eukaryotischen mRNAs durch Oligoribonukleotide zu ersetzen“. Gene . 138 (1–2): 171–4. doi : 10.1016/0378-1119(94)90802-8 . PMID 8125298 .
- Thompson SA, Higashiyama S, Wood K, et al. (1994). "Charakterisierung von Sequenzen innerhalb des Heparin-bindenden EGF-ähnlichen Wachstumsfaktors, die die Wechselwirkung mit Heparin vermitteln" . J. Biol. Chem . 269 (4): 2541-9. doi : 10.1016/S0021-9258(17)41979-X . PMID 8300582 .
- Fen Z, Dhadly MS, Yoshizumi M, et al. (1993). „Strukturelle Organisation und chromosomale Zuordnung des Gens, das den humanen Heparin-bindenden epidermalen Wachstumsfaktor-ähnlichen Wachstumsfaktor/Diphtherietoxin-Rezeptor codiert“. Biochemie . 32 (31): 7932–8. doi : 10.1021/bi00082a014 . PMID 8347598 .
- Elenius K., Paul S., Allison G. et al. (1997). „Die Aktivierung von HER4 durch Heparin-bindenden EGF-ähnlichen Wachstumsfaktor stimuliert die Chemotaxis, aber nicht die Proliferation“ . EMBO J . 16 (6): 1268–78. doi : 10.1093/emboj/16.6.1268 . PMC 1169725 . PMID 9135143 .
- Y. Suzuki, K. Yoshitomo-Nakagawa, K. Maruyama et al. (1997). „Konstruktion und Charakterisierung einer Volllängen-angereicherten und einer 5'-Ende-angereicherten cDNA-Bibliothek“. Gene . 200 (1–2): 149–56. doi : 10.1016/S0378-1119(97)00411-3 . PMID 9373149 .
- Louie GV, Yang W, Bowman ME, Choe S (1998). "Kristallstruktur des Komplexes von Diphtherietoxin mit einem extrazellulären Fragment seines Rezeptors" . Mol.-Nr. Zelle . 1 (1): 67–78. doi : 10.1016/S1097-2765(00)80008-8 . PMID 9659904 .
- JG Borer, JM Park, A. Atala et al. (1999). "Die Expression des Heparin-bindenden EGF-ähnlichen Wachstumsfaktors steigt selektiv in der glatten Muskulatur der Blase als Reaktion auf eine Obstruktion der unteren Harnwege". Labor. Investieren . 79 (11): 1335–45. PMID 10576204 .
- K. Nakamura, T. Mitamura, T. Takahashi et al. (2000). "Bedeutung der wichtigsten extrazellulären Domäne von CD9 und der epidermalen Wachstumsfaktor (EGF)-ähnlichen Domäne des Heparin-bindenden EGF-ähnlichen Wachstumsfaktors für die Hochregulierung von Bindung und Aktivität" . J. Biol. Chem . 275 (24): 18284–90. doi : 10.1074/jbc.M907971199 . PMID 10749879 .
- Duque JL, Adam RM, Mullen JS et al. (2001). "Heparin-bindender epidermaler Wachstumsfaktor-ähnlicher Wachstumsfaktor ist ein autokriner Mediator des menschlichen Prostatastromazellwachstums in vitro". J. Urol . 165 (1): 284–8. doi : 10.1097/00005392-200101000-00080 . PMID 11125426 .
- Lin J, Hutchinson L, Gaston SM, et al. (2001). „BAG-1 ist ein neuartiger zytoplasmatischen Bindungspartner des Membranform von Heparin-bindenden EGF-ähnlichem Wachstumsfaktor: eine einzigartige Rolle für proHB-EGF in dem Überleben der Zelle regulation“ . J. Biol. Chem . 276 (32): 30127–32. doi : 10.1074/jbc.M010237200 . PMID 11340068 .
Externe Links
- Heparin-bindender EGF-ähnlicher Wachstumsfaktor bei der US National Library of Medicine Medical Subject Headings (MeSH)