Lithium-Schwefel-Batterie - Lithium–sulfur battery
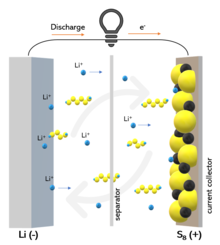 Funktionsprinzip Lithium-Schwefel-Batterie und "Shuttle"-Effekt
| |
| Spezifische Energie | 450 [Wh/kg] |
|---|---|
| Energiedichte | 550 [Wh/L] |
| Lade-/Entladeeffizienz | C/5 nominal |
| Zyklushaltbarkeit | umstritten |
| Zellnennspannung | Zellenspannung ändert sich nicht linear in dem Bereich von 2,5 bis 1,7 V während der Entladung; Batterien oft verpackt für 3 V |
Die Lithium-Schwefel-Batterie (Li-S-Batterie) ist ein Akkutyp , der sich durch seine hohe spezifische Energie auszeichnet . Das geringe Atomgewicht von Lithium und das moderate Atomgewicht von Schwefel bedeuten, dass Li-S-Batterien relativ leicht sind (etwa die Dichte von Wasser). Sie wurden auf dem (damals) längsten und höchsten unbemannten solarbetriebenen Flugzeugflug von Zephyr 6 im August 2008 eingesetzt.
Lithium-Schwefel-Batterien können aufgrund ihrer höheren Energiedichte und geringeren Kosten aufgrund der Verwendung von Schwefel anstelle von Kobalt, das üblicherweise in Lithium-Ionen -Batterien verwendet wird, Lithium-Ionen- Zellen nachfolgen. Einige Li-S-Akkus bieten spezifische Energien in der Größenordnung von 550 Wh / kg , während die meisten Lithium-Ionen-Akkus im Bereich von 150-260 Wh/kg liegen. Li-S-Batterien mit bis zu 1.500 Lade- und Entladezyklen wurden 2017 demonstriert, aber Zyklenlebensdauertests im kommerziellen Maßstab und mit magerem Elektrolyt sind noch erforderlich. Anfang 2021 waren keine im Handel erhältlich. Das Hauptproblem von Li-S-Batterien ist der Polysulfid-"Shuttle"-Effekt, der für das fortschreitende Austreten von aktivem Material aus der Kathode verantwortlich ist, was zu einer geringen Lebensdauer der Batterie führt. Außerdem erfordert die extrem niedrige elektrische Leitfähigkeit einer Schwefelkathode eine zusätzliche Masse für ein Leitmittel, um den gesamten Beitrag der aktiven Masse zur Kapazität auszunutzen. Eine große Volumenausdehnung der Schwefelkathode von S zu Li 2 S und die große Menge an benötigtem Elektrolyt sind ebenfalls Probleme, die angegangen werden müssen.
Geschichte
Die Erfindung von Li-S-Batterien geht auf die 1960er Jahre zurück, als Herbert und Ulam 1962 eine Primärbatterie patentieren lassen, die Lithium oder Lithiumlegierungen als anodisches Material, Schwefel als kathodisches Material und einen Elektrolyten aus aliphatischen gesättigten Aminen verwendet . Einige Jahre später wurde die Technologie durch die Einführung organischer Lösungsmittel wie PC , DMSO und DMF verbessert , um eine 2,35-2,5 V-Batterie zu erhalten. Ende der 1980er Jahre wurde eine wiederaufladbare Li-S-Batterie mit Ethern, insbesondere DOL , als Lösungsmittel für den Elektrolyten demonstriert . Dank wissenschaftlicher Verbesserungen auf diesem Gebiet wurde das Potenzial von Li-S-Batterien aufgezeigt. Li-S-Batterien haben in den letzten zwanzig Jahren eine erneute und wachsende Popularität erfahren. Insbesondere wurden Strategien zur Hemmung oder Abschwächung des Polysulfid-"Shuttle"-Effekts von vielen Forschern eingehend untersucht und untersucht.
Manthiram identifizierte die kritischen Parameter, die für eine kommerzielle Akzeptanz erforderlich sind. Insbesondere müssen Li-S-Batterien eine Schwefelbeladung von >5 mg cm -2 , einen Kohlenstoffgehalt von <5%, ein Elektrolyt-zu-Schwefel-Verhältnis von <5 μL mg -1 , ein Elektrolyt-zu-Kapazitäts-Verhältnis von < . erreichen 5 μL (mA h) –1 und ein negatives zu positives Kapazitätsverhältnis von <5 in Zellen vom Pouch-Typ.
Bis 2017 waren 700 verwandte Publikationen erschienen.
Im Jahr 2021 kündigten Forscher die Verwendung eines Anodenadditivs auf Zuckerbasis an, das die Freisetzung von Polysulfidketten aus der Kathode verhindert, die die Anode verschmutzen. Eine Prototypzelle demonstrierte 1.000 Ladezyklen mit einer Kapazität von 700 mAh/g.
Chemie
Chemische Prozesse in der Li-S - Zelle umfassen Lithium Auflösung von der Anodenoberfläche (und Einbau in Alkalimetall Polysulfid Salze ) während der Entladung und umgekehrte Lithium Plattierung an die Anode während des Ladevorgangs.
Anode
An der anodischen Oberfläche kommt es zur Auflösung des metallischen Lithiums unter Bildung von Elektronen und Lithiumionen während der Entladung und galvanischer Abscheidung während der Ladung. Die Halbreaktion wird ausgedrückt als:
In Analogie zu Lithiumbatterien verursacht die Auflösungs-/Elektroabscheidungsreaktion im Laufe der Zeit Probleme des instabilen Wachstums der Festelektrolytgrenzfläche (SEI), wodurch aktive Zentren für die Nukleation und das dendritische Wachstum von Lithium erzeugt werden. Dendritisches Wachstum ist für den internen Kurzschluss in Lithiumbatterien verantwortlich und führt zum Tod der Batterie selbst.
Kathode
In Li-S - Batterien, Energie in der Schwefel gespeichert Kathode (S 8 ). Während der Entladung wandern die Lithiumionen im Elektrolyten zur Kathode, wo der Schwefel zu Lithiumsulfid (Li 2 S) reduziert wird . Während der Wiederaufladephase wird der Schwefel zu S 8 reoxidiert . Die Halbreaktion wird daher ausgedrückt als:
(E ° ≈ 2,15 V gegen Li / Li + )
Tatsächlich ist die Schwefelreduktionsreaktion zu Lithiumsulfid viel komplexer und beinhaltet die Bildung von Lithiumpolysulfiden (Li 2 S x , 2 ≤ x ≤ 8) bei abnehmender Kettenlänge gemäß der Reihenfolge:
Das Endprodukt ist eigentlich eine Mischung aus Li 2 S 2 und Li 2 S statt reinem Li 2 S, aufgrund der langsamen Reduktionskinetik an Li 2 S. Dies steht im Gegensatz zu herkömmlichen Lithium-Ionen - Zellen, wobei die Lithiumionen interkaliert in die Anode und Kathode. Jedes Schwefelatom kann zwei Lithiumionen aufnehmen. Typischerweise nehmen Lithium-Ionen-Batterien nur 0,5–0,7 Lithium-Ionen pro Wirtsatom auf. Folglich ermöglicht Li-S eine viel höhere Lithium-Speicherdichte. Polysulfide werden an der Kathodenoberfläche nacheinander reduziert, während sich die Zelle entlädt:
-
S
8→ Li
2S
8→ Li
2S
6→ Li
2S
4→ Li
2S
3
Über einen porösen Diffusions Separator, Schwefelpolymere bilden auf der Kathode als Zellkosten:
- Li
2S → Li
2S
2→ Li
2S
3→ Li
2S
4→ Li
2S
6→ Li
2S
8 → S
8
Diese Reaktionen sind denen in der Natrium-Schwefel-Batterie analog .
Die Hauptherausforderungen von Li-S-Batterien sind die geringe Leitfähigkeit von Schwefel und seine erhebliche Volumenänderung beim Entladen und die Suche nach einer geeigneten Kathode ist der erste Schritt zur Kommerzialisierung von Li-S-Batterien. Daher verwenden die meisten Forscher eine Kohlenstoff/Schwefel-Kathode und eine Lithium-Anode. Schwefel ist sehr billig, hat aber praktisch keine elektrische Leitfähigkeit , 5 × 10 −30 S ⋅cm −1 bei 25 °C. Eine Kohlenstoffbeschichtung sorgt für die fehlende elektrische Leitfähigkeit. Kohlenstoff-Nanofasern bieten einen effektiven Elektronenleitungspfad und strukturelle Integrität, jedoch mit dem Nachteil höherer Kosten.
Ein Problem beim Lithium-Schwefel-Design besteht darin, dass, wenn der Schwefel in der Kathode Lithium absorbiert, eine Volumenausdehnung der Li x S-Zusammensetzungen auftritt und die vorhergesagte Volumenausdehnung von Li 2 S fast 80 % des Volumens des ursprünglichen Schwefels beträgt. Dies verursacht große mechanische Belastungen an der Kathode, was eine der Hauptursachen für einen schnellen Abbau ist. Dieser Prozess reduziert den Kontakt zwischen Kohlenstoff und Schwefel und verhindert den Fluss von Lithiumionen an die Kohlenstoffoberfläche.
Die mechanischen Eigenschaften der lithiierten Schwefelverbindungen hängen stark vom Lithiumgehalt ab und mit steigendem Lithiumgehalt verbessert sich die Festigkeit lithiierter Schwefelverbindungen, obwohl dieser Anstieg nicht linear mit der Lithiierung verläuft.
Einer der Hauptdefizite der meisten Li-S-Zellen sind unerwünschte Reaktionen mit den Elektrolyten. Während S und Li
2S sind in den meisten Elektrolyten relativ unlöslich, viele intermediäre Polysulfide sind es nicht. Auflösen von Li
2S
nin Elektrolyte führt zu einem irreversiblen Verlust an aktivem Schwefel. Die Verwendung von hochreaktivem Lithium als negative Elektrode verursacht die Dissoziation der meisten der üblicherweise verwendeten Elektrolyte anderer Art. Verwendung einer Schutzschicht in der Anodenoberfläche untersucht worden Zelle Sicherheit zu verbessern, das heißt, unter Verwendung von Teflon zeigte eine Verbesserung Beschichtung in der Elektrolytstabilität, LIPON, Li 3 N ebenfalls vielversprechende Leistung zeigt.
Polysulfid "Shuttle"
Historisch gesehen ist der "Shuttle"-Effekt die Hauptursache für die Degradation einer Li-S-Batterie. Das Lithiumpolysulfid Li 2 S x (6≤x≤8) ist in den üblichen Elektrolyten für Li-S-Batterien gut löslich. Sie werden gebildet und entweichen aus der Kathode und diffundieren zur Anode, wo sie zu kurzkettigen Polysulfiden reduziert werden und zurück zur Kathode diffundieren, wo wieder langkettige Polysulfide gebildet werden. Dieser Prozess führt zum kontinuierlichen Austreten von aktivem Material aus der Kathode, Lithiumkorrosion, niedrigem Coulomb-Wirkungsgrad und geringer Batterielebensdauer. Darüber hinaus ist der "Shuttle"-Effekt für die charakteristische Selbstentladung von Li-S-Batterien verantwortlich, da sich Polysulfide auch im Ruhezustand langsam auflösen. Der „Shuttle“-Effekt in einer Li-S-Batterie lässt sich mit einem Faktor f c (0<f c <1) quantifizieren , bewertet durch die Verlängerung des Ladespannungsplateaus. Der Faktor f c ist gegeben durch den Ausdruck:
wobei k s , q up , [S tot ] und I c jeweils die kinetische Konstante, die spezifische Kapazität, die zum anodischen Plateau beiträgt, die Gesamtschwefelkonzentration und der Ladestrom sind.
Elektrolyt
Herkömmlicherweise verwenden Li-S-Batterien einen flüssigen organischen Elektrolyten, der in den Poren des PP-Separators enthalten ist. Der Elektrolyt spielt eine Schlüsselrolle in Li-S-Batterien, da er sowohl auf den "Shuttle"-Effekt durch die Polysulfid-Auflösung als auch auf die SEI-Stabilisierung an der Anodenoberfläche einwirkt. Es wurde gezeigt, dass die Elektrolyte auf Basis organischer Carbonate, die üblicherweise in Li-Ionen-Batterien verwendet werden (dh PC, EC , DEC und Mischungen davon) mit der Chemie von Li-S-Batterien nicht kompatibel sind. Langkettige Polysulfide werden an elektrophilen Stellen von Carbonaten nukleophil angegriffen, was zur irreversiblen Bildung von Nebenprodukten wie Ethanol , Methanol , Ethylenglykol und Thiocarbonaten führt . In Li-S-Batterien werden herkömmlicherweise zyklische Ether (als DOL ) oder kurzkettige Ether (als DME ) sowie die Familie der Glykolether, einschließlich DEGDME und TEGDME, verwendet . Ein üblicher Elektrolyt ist 1M LiTFSI in DOL:DME 1:1 vol. mit 1% w/w di LiNO 3 als Additiv für die Lithium-Oberflächenpassivierung.
Sicherheit
Aufgrund der hohen potentiellen Energiedichte und der nichtlinearen Entladungs- und Ladereaktion der Zelle werden manchmal ein Mikrocontroller und andere Sicherheitsschaltungen zusammen mit Spannungsreglern verwendet , um den Zellenbetrieb zu steuern und eine schnelle Entladung zu verhindern .
Forschung
| Anode | Kathode | Datum | Quelle | Spezifische Kapazität nach dem Radfahren | Anmerkungen |
|---|---|---|---|---|---|
| Lithiummetall | Polyethylenglykol- beschichteter, narbiger mesoporöser Kohlenstoff | 17. Mai 2009 | Universität Waterloo | 1.110 mA⋅h/g nach 20 Zyklen bei einem Strom von 168 mA⋅g −1 | Minimale Verschlechterung während des Ladezyklus. Um Polysulfide in der Kathode zurückzuhalten, wurde die Oberfläche funktionalisiert, um (hydrophobe) Polysulfide abzustoßen. In einem Test mit einem Glyme- Lösungsmittel verlor eine herkömmliche Schwefelkathode über 30 Zyklen 96 % ihres Schwefels , während die experimentelle Kathode nur 25 % verlor. |
| Lithiummetall | Schwefelbeschichtete, ungeordnete Kohlenstoff-Hohlkohlenstoff-Nanofasern | 2011 | Universität in Stanford | 730 mA⋅h/g nach 150 Zyklen (bei 0,5 C) | Ein Elektrolytzusatz steigerte die Faraday-Effizienz von 85 % auf über 99 %. |
| Silizium-Nanodraht/Kohlenstoff | Schwefelbeschichtete, ungeordnete Kohlenstoffnanoröhren aus Kohlenhydraten | 2013 | CGS | 1.300 mAh/g nach 400 Zyklen (bei 1 C) | Mikrowellenbearbeitung von Materialien und Laserdruck von Elektroden. |
| Siliziumkohle | Schwefel | 2013 | Fraunhofer-Institut für Werkstoff- und Strahltechnik IWS | ? nach 1.400 Zyklen | |
| Copolymerisierter Schwefel | 2013 | Universität von Arizona | 823 mAh/g bei 100 Zyklen | Verwendet "inverse Vulkanisation " auf hauptsächlich Schwefel mit einer kleinen Menge 1,3-Diisopropenylbenzol (DIB) Additiv | |
| Poröses TiO 2-eingekapselte Schwefel-Nanopartikel |
2013 | Universität in Stanford | 721 mA⋅h/g bei 1.000 Zyklen (0,5 C) | Schale schützt das Schwefel-Lithium-Zwischenprodukt vor Elektrolytlösungsmittel. Jedes Kathodenteilchen hat einen Durchmesser von 800 Nanometern. Faraday-Wirkungsgrad von 98,4 %. | |
| Schwefel | Juni 2013 | Oak Ridge National Laboratory | 1200 mAh/g bei 300 Zyklen bei 60 °C (0,1 C)
800 mA·h/g bei 300 Zyklen bei 60 °C (1 C) |
Fester Elektrolyt aus Lithiumpolysulfidophosphat. Halbe Spannung typischer LIBs. Verbleibende Probleme sind die geringe Ionenleitfähigkeit des Elektrolyten und die Sprödigkeit der Keramikstruktur. | |
| Lithium | Schwefel- Graphenoxids Nanokomposit mit Styrol-Butadien - Carboxymethylcellulose Copolymerbindemittel | 2013 | Lawrence Berkeley National Laboratory | 700 mAh/g bei 1.500 Zyklen (0,05 C Entladung)
400 mA·h/g bei 1.500 Zyklen (0,5 C Laden / 1 C Entladen) |
Spannung zwischen ca. 1,7 und 2,5 Volt, je nach Ladezustand. Lithium-bis(trifluormethansulfonyl)imid) gelöst in einer Mischung aus n-Methyl-(n-butyl)pyrrolidinium-bis(trifluormethansulfonyl)-imid (PYR14TFSI), 1,3-Dioxolan (DOL), Dimethoxyethan (DME) mit 1 M Lithium-bis-( Trifluormethylsulfonyl)imid (LiTFSI) und Lithiumnitrat ( LiNO 3). Separator aus Polypropylen mit hoher Porosität. Spezifische Energie beträgt 500 W⋅h/kg (anfänglich) und 250 W⋅h/kg bei 1.500 Zyklen (C=1,0) |
| lithiierter Graphit | Schwefel | Februar 2014 | Pacific Northwest National Laboratory | 400 Zyklen | Die Beschichtung verhindert, dass Polysulfide die Anode zerstören. |
| lithiiertes Graphen | Schwefel/Lithium-Sulfid-Passivierungsschicht | 2014 | OXIS-Energie | 240 mAh/g (1000 Zyklen)
25 Ah/Zelle |
Passivierungsschicht verhindert Schwefelverlust |
| lithiierter Hartkohlenstoff | Schwefel-Copolymer (Poly(S-co-DVB)) | 2019 | Chungnam National University | 400 mAh/g für 500 Zyklen bei 3C | Die SEI von Hartkohlenstoff verhindert die Ablagerung von Polysulfiden an der Anode und ermöglicht eine hohe Leistung. |
| Lithium-Schwefel-Batterien | Kohlenstoff-Nanoröhrchen/Schwefel | 2014 | Tsinghua Universität | 15,1 mA·h⋅cm −2 bei einer Schwefelbeladung von 17,3 mg S ⋅cm −2 | Es wurde eine freistehende CNT-S-Papierelektrode mit hoher flächiger Schwefelbeladung hergestellt, bei der kurze MWCNTs als kurzreichweitiges elektrisch leitfähiges Netzwerk und superlange CNTs sowohl als weitreichendes leitfähiges Netzwerk als auch als gekreuzte Bindemittel fungierten. |
| Glasbeschichteter Schwefel mit leicht reduziertem Graphenoxid zur strukturellen Unterstützung | 2015 | University of California, Riverside | 700 mA⋅h⋅g −1 (50 Zyklen) | Glasbeschichtung verhindert, dass Lithiumpolysulfide dauerhaft zu einer Elektrode wandern | |
| Lithium | Schwefel | 2016 | LEITAT | 500 Wh/kg | ALISE H2020-Projekt entwickelt eine Li-S-Batterie für Autos mit neuen Komponenten und optimiert in Bezug auf Anode, Kathode, Elektrolyt und Separator |
| Lithiummetall | Geschwefeltes Graphen | 2021 | CATRIN, Palacký-Universität [1] | 644 mA⋅h⋅g -1 (250 Zyklen) | Ein effizienter und unkomplizierter Ansatz zur Herstellung einer kovalent geschwefelten Graphenkathode für Li-S-Batterien mit hohem Schwefelgehalt und hoher Zyklenstabilität. |
Vermarktung
Bis 2021 waren nur wenige Unternehmen in der Lage, die Technologie im industriellen Maßstab zu kommerzialisieren. Unternehmen wie Sion Power haben sich mit Airbus Defence and Space zusammengetan , um ihre Lithium-Schwefel-Batterietechnologie zu testen. Airbus Defence and Space hat seinen Prototyp eines High Altitude Pseudo-Satellite (HAPS)-Flugzeugs, das tagsüber mit Sonnenenergie und nachts mit Lithium-Schwefel-Batterien betrieben wird, erfolgreich während eines 11-tägigen Fluges unter realen Bedingungen gestartet . Die im Testflug verwendeten Batterien nutzten die Li-S-Zellen von Sion Power, die 350 Wh/kg liefern. Sion behauptete ursprünglich, sich in der Serienfertigung mit Verfügbarkeit bis Ende 2017 zu befinden; In jüngerer Zeit ist jedoch zu sehen, dass sie die Arbeit an ihrer Lithium-Schwefel-Batterie zugunsten einer Lithium-Metall-Batterie eingestellt haben.
Das britische Unternehmen OXIS Energy hat einen Prototyp von Lithium-Schwefel-Batterien entwickelt. Gemeinsam mit dem Imperial College London und der Cranfield University veröffentlichten sie Ersatzschaltbild-Netzwerkmodelle für ihre Zellen. Mit Lithium Balance of Denmark bauten sie einen Prototypen eines Rollerbatteriesystems hauptsächlich für den chinesischen Markt. Die Prototyp-Batterie hat eine Kapazität von 1,2 kWh mit 10 Ah Long Life-Zellen, wiegt 60 % weniger als Blei-Säure-Batterien mit einer deutlichen Reichweitensteigerung. Sie haben auch einen 3U- Rack-Mounted-Akku mit 3.000 Wh gebaut, der nur 25 kg wiegt und vollständig skalierbar ist. Sie gehen davon aus, dass ihre Lithium-Schwefel-Batterien in der Massenproduktion etwa 200 US-Dollar/kWh kosten werden. Das Unternehmen hat im Mai 2021 den Konkursstatus (Insolvenz) erreicht.
Sony , das auch den ersten Lithium-Ionen-Akku vermarktete, plante, im Jahr 2020 Lithium-Schwefel-Akkus auf den Markt zu bringen, hat aber seit der ersten Ankündigung im Jahr 2015 keine Updates mehr bereitgestellt.
Das Department of Mechanical and Aerospace Engineering der Monash University in Melbourne, Australien, hat eine Li-S-Batterie mit ultrahoher Kapazität entwickelt, die von Partnern des Fraunhofer-Instituts für Werkstoff- und Strahltechnik in Deutschland hergestellt wurde. Der Akku soll ein Smartphone fünf Tage lang mit Strom versorgen.
Siehe auch
Verweise
Externe Links
- "OXIS-Energie" . OXIS-Energie . Abgerufen 2013-10-30 .
- "PolyPlus Lithium-Schwefel" . Polyplus.com. Archiviert vom Original am 20.04.2013 . Abgerufen 2013-04-06 .
- "Sion Power" . Sitten macht . Abgerufen 2013-04-06 .
- "Winston Batterie Limited" . En.winston-battery.com. Archiviert vom Original am 2014-03-25 . Abgerufen 2013-04-06 .
- "EEMB-Batterie" . EEMB-Batterie. Abgerufen 2018-04-13.




![{\displaystyle fc={\frac {k_{\text{s}}q_{\text{up}}[S_{\text{tot}}]}{I_{c}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/92767aff703c9811fcd59e4023389b4a8bdf304f)