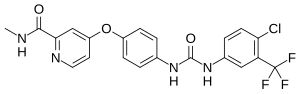
Sorafenib- Sorafenib
 | |
 | |
| Klinische Daten | |
|---|---|
| Namen austauschen | Nexavar, andere |
| Andere Namen | Nexavar Sorafenib Tosylat |
| AHFS / Drugs.com | Monographie |
| MedlinePlus | a607051 |
| Lizenzdaten | |
| Schwangerschaft Kategorie |
|
| Wege Verwaltung |
Mit dem Mund |
| ATC-Code | |
| Rechtsstellung | |
| Rechtsstellung | |
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 38–49 % |
| Proteinbindung | 99,5% |
| Stoffwechsel | Hepatische Oxidation und Glucuronidierung ( CYP3A4 & UGT1A9 -vermittelte) |
| Beseitigung Halbwertszeit | 25–48 Stunden |
| Ausscheidung | Kot (77%) und Urin (19%) |
| Bezeichner | |
| |
| CAS-Nummer | |
| PubChem- CID | |
| IUPHAR/BPS | |
| Arzneimittelbank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| PDB-Ligand | |
| CompTox-Dashboard ( EPA ) | |
| ECHA-InfoCard |
100.110.083 |
| Chemische und physikalische Daten | |
| Formel | C 21 H 16 Cl F 3 N 4 O 3 |
| Molmasse | 464,83 g·mol -1 |
| 3D-Modell ( JSmol ) | |
| |
| |
| (verifizieren) | |
Sorafenib (gemitentwickelt und Co-vermarktet von Bayer und Onyx Pharmaceuticals als Nexavar ), ist ein Kinase - Inhibitor Medikament für die Behandlung von primärem Nierenkrebs (Advanced zugelassene Nierenzellkarzinom ), erweitern primären Leberkrebs ( hepatozelluläres Karzinom ), FLT3-ITD positive AML und radioaktives Jod-resistentes fortgeschrittenes Schilddrüsenkarzinom.
Wirkmechanismus
Sorafenib ist ein Protein - Kinase - Inhibitor mit Aktivität gegen viele Proteinkinasen , einschließlich VEGFR , PDGFR und RAF - Kinasen . Von den RAF-Kinasen ist Sorafenib selektiver für c-Raf als für B-RAF . (Siehe BRAF (Gen)#Sorafenib für Details zur Wechselwirkung des Arzneimittels mit B-Raf.)
Die Behandlung mit Sorafenib induziert eine Autophagie , die das Tumorwachstum unterdrücken kann. Aufgrund seiner 1,3-disubstituierten Harnstoffstruktur ist Sorafenib auch ein potenter Inhibitor der löslichen Epoxidhydrolase , und diese Aktivität verringert wahrscheinlich die Schwere seiner Nebenwirkungen.
Medizinische Anwendungen
Sorafenib ist indiziert zur Behandlung von fortgeschrittenem Nierenzellkarzinom (RCC), nicht resezierbarem hepatozellulärem Karzinom (HCC) und Schilddrüsenkrebs .
Nierenkrebs
Klinische Studienergebnisse, die im Januar 2007 veröffentlicht wurden, zeigten, dass die Behandlung mit Sorafenib im Vergleich zu Placebo das progressionsfreie Überleben bei Patienten mit fortgeschrittenem klarzelligem Nierenzellkarzinom, bei denen eine vorherige Therapie versagt hat, verlängert. Das mediane progressionsfreie Überleben betrug 5,5 Monate in der Sorafenib-Gruppe und 2,8 Monate in der Placebo-Gruppe ( Hazard Ratio für Krankheitsprogression in der Sorafenib-Gruppe 0,44; 95 % Konfidenzintervall [KI] 0,35 bis 0,55; P < 0,01).
In Australien ist dies eine von zwei TGA-gekennzeichneten Indikationen für Sorafenib, obwohl es für diese Indikation nicht im Pharmaceutical Benefits Scheme aufgeführt ist .
Leberkrebs
Auf der ASCO 2007 wurden Ergebnisse der SHARP-Studie präsentiert, die die Wirksamkeit von Sorafenib bei Leberzellkarzinomen zeigten . Der primäre Endpunkt war das mediane Gesamtüberleben , das bei Patienten, die Sorafenib erhielten, im Vergleich zu Placebo eine Verbesserung um 44 % zeigte ( Hazard Ratio 0,69; 95 % KI 0,55 bis 0,87; p = 0,0001). Sowohl das mediane Überleben als auch die Zeit bis zur Progression zeigten 3-Monats-Verbesserungen; es gab jedoch keinen signifikanten Unterschied in der medianen Zeit bis zum symptomatischen Fortschreiten ( p = 0,77). Es gab keinen Unterschied in Bezug auf die Lebensqualität, der möglicherweise auf die Toxizität von Sorafenib oder Symptome im Zusammenhang mit der zugrunde liegenden Progression der Lebererkrankung zurückzuführen ist. Bemerkenswert ist, dass diese Studie nur Patienten mit einer Child-Pugh-Klasse A (dh der leichtesten) Zirrhose umfasste . Aufgrund dieser Studie erhielt Sorafenib im November 2007 die FDA-Zulassung für die Behandlung des fortgeschrittenen hepatozellulären Karzinoms.
In einer randomisierten, doppelblinden Phase-II-Studie zur Kombination von Sorafenib mit Doxorubicin war die mediane Zeit bis zur Progression bei Patienten mit fortgeschrittenem hepatozellulärem Karzinom im Vergleich zu Doxorubicin allein nicht signifikant verzögert. Die mediane Dauer des Gesamtüberlebens und des progressionsfreien Überlebens war bei Patienten, die Sorafenib plus Doxorubicin erhielten, signifikant länger als bei Patienten, die nur Doxorubicin erhielten.
Eine prospektive monozentrische Phase-II-Studie, an der Patienten mit inoperablem hepatozellulärem Karzinom (HCC) teilnahmen, kam zu dem Schluss, dass die Kombination von Sorafenib und DEB – TACE bei Patienten mit inoperablem HCC gut verträglich und sicher ist, wobei die meisten Toxizitäten im Zusammenhang mit Sorafenib stehen.
In Australien ist dies die einzige Indikation, für die Sorafenib in der PBS gelistet ist und damit die einzige staatlich subventionierte Indikation für Sorafenib. Das hepatozelluläre Karzinom gehört neben dem Nierenzellkarzinom zu den TGA- markierten Indikationen für Sorafenib.
Schilddrüsenkrebs
Am 22. November 2013 wurde Sorafenib von der FDA zur Behandlung des lokal rezidivierenden oder metastasierten, progressiven differenzierten Schilddrüsenkarzinoms (DTC) zugelassen, das gegenüber einer Behandlung mit radioaktivem Jod refraktär ist.
Die Phase-3-Studie DECISION zeigte eine signifikante Verbesserung des progressionsfreien Überlebens, jedoch nicht des Gesamtüberlebens. Die Nebenwirkungen waren jedoch bekanntlich sehr häufig, insbesondere Hand- und Fußhautreaktionen.
Desmoidtumoren
Nach positiven Ergebnissen in den ersten beiden Studienphasen wird derzeit eine klinische Phase-3-Studie zur Wirksamkeit von Sorafenib zur Behandlung von Desmoidtumoren (auch als aggressive Fibromatose bekannt ) getestet . Die Dosierung ist in der Regel halb so hoch wie bei bösartigen Krebsarten (400 mg vs. 800 mg). NCI sponsert diese Studie.
Nebenwirkungen
Nebenwirkungen nach Häufigkeit
Hinweis: Potenziell schwerwiegende Nebenwirkungen sind fett gedruckt .
Sehr häufig (>10% Häufigkeit)
- Lymphopenie
- Hypophosphatämie
- Blutung
- Hypertonie
- Durchfall
- Ausschlag
- Alopezie (Haarausfall; tritt bei etwa 30 % der Patienten auf, die Sorafenib erhalten)
- Hand-Fuß-Syndrom
- Pruritus (Juckreiz)
- Erythem
- Erhöhte Amylase
- Erhöhte Lipase
- Ermüdung
- Schmerzen
- Brechreiz
- Erbrechen
Häufig (1-10% Häufigkeit)
- Leukopenie
- Neutropenie
- Anämie
- Thrombozytopenie
- Anorexie (Gewichtsverlust)
- Hypokalzämie
- Hypokaliämie
- Depression
- Periphere sensorische Neuropathie
- Tinnitus
- Kongestive Herzinsuffizienz
- Herzinfarkt
- Myokardischämie
- Heiserkeit
- Verstopfung
- Stomatitis
- Dyspepsie
- Dysphagie
- Trockene Haut
- Exfoliative Dermatitis
- Akne
- Hautschuppung
- Arthralgie
- Myalgie
- Nierenversagen
- Proteinurie
- Erektile Dysfunktion
- Asthenie (Schwäche)
- Fieber
- Grippeähnliche Erkrankung
- Vorübergehender Anstieg der Transaminase
Gelegentlich (0,1-1 % Häufigkeit)
- Follikulitis
- Infektion
- Überempfindlichkeitsreaktionen
- Hypothyreose
- Hyperthyreose
- Hyponatriämie
- Dehydration
- Reversible posteriore Leukenzephalopathie
- Hypertensiven Krise
- Rhinorrhö
- Interstitielle lungenkrankheitsähnliche Ereignisse
- Gastroösophageale Refluxkrankheit (GERD)
- Pankreatitis
- Gastritis
- Magen-Darm-Perforationen
- Anstieg des Bilirubins , der möglicherweise zu Gelbsucht führt
- Cholezystitis
- Cholangitis
- Ekzem
- Erythema multiforme
- Keratoakanthom
- Plattenepithelkarzinom
- Gynäkomastie (Schwellung des Brustgewebes bei Männern)
- Vorübergehender Anstieg der alkalischen Phosphatase im Blut
- INR abnormal
- Prothrombinspiegel abnormal
- bauchige Hautreaktion
Selten (0,01-0,1% Häufigkeit)
- Verlängerung des QT-Intervalls
- Angioödem
- Anaphylaktische Reaktion
- Hepatitis
- Strahlenrückrufdermatitis
- Stevens-Johnson-Syndrom
- Leukozytoklastische Vaskulitis
- Toxische epidermale Nekrolyse
- Nephrotisches Syndrom
- Rhabdomyolyse
Geschichte
Nierenkrebs
Sorafenib wurde im Dezember 2005 von der US-amerikanischen Food and Drug Administration (FDA) zugelassen und im Juli 2006 von der Europäischen Kommission für die Behandlung von fortgeschrittenem Nierenkrebs zugelassen.
Leberkrebs
Die Europäische Kommission erteilte dem Medikament im Oktober 2007 die Marktzulassung für die Behandlung von Patienten mit hepatozellulärem Karzinom (HCC), der häufigsten Form von Leberkrebs, und die FDA-Zulassung für diese Indikation folgte im November 2007.
Im November 2009 lehnte das britische National Institute of Clinical Excellence die Zulassung des Medikaments für den NHS in England, Wales und Nordirland mit der Begründung ab, dass seine Wirksamkeit (die Überlebensrate bei primärem Leberkrebs um 6 Monate verlängert) seinen hohen Preis nicht rechtfertige , bei bis zu £3000 pro Patient und Monat. In Schottland war dem Medikament aus dem gleichen Grund bereits die Zulassung durch das Scottish Medicines Consortium für die Verwendung innerhalb des NHS Scotland verweigert worden .
Im März 2012 erteilte das indische Patentamt dem inländischen Unternehmen Natco Pharma eine Lizenz zur Herstellung von generischem Sorafenib, wodurch der Preis um 97 % gesenkt wurde. Bayer verkauft einen Monatsvorrat von 120 Tabletten Nexavar für 280.000 Yen (3.900 US-Dollar). Natco Pharma wird 120 Tabletten für verkaufen ₹ 8.800 (US $ 120), während immer noch ein 6% Lizenzgebühren an Bayer zahlen. Die Lizenzgebühr wurde später auf Berufung von Bayer auf 7 % angehoben. Gemäß dem Patents Act von 1970 und dem TRIPS-Abkommen der Welthandelsorganisation kann die Regierung eine Zwangslizenz erteilen, wenn ein Medikament nicht zu einem erschwinglichen Preis erhältlich ist.
Forschung
Lunge
In einigen Arten von Lungenkrebs (mit Histologie Plattenepithelkarzinom-Zellen) Sorafenib zusätzlich zu verabreichten Paclitaxel und Carboplatin kann schädlich für den Patienten.
Ovarialkarzinom
Sorafenib wurde als Erhaltungstherapie nach einer Behandlung von Eierstockkrebs und in Kombination mit einer Chemotherapie bei wiederkehrendem Eierstockkrebs untersucht, zeigte jedoch keine Ergebnisse, die zur Zulassung des Arzneimittels für diese Indikationen führten.
Gehirn (rezidivierendes Glioblastom)
An der Mayo-Klinik gibt es eine Phase-I/II-Studie zu Sorafenib und CCI-779 ( Temsirolimus ) für rezidivierendes Glioblastom .
Desmoidtumor (aggressive Fibromatose)
Eine 2011 durchgeführte Studie zeigte, dass Sorafenib gegen aggressive Fibromatose wirksam ist . Diese Studie wird als Rechtfertigung für die Anwendung von Sorafenib als Erstbehandlung bei einigen Patienten mit aggressiver Fibromatose herangezogen .
Nexavar-Kontroverse
Im Januar 2014 soll Bayer-Chef Marijn Dekkers erklärt haben, Nexavar sei für "westliche Patienten, die es sich leisten können, nicht für Inder" entwickelt worden. Dekkers hat dies jedoch nie gesagt. Tatsächlich wurden seine Worte falsch zitiert und der Kontext weggelassen. Ein Nierenkrebspatient würde 96.000 Dollar (58.000 Pfund) für eine einjährige Behandlung mit dem von Bayer hergestellten Medikament zahlen, während die Kosten für die indische Version des Generikums rund 2.800 Dollar (1.700 Pfund) betragen würden.
Anmerkungen
Verweise
Externe Links
- "Sorafenib" . Informationsportal für Arzneimittel . US-amerikanische Nationalbibliothek für Medizin.
- "Sorafenib" . Nationales Krebsinstitut .
- Klinische Studiennummer NCT00217399 für "Sorafenib and Anastrozol in Treatment Postmenopausal Women With Metastatic Breast Cancer" bei ClinicalTrials.gov
