Adenokarzinom der Lunge - Adenocarcinoma of the lung
| Adenokarzinom der Lunge | |
|---|---|
| Andere Namen | Lungenadenokarzinom |
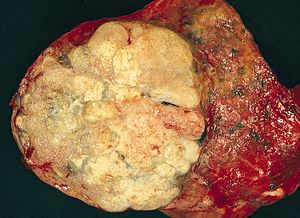 | |
| Ein grobes pathologisches Präparat eines Lungenadenokarzinoms, das bei einer Lobektomie entfernt wurde . | |
| Spezialität | Onkologie |
Das Adenokarzinom der Lunge ist die häufigste Form von Lungenkrebs und zeichnet sich wie andere Formen von Lungenkrebs durch unterschiedliche zelluläre und molekulare Merkmale aus. Es wird als einer von mehreren nicht-kleinzelligen Lungenkrebs (NSCLC) klassifiziert , um ihn von kleinzelligem Lungenkrebs zu unterscheiden, der ein anderes Verhalten und eine andere Prognose hat. Das Lungenadenokarzinom wird weiter in mehrere Subtypen und Varianten eingeteilt. Die Anzeichen und Symptome dieser speziellen Art von Lungenkrebs ähneln denen anderer Formen von Lungenkrebs, und die Patienten klagen am häufigsten über anhaltenden Husten und Kurzatmigkeit.
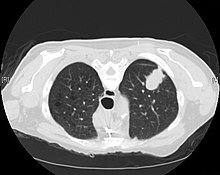
Das Adenokarzinom tritt häufiger bei Patienten mit Zigarettenrauchen in der Vorgeschichte auf und ist die häufigste Form von Lungenkrebs bei jüngeren Frauen und der asiatischen Bevölkerung. Die Pathophysiologie des Adenokarzinoms ist kompliziert, folgt aber im Allgemeinen einer histologischen Progression von Zellen in gesunden Lungen zu deutlich dysmorphen oder unregelmäßigen Zellen. Es gibt mehrere verschiedene molekulare und genetische Wege, die zu dieser Progression beitragen. Wie viele Lungenkrebsarten ist das Adenokarzinom der Lunge zum Zeitpunkt der Diagnose oft fortgeschritten. Sobald eine Läsion oder ein Tumor mit verschiedenen bildgebenden Verfahren wie Computertomographie (CT) oder Röntgen identifiziert wurde , ist eine Biopsie erforderlich, um die Diagnose zu bestätigen.
Die Behandlung dieses Lungenkrebses basiert auf dem spezifischen Subtyp und dem Ausmaß der Ausbreitung vom Primärtumor. Chirurgische Resektion, Chemotherapie , Strahlentherapie , zielgerichtete Therapie und Immuntherapie werden verwendet, um die Krebszellen basierend auf diesen Faktoren auszurotten.
Anzeichen und Symptome
Bei den meisten Patienten, bei denen Lungenkrebs diagnostiziert wird, liegt in der Regel eine lokal fortgeschrittene oder metastasierende Erkrankung vor. Nur etwa ein Drittel der Patienten hat zum Zeitpunkt der Diagnose eine Erkrankung im Stadium I. Die Symptome, die der Patient zeigt, spiegeln normalerweise das Ausmaß der Ausbreitung des Krebses wider. Lungenkrebs, der früh entdeckt wird, kann Symptome verursachen, die auf das Atmungssystem lokalisiert sind. Bei fortgeschrittenem Lungenkrebs treten jedoch bei Patienten zusätzliche Anzeichen und Symptome auf, die auf die Ausbreitung des Krebses auf andere Organsysteme zurückzuführen sind. Die häufigsten Anzeichen von Lungenkrebs sind nach der höchsten Häufigkeit geordnet:
- Husten, der nicht verschwindet oder schlimmer wird
- Gewichtsverlust
- Dyspnoe (Kurzatmigkeit oder Atembeschwerden)
- Brustschmerzen, die durch tiefes Atmen, Husten oder Lachen verstärkt werden können
- Hämoptyse (Husten von Blut oder rostfarbenem Schleim)
- Knochenschmerzen
- Clubbing
- Fieber
- sich allgemein müde oder schwach fühlen
- Obstruktion der oberen Hohlvene – Gesichts-, Hals-, Oberkörperschwellung. Dies wird durch eine Kompression des Gefäßsystems durch den Lungentumor verursacht, die den Blutrückfluss aus dem Oberkörper einschränkt.
- Dysphagie (Schluckbeschwerden oder das Gefühl, dass etwas im Hals stecken bleibt) und Heiserkeit
- erneutes Auftreten von Keuchen ohne Asthma in der Vorgeschichte
Ärzte sollten einen hohen Verdacht auf Lungenkrebs haben, insbesondere bei Patienten mit Raucheranamnese. Patienten mit wiederkehrenden oder nicht abklingenden Lungeninfektionen (z. B. Bronchitis und Lungenentzündung), die auf Antibiotika nicht ansprechen, sollten auch weiter auf Lungenkrebs untersucht werden. Bei Nichtrauchern, Frauen und Ostasiaten ist die Wahrscheinlichkeit, dass sie in jüngeren Jahren Symptome eines zugrunde liegenden Lungenkrebses aufweisen, höher. Wichtig ist, dass viele dieser Anzeichen häufig auf andere Ursachen zurückzuführen sind, die nicht Krebs sind. Von jedem Patienten sollte eine detaillierte Anamnese erhoben werden, um die Relevanz der weiteren diagnostischen Abklärung und des Managements zu bestimmen.
Extrapulmonale Manifestationen
Das Adenokarzinom ist wie andere Formen von Lungenkrebs zum Zeitpunkt der Diagnose in der Regel fortgeschritten oder metastasiert. Patienten können über Anzeichen oder Symptome außerhalb des Respirationstraktes klagen, die eine hämatologische oder metabolische Komplikation der Malignität darstellen, ohne jedoch notwendigerweise aus einer Obstruktion oder Metastasierung zu resultieren. Diese werden als paraneoplastische Syndrome bezeichnet , die oft auf eine fortgeschrittene Erkrankung und eine schlechtere Prognose hinweisen. Die häufigsten paraneoplastischen Syndrome im Zusammenhang mit einem Adenokarzinom der Lunge werden im Folgenden beschrieben:
- Eine maligne Hyperkalzämie tritt häufiger beim Plattenepithelkarzinom der Lunge auf, kann aber auch beim Adenokarzinom auftreten. Parathormon-verwandtes Peptid (PTHrP) wird von Tumorzellen produziert und funktioniert ähnlich wie Parathormon (PTH). Die Produktion dieses hormonell aktiven Peptids durch Krebszellen bewirkt eine erhöhte Knochenresorption durch Hochregulierung von Osteoklasten, einer der Zellen, die für den Knochenumbau verantwortlich sind. Beim Knochenabbau wird Kalzium in den Blutkreislauf freigesetzt, was zu einer Hyperkalzämie führt. Zu den Anzeichen und Symptomen eines erhöhten Kalziumspiegels im Blut gehören: Durst, Müdigkeit, Verstopfung, Polyurie (vermehrtes Wasserlassen) und Übelkeit. Es ist wichtig, Knochenmetastasen bei Patienten mit NSCLC auszuschließen, da sie auch eine Hyperkalzämie aufweisen.
- Hypertrophe pulmonale Osteoarthropathie (HPO) ist beim Adenokarzinom relativ selten. Weniger als 1% der Patienten mit Adenokarzinom der Lunge zeigen diesen Befund, aber wenn er auftritt, ist er ein schlechter prognostischer Faktor. Der genaue Mechanismus von HPO ist unbekannt, aber es wird angenommen, dass es hormonell oder neurogen in der Ätiologie ist. Die Trias der HPO umfasst distales Clubbing, Arthritis und bilaterale symmetrische Periostbildung.
Ursachen
Risikofaktoren
Laut Nurses' Health Study steigt das Risiko für ein Lungenadenokarzinom nach längerem Tabakrauchen deutlich an : Raucher mit einer vorherigen Rauchdauer von 30–40 Jahren erkranken mehr als doppelt so häufig an Lungenadenokarzinomen wie Nie-Raucher ( relatives Risiko von ungefähr 2,4); eine Dauer von mehr als 40 Jahren erhöht das relative Risiko auf 5.
Dieser Krebs tritt normalerweise peripher in der Lunge auf, im Gegensatz zu kleinzelligem Lungenkrebs und Plattenepithelkarzinom , die beide tendenziell zentraler lokalisiert sind, obwohl er auch als zentrale Läsionen auftreten kann. Aus unbekannten Gründen tritt sie häufig im Zusammenhang mit peripheren Lungennarben auf. Die aktuelle Theorie ist, dass die Narbe wahrscheinlich sekundär zum Tumor entstanden ist und nicht den Tumor verursacht hat. Das Adenokarzinom hat eine erhöhte Inzidenz bei Rauchern und ist die häufigste Art von Lungenkrebs bei Nichtrauchern und Frauen. Tieferes Einatmen von Zigarettenrauch führt zu peripheren Läsionen, die bei Adenokarzinomen der Lunge häufig der Fall sind. Im Allgemeinen wächst das Adenokarzinom langsamer und bildet kleinere Massen als die anderen Subtypen. Es neigt jedoch dazu, in einem frühen Stadium zu metastasieren .
Mechanismus
Pathogenese
Groß angelegte Studien wie der Cancer Genome Atlas (TCGA) haben systematisch wiederkehrende somatische Veränderungen charakterisiert, die wahrscheinlich die Entstehung und Entwicklung von Lungenadenokarzinomen antreiben.
Genmutationen und Kopienzahländerungen
Da Rauchen ein stark mutagener Faktor ist, gehört das Lungenadenokarzinom zu den Tumorarten mit der höchsten Mutationszahl. Häufige somatische Mutationen beim Lungenadenokarzinom betreffen viele Onkogene und Tumorsuppressorgene , einschließlich TP53 (mutiert in 46 % der Fälle), EGFR (27 %), KRAS (32 %), KEAP1 , STK11 und NF1 . EGFR- und KRAS-Mutationen neigen dazu, sich gegenseitig auszuschließen. KRAS-Mutationen werden mit Rauchgewohnheiten in Verbindung gebracht, während EGFR-Mutationen häufiger bei Frauen, Menschen asiatischer Abstammung und Nie-Rauchern auftreten.
Kopienzahlamplifikationen in Onkogenen wie TERT , MDM2 , EGFR, MET und MYC wurden ebenso berichtet wie Deletionen von Tumorsuppressorgenen wie CDKN2A .
Häufige Veränderungen treten in Genen auf, die zum Rezeptor-Tyrosin-Kinase- Weg gehören, von denen EGFR das prominenteste Beispiel ist. Dieser Weg ist an der Zellproliferation und am Überleben beteiligt und wird bei Krebs oft dereguliert. Als Konsequenz wurden gezielte Therapien entwickelt, um Komponenten des mutierten Signalwegs zu hemmen.
Chromosomenumlagerungen
Drei membranassoziierte Tyrosinkinase-Rezeptoren sind wiederholt an Fusionen oder Umlagerungen bei Adenokarzinomen beteiligt : ALK , ROS1 und RET , und es wurde auch über mehr als achtzig andere Translokationen bei Adenokarzinomen der Lunge berichtet.
Bei ALK-Rearrangements ist das häufigste Partnergen EML4. EML4-ALK-Fusionen treten tendenziell bei Tumoren auf, die keine EGFR- oder KRAS-Mutationen tragen und auch eine geringere Häufigkeit von TP53-Mutationen aufweisen. ALK- und ROS-Fusionen bieten Möglichkeiten für gezielte Therapien mit Tyrosinkinase-Inhibitoren.
Pathophysiologie
Die Atemwege lassen sich in zwei Hauptkomponenten unterteilen: die leitenden Atemwege und die Gasaustauschwege. Die Gasaustausch-Atemwege bestehen aus Alveolen oder kleinen mikroskopischen Luftsäcken, die für den Austausch von Sauerstoff und Kohlendioxid während der normalen Atmung verantwortlich sind. Alveolen bestehen aus zwei Zelltypen, den Pneumozyten Typ I und Typ II. Pneumozyten vom Typ I bedecken 95 % der Alveolaroberflächen und können sich nicht regenerieren. Pneumozyten vom Typ II sind häufiger und machen 60 % der Zellen innerhalb des Alveolarepithels aus, machen jedoch nur 3 % der Alveolaroberfläche aus.
Es gibt mehrere Faktoren, die zur Umwandlung des normalen Alveolarepithels in dysplastische oder präkanzeröse Läsionen beitragen. Das Adenokarzinom der Lunge entwickelt sich schrittweise, da Pneumozyten vom Typ II konsekutive molekulare Veränderungen durchlaufen, die die normale Zellregulation und den normalen Zellumsatz stören. Die atypische adenomatöse Hyperplasie (AAH) gilt als präkanzeröse Läsion und wird vermutlich zu einem Adenokarzinom in situ und einem invasiven Adenokarzinom der Lunge fortschreiten. Die Läsionen von AAH sind < 5 mm, können einzeln oder mehrfach sein und haben in der CT-Bildgebung ein mattes Aussehen. Da sich mehr genetische Mutationen und Fehlregulationen der normalen Zellsignalwege anhäufen, kann sich AAH zu einem Adenokarzinom in situ (AIS) entwickeln. AIS-Läsionen werden als kleine Tumoren < 3 cm mit abnormalem Wachstum von Pneumozyten vom Typ II klassifiziert, das auf die Alveolarräume beschränkt ist, dh ohne Invasion in das Stroma, die Pleura oder das Gefäßsystem. Diese Art des Wachstums wird als "lepidisch" bezeichnet und ist charakteristisch für das Adenokarzinom der Lunge in seinen frühesten Stadien.
Diagnose
Die Diagnose Lungenkrebs kann aufgrund typischer Symptome , insbesondere bei einer Person mit Raucheranamnese , vermutet werden . Symptome wie Bluthusten und unbeabsichtigter Gewichtsverlust können weitere Untersuchungen, wie z. B. medizinische Bildgebung, veranlassen .
Einstufung
Die Mehrheit der Lungenkrebsarten kann entweder als kleinzelliger Lungenkrebs (SCLC) oder nicht-kleinzelliger Lungenkrebs (NSCLC) charakterisiert werden. Das Lungenadenokarzinom ist einer der drei Hauptsubtypen des NSCLC, zu dem auch Plattenepithelkarzinom und großzelliges Karzinom gehören .
Historisch wurde viel über die genaueste Methode zur Beschreibung von Adenokarzinomen der Lunge diskutiert, und es wurden mehrere Revisionen der Klassifikationssysteme veröffentlicht. Zuletzt wurde 2011 die Internationale Multidisziplinäre Klassifikation des Lungenadenokarzinoms veröffentlicht und stellt den Konsens mehrerer Organisationen dar, diese spezielle Art von Lungenkrebs genauer zu beschreiben. Das aktuelle Klassifikationssystem zielt darauf ab, die Prognose und die Bestimmung des therapeutischen Managements zuverlässiger vorherzusagen.
Die Tumorgröße, das Zellwachstumsmuster und die Tiefe der Zellinvasion in normales Lungengewebe werden bei der Bestimmung der Klassifizierung berücksichtigt. Die folgenden Namen stellen eine schrittweise pathologische Progression im natürlichen Verlauf der Adenokarzinomentwicklung dar; Adenokarzinom in situ (AIS), minimalinvasives Adenokarzinom (MIA) und invasives Adenokarzinom. Das invasive Adenokarzinom der Lunge umfasst eine heterogene Mischung von Subtypen und Varianten.
Der Konsens von 2011 beschreibt fünf Subtypen invasiver Adenokarzinome basierend auf dem vorherrschenden Zellmuster. Diese Untertypen werden im Folgenden beschrieben:
- lepidisch vorherrschend
- Acinar vorherrschend
- papillär vorherrschend
- mikropapillär vorherrschend
- Feststoff überwiegend mit Muzinproduktion
Zellmuster, die Subtypen identifizieren, sind mit der Prognose verbunden, die von günstig (lepidisch) über mittel (azinär und papillär) bis hin zu schlecht (mikropapillär und solide) reicht.
Vier diskrete Varianten von invasiven Adenokarzinomen, die diesen fünf Subtypen nicht zuordenbar sind, sind ebenfalls in der aktuellen Klassifikation enthalten:
- invasives muzinöses Adenokarzinom
- kolloidales Adenokarzinom
- fetales Adenokarzinom
- enterisches Adenokarzinom
Bildgebung
Eine Röntgenaufnahme des Brustkorbs ( Röntgenbild ) ist oft der erste bildgebende Test, der durchgeführt wird, wenn eine Person mit Husten oder Brustschmerzen vorstellig wird, insbesondere in der Grundversorgung. Eine Röntgenaufnahme des Brustkorbs kann einen Lungenknoten/eine Lungenmasse erkennen, die auf Krebs hindeutet, obwohl die Sensitivität und Spezifität begrenzt sind.
Die CT-Bildgebung bietet eine bessere Beurteilung der Lunge mit höherer Sensitivität und Spezifität für Lungenkrebs im Vergleich zur Röntgenaufnahme des Thorax (obwohl immer noch eine signifikante falsch-positive Rate vorhanden ist). Die Computertomographie (CT) , die speziell auf die Beurteilung von Lungenkrebs ausgerichtet ist, umfasst den Brustkorb und den Oberbauch. Dies ermöglicht die Beurteilung anderer relevanter anatomischer Strukturen wie nahegelegener Lymphknoten, Nebennieren, Leber und Knochen, die Hinweise auf eine metastatische Ausbreitung der Krankheit zeigen können. Tatsächlich empfiehlt die US Präventive Services Task Force - jährliches Screening mit Niedrigdosis - CT bei Erwachsenen im Alter von 55 bis 80 Jahren , die eine 30 - pack-Jahre Raucht Geschichte haben und zur Zeit rauchen oder in den letzten 15 Jahren verlassen haben, mit gewissen Einschränkungen (siehe Lung Krebsvorsorge ).
Nuklearmedizinische Bildgebung, wie PET/CT und Knochenscan , können auch hilfreich sein, um an anderen Stellen des Körpers Metastasen zu diagnostizieren und zu erkennen. PET/CT verwendet einen stoffwechselaktiven Tracer, der es Klinikern ermöglicht, hypermetabolische Körperbereiche zu identifizieren. Eine erhöhte Aufnahme des Tracers tritt in malignen Zellen und in entzündlichen oder infektiösen Bereichen auf. Die Integration der Bildgebung, die die Stoffwechselaktivität widerspiegelt, mit der normalen CT-Bildgebung ermöglicht eine höhere Sensitivität und Spezifität im Vergleich zur alleinigen PET .
Die MRT ist Patienten mit fortgeschrittener Erkrankung vorbehalten, bei denen eine intrakranielle Beteiligung oder eine Beteiligung des Gehirns wahrscheinlich ist. Es ist auch hilfreich, um das Ausmaß der Brustwand, des Zwerchfells, des Plexus brachialis (wie bei Tumoren des oberen Sulkus ) oder der Wirbelsäulenbeteiligung zu beurteilen.
Histopathologie
Wenn möglich, wird eine Biopsie eines vermuteten Lungentumors durchgeführt, um eine mikroskopische Beurteilung der beteiligten Zellen vorzunehmen und ist letztendlich erforderlich, um die Diagnose zu bestätigen. Bei entfernten Läsionen sollte zunächst eine Biopsie versucht werden, um eine histologische Diagnose zu stellen und gleichzeitig das Metastasen-Staging zu bestätigen. Das Biopsiematerial wird auch verwendet, um zu analysieren, ob der Tumor irgendwelche spezifischen Mutationen exprimiert, die für eine tagesgesteuerte Therapie geeignet sind (zB EGFR-Mutation oder ALK-Mutation). Die Biopsie kann durch Bronchoskopie, transthorakale Nadelbiopsie und videoassistierte thoraskopische Chirurgie (VATS) durchgeführt werden.
Während sich die Sputumzytologie als begrenzt nützlich erwiesen hat, sollte eine Thorakozentese oder Aspiration von Pleuraflüssigkeit mit einer ultraschallgeführten Nadel durchgeführt werden, wenn ein Pleuraerguss vorliegt. Wenn maligne Zellen im Pleuraaspirat von Patienten mit hohem Verdacht auf Lungenkrebs identifiziert werden, wird eine definitive Diagnose und ein Staging (Adenokarzinom der Lunge im Stadium IV) gestellt.
Adenokarzinom der Lunge neigt dazu, Mucin positiv zu färben, da es aus den Schleim produzierenden Drüsen der Lunge stammt. Ähnlich wie bei anderen Adenokarzinomen ähnelt dieser Tumor, wenn er gut differenziert (niedriggradig) ist, der normalen Drüsenstruktur. Ein schlecht differenziertes Adenokarzinom ähnelt nicht den normalen Drüsen (hochgradig) und wird dadurch erkannt, dass es sich positiv auf Mucin (das die Drüsen produzieren) färbt. Adenokarzinom kann auch durch Färbung auf TTF-1 , einen Zellmarker für Adenokarzinom, unterschieden werden.
Wie zuvor besprochen, umfasst die Kategorie des Adenokarzinoms eine Reihe von Subtypen, und jeder Tumor neigt dazu, eine heterogene Zusammensetzung zu haben. Mehrere wichtige Subtypen werden derzeit von der Weltgesundheitsorganisation (WHO) und der International Association for the Study of Lung Cancer (IASLC) / American Thoracic Society (ATS) / European Respiratory Society (ERS) anerkannt: lepidisches prädominantes Adenokarzinom, azinäres prädominantes Adenokarzinom, papilläres vorherrschendes Adenokarzinom, mikropapilläres vorherrschendes Adenokarzinom, solides vorherrschendes Adenokarzinom und solides vorherrschendes mit Muzinproduktion. Bei bis zu 80 % dieser Tumoren werden Komponenten von mehr als einem Subtyp erkannt. Chirurgisch resezierte Tumoren sollten durch eine umfassende histologische Subtypisierung klassifiziert werden, die Befallsmuster in Schritten von 5 % beschreibt. Der vorherrschende histologische Subtyp wird dann verwendet, um den Tumor insgesamt zu klassifizieren. Der vorherrschende Subtyp ist prognostisch für das Überleben nach vollständiger Resektion.
Um die adenokarzinomatöse Abstammung der festen Variante aufzudecken, kann der Nachweis der intrazellulären Mucinproduktion durchgeführt werden. Im Epithel proximal von Adenokarzinomen können Herde von Plattenepithelmetaplasie und -dysplasie vorhanden sein, dies sind jedoch nicht die Vorläuferläsionen für diesen Tumor. Vielmehr wurde die Vorstufe peripherer Adenokarzinome als atypische adenomatöse Hyperplasie (AAH) bezeichnet. Mikroskopisch ist AAH eine gut abgegrenzte Schwerpunkt Epithelproliferation, enthaltend kubisches arme Cylinderzelle ähnelnd Club Zellen oder II - Pneumozyten Typ . Diese zeigen verschiedene Grade von zytologischen Atypien, einschließlich Hyperchromasie , Pleomorphismus , prominente Nukleolen . Die Atypie ist jedoch nicht so ausgeprägt wie bei offenen Adenokarzinomen. Läsionen von AAH sind monoklonal und teilen viele der molekularen Aberrationen (wie KRAS- Mutationen), die mit Adenokarzinomen verbunden sind.
Siegelring und klarzelliges Adenokarzinom sind keine histologischen Subtypen mehr, sondern eher zytologische Merkmale, die in Tumorzellen mehrerer histologischer Subtypen auftreten können, meistens solides Adenokarzinom.
Behandlung
Die Behandlung des Adenokarzinoms der Lunge hängt von mehreren Faktoren ab, einschließlich Stadium , Resektabilität, Leistungsstatus , Histologie und genomischen Veränderungen, die durch den individuellen Tumor erworben werden. Wie bei den meisten Krebsarten lassen sich die Behandlungsansätze grob in 5 Kategorien einteilen: Operation, Chemotherapie, Strahlentherapie, zielgerichtete Therapie und Immuntherapie.
Operation
Lungenadenokarzinome im Frühstadium (I, II und IIIA) werden typischerweise chirurgisch behandelt, um den Tumor mit Pneumonektomie oder Lobektomie zu entfernen , wenn er mit bildgebenden Studien und Biopsien als resektabel befunden wird und wenn der Patient in der Lage ist, eine Operation zu tolerieren. Video-assistierte thoraskopische Chirurgie (VATS) wird häufig angewendet, die darin besteht, ein Thorakop in einen kleinen Schnitt in der Brust einzuführen; Durch diesen kleinen Schnitt kann ein Lappen über das Endoskop entfernt werden.

Chemotherapie
Bei fortgeschrittenen (Stadium IV) und nicht resezierbaren Lungentumoren ist die Erstlinientherapie eine platinbasierte Dublett-Chemotherapie, bei der Cisplatin oder Carboplatin mit einem anderen zytotoxischen Wirkstoff kombiniert wird. Die Behandlungsschemata hängen stark vom Leistungsstatus und dem Ansprechen jedes Patienten ab, und wenn das Risiko unerwünschter Ereignisse die Lebensqualität erheblich verschlechtern könnte, wird eine unterstützende Grundversorgung eher empfohlen. Chemotherapie wird auch als adjuvante Therapie nach einer Operation eingesetzt, um verbleibende Krebszellen bei Patienten mit NSCLC im Stadium IIA, IIB und IIIA abzutöten.
Strahlentherapie
Das Adenokarzinom ist ein nicht-kleinzelliges Lungenkarzinom und spricht im Vergleich zum kleinzelligen Lungenkarzinom nicht so gut auf eine Strahlentherapie an . Die Strahlentherapie kann jedoch als adjuvante Therapie bei Patienten eingesetzt werden, die sich einer Resektion unterzogen haben, um das Risiko eines Lungenkrebsrezidivs zu verringern. Es kann auch inoperablen Tumoren, die im Brustbereich lokalisiert sind, zugute kommen und Teil der Palliativversorgung sein, um die Lebensqualität von Patienten zu verbessern, die nicht auf eine Operation oder Chemotherapie ansprechen.
Gezielte Therapie
Für Lungenadenokarzinome mit bestimmten molekularen Merkmalen steht eine gezielte Therapie zur Verfügung. Tyrosinkinase-Inhibitoren (TKIs) wurden entwickelt, um auf mutierte Komponenten des Rezeptor-Tyrosinkinase-Signalwegs wie EGFR, ALK und ROS1 abzuzielen, die bei Lungenadenokarzinomen häufige Veränderungen zeigen.
EGFR-TKIs der ersten Generation, einschließlich Gefitinib und Erlotinib , haben sich bei der Behandlung von EGFR-mutierten Patienten im Hinblick auf eine zytotoxische Chemotherapie als wirksamer erwiesen. Inhibitoren der zweiten Generation wie Afatinib und Dacomitinib boten einen breiteren Anwendungsbereich, da sie nicht nur das Protein EGFR selbst, sondern auch andere Mitglieder der EGFR-Familie wie HER2 und HER4 (auch bekannt als ERBB2 und ERBB4) angreifen können. und sie haben ein verbessertes progressionsfreies Überleben im Vergleich zu Gefitinib gezeigt. Da die häufigste Ursache für erworbene Resistenzen gegen TKIs der ersten Generation eine zweite EGFR-Mutation auf Codon 790 ist, wurde ein EGFR-TKI der dritten Generation, Osimertinib , entwickelt, um auch diese neue Mutation zu bekämpfen . Die MET-Amplifikation ist ein weiterer bekannter Mechanismus der erworbenen Resistenz.
ALK-Inhibitoren wie Crizotinib erwiesen sich als wirksam gegen Tumore, die ALK-Fusionen beherbergen. Die meisten Patienten, die zuvor mit Crizotinib behandelt wurden, profitierten von ALK-Inhibitoren der zweiten Generation, einschließlich Ceritinib , Alectinib und Brigatinib . Bei neuen erworbenen ALK-Mutationen oder -Amplifikationen können Resistenzen gegen ALK-Inhibitoren auftreten.
Auch ROS1-positive Tumoren haben aufgrund der hohen Homologie zwischen den Kinasedomänen von ROS1 und ALK eine hohe Sensitivität gegenüber ALK-Inhibitoren gezeigt .
Immuntherapie
Eine Immunantwort kann durch die Aktivierung von Immuncheckpoints verhindert werden , die in der Bindung eines Ligandenproteins (zB PD-L1 ) an einen Rezeptor (zB PD-1 ) auf der Immunzelloberfläche bestehen. Infolgedessen können Krebszellen, die PD-L1 exprimieren, T-Zellen inaktivieren und so das Tumorwachstum fördern. Immun-Checkpoint-Inhibitoren wurden entwickelt, um die T-Zell-vermittelte Antitumor-Immunität durch Blockieren entweder des Liganden oder des Rezeptors wiederherzustellen.
Immun-Checkpoint-Inhibitoren sind für NSCLC zugelassen, einschließlich Anti-PD-1- Nivolumab und Pembrolizumab . Anti-PD-1-Wirkstoffe werden bei Patienten mit fortgeschrittenem NSCLC eingesetzt, deren Tumore nach einer zytotoxischen Erstlinien-Chemotherapie fortschreiten. Pembrolizumab wurde als neuer Behandlungsstandard für Patienten mit fortgeschrittenem oder metastasiertem NSCLC mit hohen PD-L1-Expressionsspiegeln etabliert, und das Ansprechen ist bei Tumoren mit hoher Mutationslast (dh mit einer erhöhten Anzahl von Mutationen) noch ausgeprägter.
Therapieansätze, die mehrere Immun-Checkpoint-Inhibitoren oder einen Immun-Checkpoint-Inhibitor und ein Zytotoxikum kombinieren, befinden sich seit 2018 in der klinischen Erprobung. Auch die potenzielle Rolle von Anti-PD-1-Wirkstoffen als neoadjuvante Therapie bei resektablen NSCLC wird untersucht.
Epidemiologie
Wie bei anderen Lungenkrebs-Subtypen ist die Inzidenz von Lungenadenokarzinomen stark mit dem Rauchen verbunden.
Die Inzidenz des pulmonalen Adenokarzinoms hat in den letzten Jahrzehnten in vielen westlichen Industrienationen zugenommen, mit einem Anteil von 43,3 % aller Lungenkrebserkrankungen in den USA (Stand 2012) und ersetzt damit das Plattenepithelkarzinom der Lunge als häufigste Art von Lungenkrebs. Dies ist weitgehend auf die sinkenden Raucherquoten zurückzuführen, die die Adenokarzinomhistologie begünstigt. Obwohl Rauchen immer noch der stärkste Risikofaktor ist, ist das Lungenadenokarzinom bei lebenslangen Nichtrauchern mit Abstand am häufigsten (<100 Zigaretten im Leben).