Prasteron - Prasterone
 | |
 | |
| Klinische Daten | |
|---|---|
| Namen austauschen | Astenil, Cetovister, 17-Chetovis, Dastonil S, Deandros, Diandrone, Fidelin™, Hormobago, 17-Hormoforin, Intrarosa, 17-Ketovis, Mentalormon, Psicosteron |
| Andere Namen | EL-10; GL-701; KYH-3102; Androst-5-en-3β-ol-17-on; 3β-Hydroxyandrost-5-en-17-on; 5,6-Didehydroepiandrosteron; Dehydroisoepiandrosteron |
| Wege Verwaltung |
Durch den Mund , vaginal ( Einsatz ), intramuskuläre Injektion (als Prasteron-Enanthate ), Injektion (als Prasteron-Natriumsulfat ) |
| Wirkstoffklasse | Androgen ; Anabole Steroide ; Östrogen ; Neurosteroid |
| ATC-Code | |
| Rechtsstellung | |
| Rechtsstellung | |
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 50% |
| Stoffwechsel | Leber |
| Metaboliten | • Androsteron • Etiocholanolon • DHEA- Sulfat • Androstendion • Androstendiol • Testosteron • Dihydrotestosteron • Androstandiol • Estron • Estradiol |
| Beseitigung Halbwertszeit |
DHEA : 25 Minuten DHEA-S : 11 Stunden |
| Ausscheidung | Urin |
| Bezeichner | |
| |
| CAS-Nummer | |
| PubChem- CID | |
| IUPHAR/BPS | |
| Arzneimittelbank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Chemische und physikalische Daten | |
| Formel | C 19 H 28 O 2 |
| Molmasse | 288.431 g·mol -1 |
| 3D-Modell ( JSmol ) | |
| Schmelzpunkt | 148,5 °C (299,3 °F) |
| |
| |
| (verifizieren) | |
Prasterone , auch als Dehydroepiandrosteron ( DHEA ) bekannt und unter anderem unter den Markennamen Intrarosa , Diandrone und Gynodian Depot verkauft , ist ein Medikament sowie ein rezeptfreies Nahrungsergänzungsmittel, das verwendet wird, um einen DHEA-Mangel aufgrund einer Nebenniereninsuffizienz zu korrigieren oder Alter , als Bestandteil der Hormontherapie in den Wechseljahren , zur Behandlung von Schmerzen beim Geschlechtsverkehr aufgrund von Vaginalatrophie und zur Vorbereitung des Gebärmutterhalses auf die Geburt ua . Es wird oral , durch Auftragen auf die Haut , durch die Vagina oder durch Injektion in den Muskel eingenommen .
Nebenwirkungen von Prasteron bei Frauen sind Symptome der Maskulinisierung wie fettige Haut , Akne , vermehrter Haarwuchs , Stimmveränderungen und gesteigertes sexuelles Verlangen , Kopfschmerzen , Schlaflosigkeit und andere. Die Verbindung ist ein natürlich vorkommendes Prohormon von Androgenen und Östrogenen und daher ein Agonist der Androgen- und Östrogenrezeptoren , den jeweiligen biologischen Zielen von Androgenen wie Testosteron und Östrogenen wie Östradiol . Prasteron hat auch eine Vielzahl von eigenen Aktivitäten, einschließlich Neurosteroiden und anderen Aktivitäten.
Prasteron wurde 1934 entdeckt. Ein Zusammenhang zwischen dem DHEA-Spiegel und dem Altern wurde erstmals 1965 berichtet. Die Verbindung wurde in den späten 1970er Jahren als Medikament und in den frühen 1980er Jahren als Ergänzung verwendet. Die rezeptfreie Vermarktung von Prasteron als Nahrungsergänzungsmittel ist in den Vereinigten Staaten erlaubt, in vielen anderen Ländern jedoch verboten.
Medizinische Anwendungen
Mangel
DHEA und DHEA-Sulfat werden von den Nebennieren produziert . Bei Patienten mit Nebenniereninsuffizienz wie bei der Addison-Krankheit kann ein Mangel an DHEA und DHEA-Sulfat vorliegen. Darüber hinaus nehmen die Spiegel dieser Steroide im Laufe des Lebens ab und sind bei älteren Menschen im Vergleich zu jungen Erwachsenen um 70 bis 80 % niedriger. Prasteron kann verwendet werden, um den DHEA- und DHEA-Sulfatspiegel bei Nebenniereninsuffizienz und im höheren Alter zu erhöhen. Obwohl bei solchen Personen ein Mangel an diesen Steroiden besteht, ist der klinische Nutzen einer Supplementierung, falls vorhanden, ungewiss, und es gibt derzeit keine ausreichenden Beweise, um die Verwendung von Prasteron für solche Zwecke zu unterstützen.
Menopause
Prasteron wird manchmal als Androgen bei der Hormontherapie in den Wechseljahren verwendet . Neben Prasteron selbst wird ein lang anhaltendes Ester- Prodrug von Prasteron, Prasteron-Enanthat , in Kombination mit Estradiolvalerat zur Behandlung von Wechseljahrsbeschwerden unter dem Markennamen Gynodian Depot eingesetzt.
| Route | Medikation | Wichtige Markennamen | Form | Dosierung |
|---|---|---|---|---|
| Oral | Testosteronundecanoat | Andriol, Jatenzo | Kapsel | 40–80 mg 1x/1–2 Tage |
| Methyltestosteron | Metandren, Estratest | Tablette | 0,5–10 mg/Tag | |
| Fluoxymesteron | Halotestin | Tablette | 1–2,5 mg 1x/1–2 Tage | |
| Normethandron a | Ginecosid | Tablette | 5 mg/Tag | |
| Tibolon | Livial | Tablette | 1,25–2,5 mg/Tag | |
| Prasteron ( DHEA ) b | – | Tablette | 10–100 mg/Tag | |
| Sublingual | Methyltestosteron | Metandren | Tablette | 0,25 mg/Tag |
| Transdermal | Testosteron | Intrinsa | Patch | 150–300 μg/Tag |
| AndroGel | Gel, Creme | 1–10 mg/Tag | ||
| Vaginal | Prasteron ( DHEA ) | Intrarosa | Einfügung | 6,5 mg/Tag |
| Injektion | Testosteronpropionat a | Testoviron | Öllösung | 25 mg 1x/1–2 Wochen |
| Testosteron Enantat | Delatestryl, Primodian Depot | Öllösung | 25–100 mg 1x/4–6 Wochen | |
| Testosteron Cypionat | Depo-Testosteron, Depo-Testadiol | Öllösung | 25–100 mg 1x/4–6 Wochen | |
| Testosteronisobutyrat a | Femandren M, Folavirin | Wässrige Suspension | 25–50 mg 1x/4–6 Wochen | |
| Gemischte Testosteronester | Klimakteron a | Öllösung | 150 mg 1x/4–8 Wochen | |
| Omnadren, Sustanon | Öllösung | 50–100 mg 1x/4–6 Wochen | ||
| Nandrolon Decanoat | Deca-Durabolin | Öllösung | 25–50 mg 1x/6–12 Wochen | |
| Prasteron-Enanthate a | Gynodian Depot | Öllösung | 200 mg 1x/4–6 Wochen | |
| Implantieren | Testosteron | Testopel | Pellet | 50–100 mg 1x/3–6 Monate |
| Hinweise: Prämenopausale Frauen produzieren etwa 230 ± 70 µg Testosteron pro Tag (6,4 ± 2,0 mg Testosteron pro 4 Wochen), mit einem Bereich von 130 bis 330 µg pro Tag (3,6–9,2 mg pro 4 Wochen). Fußnoten: a = Meist eingestellt oder nicht verfügbar. b = Over-the-counter . Quellen: Siehe Vorlage. | ||||
Vaginalatrophie
Prasterone, unter dem Markennamen Intrarosa, wird in den zugelassenen Vereinigten Staaten in einer vaginalen Einsatz Formulierung für die Behandlung von atrophischer Vaginitis . Der Wirkmechanismus von Prasteron für diese Indikation ist nicht bekannt, obwohl er eine lokale Metabolisierung von Prasteron in Androgene und Östrogene beinhalten kann.
Sexuelles Verlangen
Prasteron wurde oral in einer Dosierung von 10 mg/Tag verwendet, um das sexuelle Verlangen bei Frauen zu steigern .
Geburt
Da das Natriumsalz von prasterone Sulfat (Markennamen Astenile, Mylis, Teloin), ein Ester - Prodrug von prasterone wird prasterone in verwenden Japan als Injektion zur Behandlung von unzureichender Zervixreifung und Zervixdilatation während der Geburt .
Verfügbare Formulare
Prasterone wurde zuvor als pharmazeutisches Medikament unter dem Markennamen Diandrone in Form einer 10 mg oralen Tablette in Großbritannien vermarktet .
Nebenwirkungen
Prasteron wird natürlich im menschlichen Körper produziert, aber die langfristigen Auswirkungen seiner Verwendung sind weitgehend unbekannt. Kurzfristig haben mehrere Studien nur wenige Nebenwirkungen festgestellt. In einer Studie von Chang et al. wurde Prasteron in einer Dosis von 200 mg/Tag über 24 Wochen verabreicht, wobei leichte androgene Wirkungen festgestellt wurden. In einer anderen Studie wurde eine Dosis von bis zu 400 mg/Tag über 8 Wochen verwendet, wobei nur wenige unerwünschte Ereignisse berichtet wurden. Eine längerfristige Studie verfolgte Patienten, die über 12 Monate mit 50 mg Prasteron behandelt wurden, wobei die Anzahl und der Schweregrad der Nebenwirkungen als gering gemeldet wurden. In einer anderen Studie wurde eine Dosis von 50 mg Prasteron über 10 Monate verabreicht, ohne dass schwerwiegende Nebenwirkungen gemeldet wurden.
Als Hormonvorläufer gibt es Berichte über Nebenwirkungen, die möglicherweise durch die Hormonmetaboliten von Prasteron verursacht werden.
Es ist nicht bekannt, ob Prasteron für die langfristige Anwendung sicher ist. Einige Forscher glauben , dass Prasteron - Nahrungsergänzungsmittel tatsächlich das Risiko für Brustkrebs , Prostatakrebs , Herzkrankheiten , Diabetes und Schlaganfall erhöhen könnten . Prasteron kann das Tumorwachstum bei hormonempfindlichen Krebsarten stimulieren, wie zum Beispiel bei einigen Arten von Brust-, Gebärmutter- und Prostatakrebs. Prasteron kann die Prostataschwellung bei Männern mit benigner Prostatahyperplasie (BPH), einer vergrößerten Prostata, verstärken.
Prasteron ist ein Steroidhormon . Hohe Dosen können bei Frauen Aggressivität, Reizbarkeit, Schlafstörungen und das Wachstum von Körper- oder Gesichtsbehaarung verursachen. Es kann auch die Menstruation stoppen und den HDL- Spiegel ("gutes" Cholesterin) senken, was das Risiko von Herzerkrankungen erhöhen könnte. Andere berichtete Nebenwirkungen sind Akne, Herzrhythmusstörungen, Leberprobleme, Haarausfall (von der Kopfhaut) und fettige Haut. Es kann auch die Regulierung des Blutzuckers durch den Körper verändern.
Prasteron kann die Tamoxifenresistenz bei Brustkrebs fördern . Es kann auch das Risiko von Gebärmutter- und Prostatakrebs aufgrund des Metabolismus in Östrogene bzw. Androgene erhöhen . Patienten, die eine Hormonersatztherapie erhalten, können bei der Einnahme von Prasteron mehr östrogenbedingte Nebenwirkungen haben. Dieses Nahrungsergänzungsmittel kann auch andere Arzneimittel beeinträchtigen, und potenzielle Wechselwirkungen zwischen ihm und Arzneimitteln und Kräutern sind möglich.
Prasteron ist möglicherweise unsicher für Personen, die schwanger sind, stillen, hormonempfindliche Erkrankungen, Leberprobleme, Diabetes, Depressionen oder Stimmungsstörungen, polyzystisches Ovarialsyndrom (PCOS) oder Cholesterinprobleme haben.
Es wurde berichtet, dass Prasteron selbst bei sehr hohen Dosierungen (z. B. das 50-fache der empfohlenen rezeptfreien Ergänzungsdosierung) nur wenige oder keine Nebenwirkungen hat. Es kann jedoch eine Maskulinisierung und andere androgene Nebenwirkungen bei Frauen und Gynäkomastie und andere östrogene Nebenwirkungen bei Männern verursachen.
Pharmakologie
Prasteron wird im Körper zu Androgenen und Östrogenen metabolisiert . Es wird umgewandelt in Androstendion von 3β-Hydroxysteroid - Dehydrogenase (3β-HSD) und in Androstendiol von 17β-Hydroxysteroid - Dehydrogenase (17β-HSD). Dann können Androstendion und Androstendiol durch 17β-HSD bzw. 3β-HSD in Testosteron umgewandelt werden . Anschließend kann Testosteron durch die 5α-Reduktase zu Dihydrotestosteron metabolisiert werden . Darüber hinaus können Androstendion und Testosteron durch Aromatase in Östron bzw. Östradiol umgewandelt werden . Prasteron wird auch durch Steroidsulfotransferase (insbesondere SULT1E1 und SULT2A1 ) reversibel in Prasteronsulfat umgewandelt , das wiederum durch Steroidsulfatase wieder in Prasteron umgewandelt werden kann . Die Umwandlung von prasterone in Androgene und Östrogene ist gewebespezifisch auftretende zum Beispiel in der Leber , Fett , Vagina , Prostata , Haut und Haarfollikel , unter anderen Geweben .
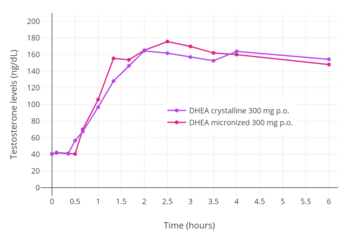
In klinischen Studien zur Prasteron-Supplementierung lagen die Dosierungen zwischen 20 und 1.600 mg pro Tag. Bei Patienten mit Nebennierenrindeninsuffizienz wurde festgestellt, dass orale Dosierungen von 20 bis 50 mg Prasteron/Tag die DHEA- und DHEA-S-Spiegel auf normale Bereiche zurückführen, die bei gesunden jungen Erwachsenen beobachtet wurden. Umgekehrt wurde festgestellt, dass orale Dosierungen von 100 bis 200 mg Prasteron/Tag zu supraphysiologischen Spiegeln von DHEA und DHEA-S führen. Bei einer hohen Dosierung von 1.600 mg/Tag oral über 4 Wochen wurde festgestellt, dass die Behandlung postmenopausaler Frauen mit Prasteron die Serumspiegel von DHEA um das 15-Fache, Testosteron um das 9-Fache, DHEA-S, Androstendion und DHT um das 20-fach und Östron und Östradiol beide um das 2-fache. Es wurde festgestellt, dass die Mikronisierung von Prasteron die bei oraler Verabreichung erreichten DHEA-S-Spiegel signifikant erhöht, jedoch keine signifikante Änderung der erreichten DHEA- oder Testosteronspiegel bewirkt.
Obwohl Prasteron den Testosteronspiegel bei Frauen zuverlässig erhöhen kann, ist dies bei Männern nicht der Fall. Es wurde festgestellt, dass eine hohe Dosierung von 1.600 mg Prasteron pro Tag bei Männern über 4 Wochen den DHEA- und Androstendionspiegel erhöht, jedoch den Testosteronspiegel nicht signifikant beeinflusst.
Chemie
Prasteron, auch bekannt als Androst-5-en-3β-ol-17-on, ist ein natürlich vorkommendes Androstan- Steroid und ein 17-Ketosteroid . Es ist strukturell eng verwandt mit Androstendiol (Androst-5-ene-3β,17β-diol), Androstendion (Androst-4-ene-3,17-dion) und Testosteron (Androst-4-en-17β-ol-3 .). -einer). Prasteron ist die δ 5 (5 (6) - dehydrierte ) analog von Epiandrosteron (5α-androstan-3β-ol-17-on), und ist auch als 5-Dehydroepiandrosteron (DHEA-5) oder δ bekannte 5 -epiandrosterone. Ein Positionsisomer von Prasteron, das eine ähnliche biologische Aktivität aufweisen kann, ist 4-Dehydroepiandrosteron (4-DHEA).
Derivate
Prasteron wird medizinisch als die C3β- Ester Prasteronenanthat und Prasteronsulfat verwendet . Das C19- Demethyl- Analogon von Prasteron ist 19-Nordehydroepiandrosteron (19-nor-DHEA), ein Prohormon von Nandrolon (19-Nortestosteron). Die 5α-reduzierten und δ 1 (1 (2) - dehydrierte ) analog prasterone ist 1-Dehydroepiandrosteron (DHEA-1 oder 1-Androsteron), die ein Prohormon von ist 1-Testosteron (δ 1 -DHT oder dihydroboldenone). Fluasteron (3β-Dehydroxy-16α-Fluor-DHEA) ist ein Derivat von Prasteron mit minimaler oder keiner hormonellen Aktivität, aber anderen erhaltenen biologischen Aktivitäten.
Geschichte
DHEA wurde entdeckt, über die Isolierung von männlicher Urin , von Adolf Butenandt und Hans Dannenbaum 1934, und die Verbindung wurde isoliert aus menschlichem Blutplasma durch Migeon und Plager 1954. DHEA - Sulfat, das 3β- Sulfatester von DHEA, wurde aus dem Urin isoliert im Jahr 1944 und wurde von Baulieu 1954 als das am häufigsten vorkommende Steroidhormon im menschlichen Plasma gefunden. Von seiner Entdeckung 1934 bis 1959 wurde DHEA in der Literatur mit einer Reihe verschiedener Namen bezeichnet, darunter Dehydroandrosteron , Transdehydroandrosteron , Dehydroisoandrosteron . und Androstenolon . Der Name Dehydroepiandrosteron , auch bekannt als DHEA , wurde erstmals 1949 von Fieser vorgeschlagen und wurde später der am häufigsten verwendete Name des Hormons. Jahrzehntelang galt DHEA nach seiner Entdeckung als inaktive Verbindung, die hauptsächlich als Zwischenprodukt bei der Produktion von Androgenen und Östrogenen aus Cholesterin diente . 1965 berichteten De Nee und Vermeulen über einen Zusammenhang zwischen DHEA-Sulfat-Spiegeln und Alterung. Danach wurde DHEA für die wissenschaftliche Gemeinschaft interessant und es wurden zahlreiche Studien durchgeführt, die den Zusammenhang zwischen DHEA- und DHEA-Sulfatspiegeln und dem Altern untersuchten.
Prasterone , die vorgeschlagene INN und empfohlene INN von DHEA und der Begriff, der verwendet wird, wenn die Verbindung als Medikament bezeichnet wird, wurden 1970 bzw. 1978 veröffentlicht. Die Kombination von 4 mg Estradiolvalerat und 200 mg Prasteronenanthat in einer Öllösung wurde 1978 unter dem Markennamen Gynodian Depot in Europa zur Anwendung in der Hormontherapie der Wechseljahre durch intramuskuläre Injektion eingeführt . In den frühen 1980er Jahren wurde Prasteron erhältlich und weit verbreitet rezeptfrei als nicht verschreibungspflichtige Ergänzung in den Vereinigten Staaten , in erster Linie als Gewichtsverlusthilfe . Es wurde als "Wundermittel" mit angeblichen Anti-Aging-, Anti-Adipositas- und Anti-Krebs-Vorteilen beschrieben. Dies dauerte bis 1985, als die Vermarktung von Prasteron von der Food and Drug Administration (FDA) aufgrund fehlender Beweise für den gesundheitlichen Nutzen und aufgrund der zu dieser Zeit unbekannten langfristigen Sicherheit und Risiken der Verbindung verboten wurde . Anschließend wurde Prasteron in den Vereinigten Staaten nach der Verabschiedung des Health and Education Act von 1994 wieder rezeptfrei als Nahrungsergänzungsmittel erhältlich . Umgekehrt ist es in Kanada , Großbritannien , Australien und Neuseeland als Ergänzung verboten .
Im Jahr 2001 reichte Genelabs einen neuen Arzneimittelantrag für Prasteron zur Behandlung von systemischem Lupus erythematodes (SLE) bei der FDA ein. Es hatte die vorläufigen Markennamen Anastar, Aslera und Prestara. Dieser Antrag wurde jedoch nicht genehmigt, und während die Entwicklung von Prasteron für SLE sowohl in den Vereinigten Staaten als auch in Europa bis 2010 andauerte, wurde das Medikament letztendlich nie für die Behandlung dieser Erkrankung zugelassen. Im Jahr 2016 hat die FDA Prasteron in einer intravaginalen Gelformulierung zur Behandlung von schmerzhaftem Geschlechtsverkehr aufgrund von vulvovaginaler Atrophie in den USA unter dem Markennamen Intrarosa zugelassen. Dies war das erste prasteronhaltige Medikament, das von der FDA in diesem Land zugelassen wurde.
Gesellschaft und Kultur
Generische Namen
Prasterone ist der generische Name von DHEA in Englisch und Italienisch und sein internationaler freier Name , der in den Vereinigten Staaten angenommene Name und der italienische Common Name , während der generische Name Prasteronum auf Latein , Prastérone auf Französisch und sein französischer Volksname und Prasteron auf Deutsch ist.
Marketing
In den Vereinigten Staaten wurden Prasteron oder Prasteronsulfat unter den Namen DHEA und DHEA-S mit der Behauptung beworben, dass sie bei einer Vielzahl von Beschwerden von Vorteil sein können. Prasteron und Prasteronsulfat sind in den Vereinigten Staaten leicht erhältlich, wo sie als rezeptfreie Nahrungsergänzungsmittel verkauft werden .
1996 schrieb der Reporter Harry Wessel vom Orlando (Florida) Sentinel über DHEA, dass "Tausende von Menschen in das Getümmel geraten sind und das Zeug in Reformhäusern, Apotheken und Versandkatalogen kaufen", aber dass "solcher Enthusiasmus" wird von vielen im medizinischen Bereich als verfrüht angesehen." Er bemerkte, dass "nationale Publikationen wie Time, Newsweek und USA Today kürzlich Artikel über das Hormon veröffentlicht haben, während mehrere große Verlage Bücher veröffentlicht haben, die es anpreisen." Seine Kolumne wurde weithin syndiziert und in anderen US-Zeitungen nachgedruckt.
Das Produkt werde "weit verbreitet an Bodybuilder vermarktet und von diesen verwendet ", schrieb Dr. Paul Donahue 2012 für das King Features Syndicate.
Verordnung
Nach Land
Australien
In Australien ist für den Kauf von Prasteron ein Rezept erforderlich, wo es auch im Vergleich zu Standardkäufen in US-Ergänzungsgeschäften vergleichsweise teuer ist. Der australische Zoll stuft Prasteron als "anabole Steroide oder Vorläufer" ein und als solche ist es nur möglich, Prasteron durch den Zoll ins Land zu bringen, wenn man eine Einfuhrgenehmigung besitzt, die man erhalten kann, wenn man eine gültige Rezept für das Hormon.
Kanada
In Kanada ist Prasteron ein kontrolliertes Arzneimittel, das unter Abschnitt 23 von Anhang IV des Gesetzes über kontrollierte Arzneimittel und Substanzen aufgeführt ist und als solches nur auf Rezept erhältlich ist.
Vereinigtes Königreich
Prasteron wird als aufgeführt Anabolikum , und ist somit ein Klasse C kontrollierter Wirkstoff .
Vereinigte Staaten
Prasteron darf in den USA als Nahrungsergänzungsmittel legal verkauft werden. Es wird derzeit grandfathered in als „Old Dietary Ingredient“ ist auf den Verkauf vor 1994 Prasterone speziell aus dem Anabolikum Control Act von 1990 und 2004 befreit ist.
Sport und Leichtathletik
Prasteron ist bei sportlichen Wettkämpfen verboten. Es ist eine verbotene Substanz nach dem Welt-Anti-Doping-Code der Welt-Anti-Doping-Agentur, die Drogentests für Olympia und andere Sportarten verwaltet.
- Yulia Efimova , die den Weltrekord sowohl im 50-Meter- als auch im 200-Meter-Brustschwimmen hält und die Bronzemedaille im 200-Meter-Brustschwimmen bei den Olympischen Spielen 2012 in London gewann, wurde außerhalb von Wettbewerben positiv auf Prasteron getestet Doping-Test.
- Rashard Lewis, damals bei den Orlando Magic, wurde positiv auf Prasteron getestet und wurde 10 Spiele vor Beginn der Saison 2009/10 gesperrt.
- Im Jahr 2016 gab der MMA- Kämpfer Fabio Maldonado bekannt, dass er während seiner Zeit bei der UFC Prasteron einnahm .
- Im Januar 2011 wurde der NBA- Spieler OJ Mayo für 10 Spiele gesperrt, nachdem er positiv auf Prasteron getestet worden war. Mayo bezeichnete seine Verwendung von Prasteron als "einen ehrlichen Fehler" und sagte, das Prasteron sei in einem rezeptfreien Nahrungsergänzungsmittel enthalten und er wisse nicht, dass das Nahrungsergänzungsmittel von der NBA verboten wurde. Mayo war der siebte Spieler, der seit Beginn der Tests der Liga im Jahr 1999 positiv auf leistungssteigernde Medikamente getestet wurde.
- Der 400-Meter-Olympiasieger Lashawn Merritt wurde 2010 positiv auf Prasteron getestet und für 21 Monate vom Sport ausgeschlossen.
- Die Tennisspielerin Venus Williams hatte die Erlaubnis des Internationalen Tennisverbandes , DHEA zusammen mit Hydrocortison zur Behandlung von "Nebenniereninsuffizienz" zu verwenden, aber sie wurde 2016 von der Welt-Anti-Doping-Agentur widerrufen , die glaubte, dass die Verwendung von DHEA Williams' sportliche Leistung verbessern würde .
Forschung
Anabole Anwendungen
Eine Metaanalyse von Interventionsstudien zeigt, dass eine Prasteron-Supplementierung bei älteren Männern einen kleinen, aber signifikanten positiven Effekt auf die Körperzusammensetzung induzieren kann, der streng von der Umwandlung von Prasteron in seine bioaktiven Metaboliten wie Androgene oder Östrogene abhängt. Die Evidenz bezüglich der Wirkung von Prasteron auf die Kraft bei älteren Menschen ist nicht eindeutig. Bei Männern mittleren Alters wurde in einer randomisierten, placebokontrollierten Studie keine signifikante Wirkung der Prasteron-Supplementierung auf fettfreie Körpermasse, Kraft oder Testosteronspiegel festgestellt.
Krebs
Es gibt keine Hinweise darauf, dass Prasteron bei der Behandlung oder Vorbeugung von Krebs von Nutzen ist .
Herzkreislauferkrankung
Eine Überprüfung im Jahr 2003 ergab, dass die damals vorliegenden Beweise ausreichend sind, um darauf hinzuweisen, dass niedrige DHEA-S-Serumspiegel mit einer koronaren Herzkrankheit bei Männern in Verbindung gebracht werden können, jedoch nicht ausreichend, um festzustellen, ob eine Prasteron-Supplementierung einen kardiovaskulären Nutzen hätte.
Prasteron kann die G6PD- mRNA-Expression verstärken und seine hemmenden Wirkungen verfälschen .
Lupus
Es gibt einige Hinweise auf einen kurzfristigen Nutzen bei Patienten mit systemischem Lupus erythematodes, jedoch nur wenige Hinweise auf einen langfristigen Nutzen oder eine Sicherheit. Prasterone wurde in den 1990er und 2000er Jahren in den USA und Europa zur Behandlung von systemischem Lupus erythematodes entwickelt und erreichte klinische Studien der Phase III bzw. die Vorregistrierung für diese Indikation, aber letztendlich wurde die Entwicklung nicht über 2010 hinaus fortgesetzt.
Speicher
Es wurde festgestellt, dass die Supplementierung mit Prasteron für die Gedächtnisfunktion bei normalen Erwachsenen mittleren Alters oder älteren Menschen nicht nützlich ist. Es wurde zur Behandlung der Alzheimer-Krankheit untersucht , aber es gibt keine Beweise dafür, dass es wirksam oder unwirksam ist. Weitere Forschung ist erforderlich, um die Vorteile zu bestimmen.
Laune
Einige kleine, kurzfristige klinische Studien haben ergeben, dass Prasteron die Stimmung verbessert, aber seine langfristige Wirksamkeit und Sicherheit sowie der Vergleich zu Antidepressiva waren bis 2015 unbekannt.
Siehe auch
Verweise
Weiterlesen
- Keppel Hesselink JM (Dezember 1997). „[Prasteron (Dihydroepiandrosteron): eine moderne Quelle ewiger Jugend?]“. Ned Tijdschr Geneeskd (auf Niederländisch). 141 (51): 2484–7. PMID 9555138 .
- Zelissen PM, Thijssen JH (Oktober 2001). „[Rolle von Prasteron (Dehydroepiandrosteron) in der Substitutionstherapie bei Nebennierenrindeninsuffizienz]“. Ned Tijdschr Geneeskd (auf Niederländisch). 145 (42): 2018–22. PMID 11695098 .
- Papst, JE; Cup, MJ; Tracy, TS (2003). Dehydroepiandrosteron (DHEA) (Prasteron) . Nahrungsergänzungsmittel . Totowa, New Jersey: Humana Press. S. 123–147. doi : 10.1007/978-1-59259-303-3_8 (inaktiv 31. Mai 2021). ISBN 9781592593033.CS1-Wartung: DOI ab Mai 2021 inaktiv ( Link )
- Kocis P (November 2006). "Prasteron". Am J Health Syst Pharm . 63 (22): 2201–10. doi : 10.2146/ajhp060100 . PMID 17090740 .
- Mendivil Dacal JM, Borges VM (April 2009). "[Dehydroepiandrosteron (DHEA), Überprüfung seiner Wirksamkeit bei der Behandlung des Libidoabfalls und anderer Symptome des Alterns]" . Actas Urol Esp (auf Spanisch). 33 (4): 390–401. doi : 10.4321/s0210-48062009000400009 . PMID 19579890 .
- Alkatib AA, Cosma M, Elamin MB, Erickson D, Swiglo BA, Erwin PJ, Montori VM (Oktober 2009). „Eine systematische Überprüfung und Metaanalyse von randomisierten, placebokontrollierten Studien zu den Auswirkungen der DHEA-Behandlung auf die Lebensqualität bei Frauen mit Nebenniereninsuffizienz“ . J. Clin. Endokrinol. Metab . 94 (10): 3676–81. doi : 10.1210/jc.2009-0672 . PMID 19773400 .
- Panjari M, Davis SR (Juni 2010). „DHEA für postmenopausale Frauen: eine Überprüfung der Beweise“. Maturitas . 66 (2): 172–9. doi : 10.1016/j.maturitas.2009.12.017 . PMID 20089375 .
- Oberbeck R, Kobbe P (2010). "Dehydroepiandrosteron (DHEA): ein Steroid mit mehreren Wirkungen. Gibt es eine mögliche Option zur Behandlung von kritischen Erkrankungen?". Curr. Med. Chem . 17 (11): 1039–47. doi : 10.2174/092986710790820570 . PMID 20156161 .
- Prati A, Santagni S, Rattighieri E, Campedelli A, Ricchieri F, Chierchia E, Despini G, Genazzani AR, Genazzani AD (Juni 2014). „[Die mutmaßliche Rolle und Verwendung von DHEA und seine Assoziation mit der Hormonersatztherapie]“. Minerva Ginecol (auf Italienisch). 66 (3): 313–24. PMID 24971788 .
- Genazzani AR, Pluchino N (August 2010). „DHEA-Therapie bei postmenopausalen Frauen: die Notwendigkeit, über den Mangel an Evidenz hinauszugehen“. Klimakterium . 13 (4): 314–6. doi : 10.3109/13697137.2010.492496 . PMID 20540592 . S2CID 5578070 .
- Luci M, Valenti G, Maggio M (September 2010). „[Dehydroepiandrosteron [DHEA(S)]: anaboles Hormon?]“. Recenti Prog Med (auf Italienisch). 101 (9): 333–44. hdl : 11381/2436727 . PMID 21268370 .
- Gleicher N , Barad DH (Mai 2011). "Dehydroepiandrosteron (DHEA) Supplementation in verminderter Ovarialreserve (DOR)" . Repro. Biol. Endokrinol . 9 : 67. doi : 10.1186/1477-7827-9-67 . PMC- 3112409 . PMID 21586137 .
- Davis SR, Panjari M, Stanczyk FZ (Juni 2011). „Klinische Überprüfung: DHEA-Ersatz für postmenopausale Frauen“ . J. Clin. Endokrinol. Metab . 96 (6): 1642–53. doi : 10.1210/jc.2010-2888 . PMID 21411558 .
- Panjari M, Davis SR (September 2011). „Vaginales DHEA zur Behandlung von Atrophie im Zusammenhang mit der Menopause: eine Überprüfung der Beweise“. Maturitas . 70 (1): 22–5. doi : 10.1016/j.maturitas.2011.06.005 . PMID 21733647 .
- Traish AM, Kang HP, Saad F, Guay AT (November 2011). „Dehydroepiandrosteron (DHEA) – ein Vorläufersteroid oder ein aktives Hormon in der menschlichen Physiologie“. J Sexmed . 8 (11): 2960–82, Quiz 2983. doi : 10.1111/j.1743-6109.2011.02523.x . PMID 22032408 .
- Savineau JP, Marthan R, Dumas de la Roque E (März 2013). „Rolle von DHEA bei Herz-Kreislauf-Erkrankungen“. Biochem. Pharmacol . 85 (6): 718–26. doi : 10.1016/j.bcp.2012.12.004 . PMID 23270992 .
- Labrie F, Labrie C (April 2013). „DHEA und Intrakrinologie in den Wechseljahren, eine positive Wahl für die Evolution der menschlichen Spezies“. Klimakterium . 16 (2): 205–13. doi : 10.3109/13697137.2012.733983 . PMID 23126249 . S2CID 6546179 .
- Rutkowski K, Sowa P, Rutkowska-Talipska J, Kuryliszyn-Moskal A, Rutkowski R (Juli 2014). „Dehydroepiandrosteron (DHEA): Hypes und Hoffnungen“. Drogen . 74 (11): 1195–207. doi : 10.1007/s40265-014-0259-8 . PMID 25022952 . S2CID 26554413 .
- Peixoto C, Devicari Cheda JN, Nardi AE, Veras AB, Cardoso A (2014). „Die Wirkungen von Dehydroepiandrosteron (DHEA) bei der Behandlung von Depressionen und depressiven Symptomen bei anderen psychiatrischen und medizinischen Erkrankungen: eine systematische Überprüfung“. Curr-Medikamentenziele . 15 (9): 901–14. doi : 10.2174/1389450115666140717111116 . PMID 25039497 .
- Elraiyah T, Sonbol MB, Wang Z, Khairalseed T, Asi N, Undavalli C, Nabhan M, Altayar O, Prokop L, Montori VM, Murad MH (Oktober 2014). "Klinische Überprüfung: Nutzen und Schaden von systemischem Dehydroepiandrosteron (DHEA) bei postmenopausalen Frauen mit normaler Nebennierenfunktion: eine systematische Überprüfung und Metaanalyse" . J. Clin. Endokrinol. Metab . 99 (10): 3536–42. doi : 10.1210/jc.2014-2261 . PMC 5393492 . PMID 25279571 .
- Maggio M, De Vita F, Fisichella A, Colizzi E, Provenzano S, Lauretani F, Luci M, Ceresini G, Dall'Aglio E, Caffarra P, Valenti G, Ceda GP (Januar 2015). „DHEA und kognitive Funktion bei älteren Menschen“. J. Steroid Biochem. Mol.-Nr. Biol . 145 : 281–92. doi : 10.1016/j.jsbmb.2014.03.014 . PMID 24794824 . S2CID 33768697 .
- Pluchino N, Drakopoulos P, Bianchi-Demicheli F, Wenger JM, Petignat P, Genazzani AR (Januar 2015). „Neurobiologie von DHEA und Auswirkungen auf Sexualität, Stimmung und Kognition“. J. Steroid Biochem. Mol.-Nr. Biol . 145 : 273–80. doi : 10.1016/j.jsbmb.2014.04.012 . PMID 24892797 . S2CID 12382989 .
- Warner M, Gustafsson JA (Januar 2015). „DHEA – ein Vorläufer von ERβ-Liganden“. J. Steroid Biochem. Mol.-Nr. Biol . 145 : 245–7. doi : 10.1016/j.jsbmb.2014.08.003 . PMID 25125389 . S2CID 26043868 .
- Lang K, Burger-Stritt S, Hahner S (Januar 2015). "Ist DHEA-Ersatz bei chronischer Nebenniereninsuffizienz von Vorteil?". Best-Practice. Res. Klin. Endokrinol. Metab . 29 (1): 25–32. doi : 10.1016/j.beem.2014.09.007 . PMID 25617170 .
- Vuksan-Ćusa B, Šagud M, Radoš I (März 2016). „Die Rolle von Dehydroepiandrosteron (DHEA) bei Schizophrenie“. Psychiater Danub . 28 (1): 30–3. PMID 26938818 .
- Prough RA, Clark BJ, Klinge CM (April 2016). „Neue Mechanismen für die DHEA-Wirkung“ . J.Mol. Endokrinol . 56 (3): R139–55. doi : 10.1530/JME-16-0013 . PMID 26908835 .
- Qin JC, Fan L, Qin AP (Mai 2016). „Die Wirkung einer Dehydroepiandrosteron (DHEA)-Supplementierung bei Frauen mit verminderter ovarieller Reserve (DOR) im IVF-Zyklus: Beweise aus einer Meta-Analyse“. J Gynecol Obstet Biol Reprod (Paris) . 46 : 1–7. doi : 10.1016/j.jgyn.2016.01.002 . PMID 27212610 .
- Ohnaka K (Juli 2016). „[Dehydroepiandrosteron (DHEA) und Knochenstoffwechsel]“ . Clin Calcium (auf Japanisch). 26 (7): 987–93. PMID 27346309 .
- Handelsman DJ, Matsumoto AM, Gerrard DF (Januar 2017). „Dopingstatus der DHEA-Behandlung für weibliche Athleten mit Nebenniereninsuffizienz“. Clin J Sport Med . 27 (1): 78–85. doi : 10.1097/JSM.000000000000300 . PMID 26844622 . S2CID 24168278 .
- Qin JC, Fan L, Qin AP (Januar 2017). „Die Wirkung einer Dehydroepiandrosteron (DHEA)-Supplementierung bei Frauen mit verminderter ovarieller Reserve (DOR) im IVF-Zyklus: Beweise aus einer Meta-Analyse“. J Gynecol Obstet Hum Reprod . 46 (1): 1–7. doi : 10.1016/j.jgyn.2016.01.002 . PMID 28403950 .
- Labrie F, Martel C, Bélanger A, Pelletier G (April 2017). "Androgene bei Frauen werden im Wesentlichen aus DHEA in jedem peripheren Gewebe gemäß der Intrakrinologie hergestellt". J. Steroid Biochem. Mol.-Nr. Biol . 168 : 9–18. doi : 10.1016/j.jsbmb.2016.12.007 . PMID 28153489 . S2CID 2620899 .
- Triantafyllidou O, Sigalos G, Vlahos N (Juni 2017). „Dehydroepiandrosteron (DHEA) Supplementation und IVF-Ergebnis bei armen Respondern“. Hum Fertil (Camb) . 20 (2): 80–87. doi : 10.1080/14647273.2016.1262065 . PMID 27927044 . S2CID 3425127 .
- Archer DF, Labrie F, Montesino M, Martel C (November 2017). „Vergleich von intravaginalen 6,5 mg (0,50%) Prasteron, 0,3 mg konjugierten Östrogenen und 10 μg Östradiol bei Symptomen einer vulvovaginalen Atrophie“. J. Steroid Biochem. Mol.-Nr. Biol . 174 : 1–8. doi : 10.1016/j.jsbmb.2017.03.014 . PMID 28323042 . S2CID 140206697 .

